填空题 较易0.85 引用1 组卷217
已知:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=Q。其平衡常数随温度变化如下表所示:
回答下列问题:
(1)上述反应的化学平衡常数表达式为_______ ,该反应的Q_______ (填“>”或“<”)0。
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=_______ 。
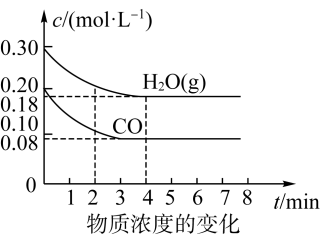
(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为_______ 。(提示:利用平衡常数,三段式计算)
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:_______ (填“能”或“不能”)。理由是_______ 。
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=

(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:
21-22高二上·江苏扬州·阶段练习
类题推荐
已知:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________。该反应的Q______0(填“>”或“<”)。
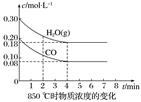
(2)850 ℃时在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4 min时平均反应速率v(CO)=____________。
(3)若在500 ℃时进行。且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为 。
(4)若在850 ℃时进行,设起始时CO和H2O(g)共为1 mol,其中H2O(g)的体积分数为x,平衡时CO的_________________转化率为y,试推导y与x之间的关系________。
 CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________。该反应的Q______0(填“>”或“<”)。

(2)850 ℃时在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4 min时平均反应速率v(CO)=____________。
(3)若在500 ℃时进行。且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为 。
(4)若在850 ℃时进行,设起始时CO和H2O(g)共为1 mol,其中H2O(g)的体积分数为x,平衡时CO的_________________转化率为y,试推导y与x之间的关系________。
已知:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
请回答下列问题:
(1)上述反应的化学平衡常数表达式为___ ,该反应的Q__ 0(填“>”或“<”)。
(2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)浓度变化如图所示,则0~4 min时平均反应速率v(CO)=__ 。
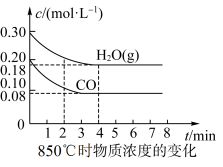
(3)400℃时,压强恒定的密闭容器中进行上述反应。该可逆反应达到平衡的标志是__ (填字母)。
A.v逆(H2)=v正(CO)
B.容器的总体积不再随时间而变化
C.混合气体的密度不再随时间变化
D.CO、H2O、CO2、H2的分子数之比为1∶1∶1∶1
(4)若在500℃时进行,且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为__ 。
(5)若在850℃时进行,某时刻时测得CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1mol、0.5mol、0.6mol、0.6mol,此时V正__ V逆。(填“>”或“<”或“=”)
(6)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中水蒸气的体积分数为x,平衡时CO的转化率为y,试推导y随x变化的函数关系式为__ 。
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为
(2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)浓度变化如图所示,则0~4 min时平均反应速率v(CO)=

(3)400℃时,压强恒定的密闭容器中进行上述反应。该可逆反应达到平衡的标志是
A.v逆(H2)=v正(CO)
B.容器的总体积不再随时间而变化
C.混合气体的密度不再随时间变化
D.CO、H2O、CO2、H2的分子数之比为1∶1∶1∶1
(4)若在500℃时进行,且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为
(5)若在850℃时进行,某时刻时测得CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1mol、0.5mol、0.6mol、0.6mol,此时V正
(6)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中水蒸气的体积分数为x,平衡时CO的转化率为y,试推导y随x变化的函数关系式为
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g) 十H2O (g)⇌CO2 (g) 十 H2(g) ; △H<0
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率v(CO2)=______ mol·L-1·min-1
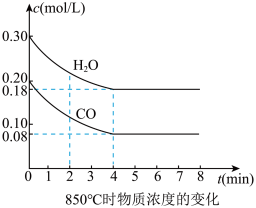
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如表:
① 计算t1℃该反应的平衡常数为K = ______ 。
② t1℃时,反应在5min~6min间,平衡______ 移动(填向左、向右或不 ),若在第5分钟改变一种条件达到第6分钟的浓度,改变的条件是______ 。
(3)t2℃时,化学反应CO (g) + H2O (g)⇌CO2 (g) + H2(g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃______ 850℃, 判断依据是:______
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率v(CO2)=

(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如表:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
② t1℃时,反应在5min~6min间,平衡
(3)t2℃时,化学反应CO (g) + H2O (g)⇌CO2 (g) + H2(g)的平衡浓度符合c(CO2)·c(H2)=2 c(CO)·c(H2O),则t2℃
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


