解答题-结构与性质 较易0.85 引用1 组卷214
钛硅分子筛是一种新型固体催化剂,可催化合成重要有机合成活性试剂甲乙酮肟(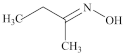 )。回答下列问题:
)。回答下列问题:
(1)基态硅原子的核外电子空间运动状态有___________ 种。
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为___________ ,氮原子的杂化方式为___________ ,C=N与C-C键夹角___________ (填“<”“>”或“=”)C=N与N-O键夹角。
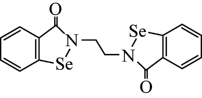
(3) 和
和 均是制备钛硅分子筛的重要中间体。
均是制备钛硅分子筛的重要中间体。
① 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为___________ ,其空间构型为___________ 。
② 与金属
与金属 在高温条件下可反应生成
在高温条件下可反应生成 ,
, 中
中 极易被氧化,还原性很强。试解释
极易被氧化,还原性很强。试解释 还原性强的原因
还原性强的原因___________ 。
 )。回答下列问题:
)。回答下列问题:(1)基态硅原子的核外电子空间运动状态有
(2)甲乙酮肟中同周期三种元素电负性由大到小的顺序为
(3)
①
②
21-22高三下·福建·开学考试
类题推荐
碳的多种同素异形体及一系列化合物广泛应用于科研、医疗、工农业生产等领域。回答下列问题:
(1)写出基态C原子核外电子排布的轨道表示式________________________ 。
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多, C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是 (填编号)。
(3)TiO2与光气COCl2反应可用于制取四氯化钛。COCl2中σ键和π键的数目比为________ , 其空间构型为_______________ 。
(4)甲乙酮肟( )中同周期三种元素电负性由大到小的顺序为
)中同周期三种元素电负性由大到小的顺序为___________________ ,氮原子的杂化方式为________________ ,C=N与C-C键夹角_______________ C=N与N-O键夹角(填“<”“>”或“=”)。
(5)CO2分子中并不存在简单的“碳氧双键”,除了正常的σ键,还有两个方向互相垂直的大π键(每个O原子上还有一对孤对电子),则每个大π键中有______ 个电子。
(6)从化学键的角度解释石墨的熔点高于金刚石的原因_________________ 。
(7)利用皮秒激光照射悬浮在甲醇溶液中的多壁碳纳米管可以合成T-碳。T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示[其中图(a)、(b) 为T-碳的晶胞和晶胞俯视图,图(c)为金刚石晶胞]。
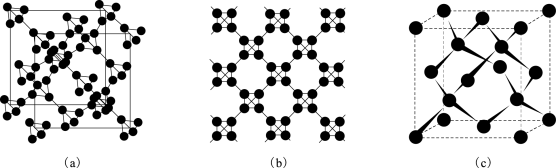
一个T-碳晶胞中含有____ 个碳原子。 T-碳的密度非常小,是金刚石的一半,则T-碳晶胞的棱长和金刚石晶胞的棱长之比为________________ 。
(1)写出基态C原子核外电子排布的轨道表示式
(2)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多, C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是 (填编号)。
| A.CH4 | B.CH2=CH2 | C.CH ≡ CH | D.苯 |
(4)甲乙酮肟(
 )中同周期三种元素电负性由大到小的顺序为
)中同周期三种元素电负性由大到小的顺序为(5)CO2分子中并不存在简单的“碳氧双键”,除了正常的σ键,还有两个方向互相垂直的大π键(每个O原子上还有一对孤对电子),则每个大π键中有
(6)从化学键的角度解释石墨的熔点高于金刚石的原因
(7)利用皮秒激光照射悬浮在甲醇溶液中的多壁碳纳米管可以合成T-碳。T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示[其中图(a)、(b) 为T-碳的晶胞和晶胞俯视图,图(c)为金刚石晶胞]。

一个T-碳晶胞中含有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
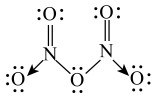 ,而固态N2O5则由一种直线形的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为
,而固态N2O5则由一种直线形的阳离子X与一种平面正三角形的阴离子Y构成,X的化学式为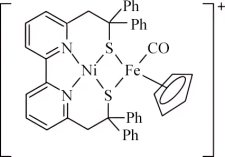
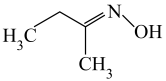 )是一种重要有机合成活性试剂。其中,
)是一种重要有机合成活性试剂。其中,