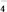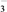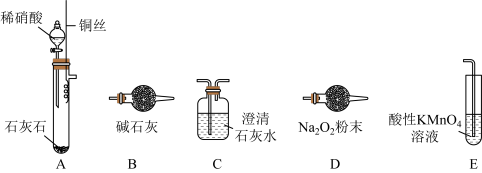解答题-实验探究题 适中0.65 引用2 组卷880
硝酸是一种重要的化工原料。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出发生反应的离子方程式_______ ;反应停止后,仍有铜剩余,加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是_______ (填字母)。
A.还原剂 B.氧化剂 C.酸化 D.提供热能
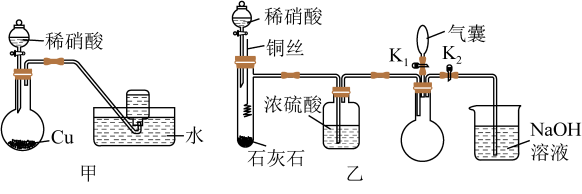
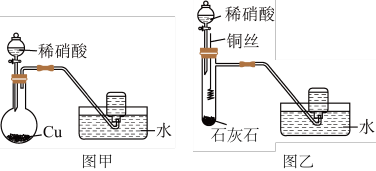
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。
①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了 ,因为集气瓶中无色气体的来源可能是
,因为集气瓶中无色气体的来源可能是_______ 。
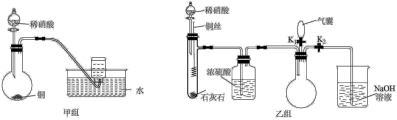
②乙组实验的操作步骤是:
a.关闭活塞 ,打开活塞
,打开活塞 ,将过量稀硝酸加入石灰石中。该操作的目的是
,将过量稀硝酸加入石灰石中。该操作的目的是_______ 。
b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是 ,应进行的操作是
,应进行的操作是_______ ,观察到的现象是_______ 。
(3)某些资料认为 不能与
不能与 反应。某同学提出质疑,他认为
反应。某同学提出质疑,他认为 易与
易与 发生反应,应该更容易被
发生反应,应该更容易被 氧化。
氧化。
查阅资料:a. ;
;
b.
c.酸性条件下, 能被
能被 氧化生成
氧化生成 。
。
该同学在乙组实验的基础上,用如图所示装置探究 与
与 的反成。
的反成。
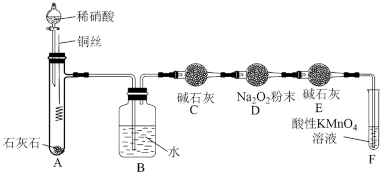
①C装置中碱石灰的作用是_______ ;F装置中反应的离子方程式为_______ 。
②充分反应后,检验D装置中是否发生反应a的实验操作及现象是_______ 。
(1)在浓硝酸中加入铜片,开始反应时有红棕色气体产生,写出发生反应的离子方程式
A.还原剂 B.氧化剂 C.酸化 D.提供热能
(2)实验小组用稀硝酸和铜分别设计了甲、乙两组实验(装置如图所示,夹持仪器已略去)。
①甲组实验中,同学们观察到集气瓶中收集到无色气体。部分同学认为该实验不能确定是铜与稀硝酸反应生成了

②乙组实验的操作步骤是:
a.关闭活塞
b.待石灰石反应完全后,将铜丝插入过量稀硝酸中。
c.一段时间后,欲证明圆底烧瓶中收集列的无色气体是
(3)某些资料认为
查阅资料:a.
b.
c.酸性条件下,
该同学在乙组实验的基础上,用如图所示装置探究

①C装置中碱石灰的作用是
②充分反应后,检验D装置中是否发生反应a的实验操作及现象是
21-22高一上·陕西渭南·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网