解答题-实验探究题 适中0.65 引用2 组卷569
硫酸是重要的化工原料,某兴趣小组对浓硫酸的性质进行如下探究。
(1)棉布上滴浓H2SO4后破洞。体现了浓H2SO4的_______ (填“脱水”“吸水”或“强氧化”、下同)性;在冷的浓H2SO4中放入铁片无明显现象,体现了浓H2SO4的_______ 性。
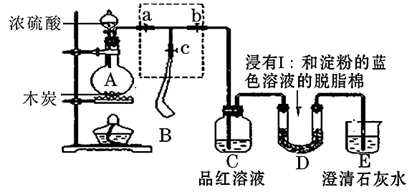
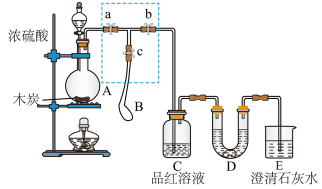
为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊。(已知淀粉溶液遇I2变蓝)
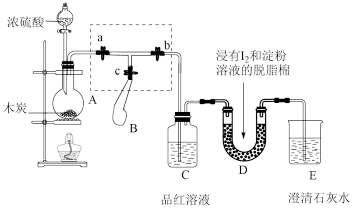
(2)装置A中发生反应的化学方程式为_______ 。
(3)实验时,装置C中的现象为_______ 。
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,正确的操作顺序是_______ (填序号)。
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b
③打开止水夹a和c,关闭止水夹b
(5)若要检验浓硫酸与木炭在加热条件下生成的水蒸气,可在装置_______ 之间加上一个盛有无水CuSO4的硬质玻璃管。
(6)当D中产生_______ 现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;写出D中发生反应的化学方程式_______ 。
(7)当D中反应转移电子0.3mol时,参加反应的气体体积(标准状况下)为_______ L。
(1)棉布上滴浓H2SO4后破洞。体现了浓H2SO4的
为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊。(已知淀粉溶液遇I2变蓝)

(2)装置A中发生反应的化学方程式为
(3)实验时,装置C中的现象为
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,正确的操作顺序是
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b
③打开止水夹a和c,关闭止水夹b
(5)若要检验浓硫酸与木炭在加热条件下生成的水蒸气,可在装置
(6)当D中产生
(7)当D中反应转移电子0.3mol时,参加反应的气体体积(标准状况下)为
21-22高一上·陕西西安·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网