解答题-原理综合题 适中0.65 引用1 组卷44
氨是一种重要的工业品,也可作燃料电池的原料。回答下列问题:
(1)NH3的电子式为_______ ,Sb与N位于同一主族,核电荷数为51,其在元素周期表中的位置为_______ 。
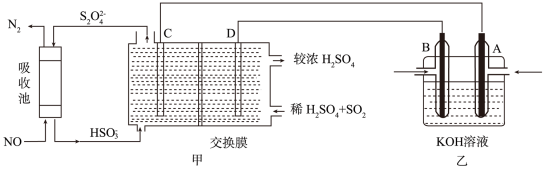
(2) 等利用BaZrO3基质子陶瓷膜反应器,通过电化学方法合成氨的装置如图所示。
等利用BaZrO3基质子陶瓷膜反应器,通过电化学方法合成氨的装置如图所示。

①电解质溶液可能为_______ (填“稀H2SO4”或“KOH”)溶液。
②有NH3生成的电极为该电池的_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
(3)N2H4(联氨)可由NH3与NaClO溶液制得,该反应的离子方程式为_______ 。
(4)标准状况下,将由11.2LN2和33.6LH2组成的混合气体通入一体积为1L的恒容密闭容器中,在一定条件下发生反应:N2+3H2 2NH3。5min后反应达到平衡,此时容器压强为起始压强的
2NH3。5min后反应达到平衡,此时容器压强为起始压强的 ,0~5min内υ(NH3)
,0~5min内υ(NH3)_______ mol∙L−1∙min−1,N2的转化率为_______ 。
(1)NH3的电子式为
(2)

①电解质溶液可能为
②有NH3生成的电极为该电池的
(3)N2H4(联氨)可由NH3与NaClO溶液制得,该反应的离子方程式为
(4)标准状况下,将由11.2LN2和33.6LH2组成的混合气体通入一体积为1L的恒容密闭容器中,在一定条件下发生反应:N2+3H2
21-22高二上·四川南充·阶段练习
类题推荐
完成下列填空
(1)天然气使用前需要脱硫,发生下列反应:
①H2S(g)+ O2(g)=SO2(g)+H2O(g) △H1
O2(g)=SO2(g)+H2O(g) △H1
②2H2S(g)+SO2(g)= S2(g)+2H2O(g) △H2
S2(g)+2H2O(g) △H2
③H2S(g)+ O2(g)=S(g)+H2O(g) △H3
O2(g)=S(g)+H2O(g) △H3
④2S(g)=S2(g) △H4
则△H4的正确表达式为___________
(2)甲醇是一种重要的工业品,也可作燃料电池的原料。回答下列问题:
①CH3OH的电子式为___________ ;Sn与C位于同一主族,核电荷数为50,其在元素周期表中的位置为___________ 。
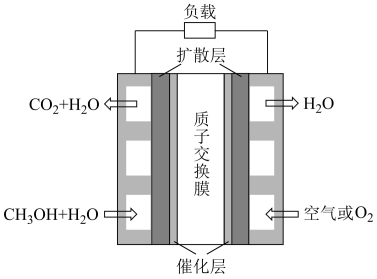
②微型直接甲醇燃料电池是通过MEMS工艺制作的一种微型能源装置,具有结构简单、体积小、质量轻、比能量密度高、环境污染小等优点,其装置如图所示:
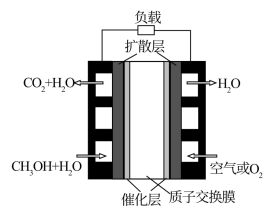
通入CH3OH和H2O的电极为该电池的___________ (填“正极”或“负极”),该电极上的电极反应式为___________ 。
③电解质溶液可能为___________ (填“稀H2SO4”或“KOH溶液”)。
(3)T℃时,将0.75 mol CO2和2.25 mol H2的混合气体通入体积为1 L的恒容密闭容器中,在一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的
CH3OH(g)+H2O(g),5min后反应达到平衡,此时容器压强为起始压强的 。平衡时,CH3OH的物质的量为
。平衡时,CH3OH的物质的量为___________ mol。
(1)天然气使用前需要脱硫,发生下列反应:
①H2S(g)+
②2H2S(g)+SO2(g)=
③H2S(g)+
④2S(g)=S2(g) △H4
则△H4的正确表达式为___________
| A.△H4= | B.△H4= |
| C.△H4= | D.△H4= |
①CH3OH的电子式为
②微型直接甲醇燃料电池是通过MEMS工艺制作的一种微型能源装置,具有结构简单、体积小、质量轻、比能量密度高、环境污染小等优点,其装置如图所示:

通入CH3OH和H2O的电极为该电池的
③电解质溶液可能为
(3)T℃时,将0.75 mol CO2和2.25 mol H2的混合气体通入体积为1 L的恒容密闭容器中,在一定条件下发生反应:CO2(g)+3H2(g)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网