填空题 适中0.65 引用1 组卷270
按要求完成下列问题。
(1)对于反应2NO(g)+O2(g)⇌2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如下图)。
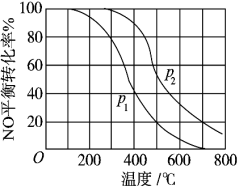
①比较P1、P2的大小关系:P1___________ P2(填“>”、“<”或“=”)。
②该反应的平衡常数K的表达式为___________ ,随温度升高,该反应平衡常数变化的趋势是___________ 。(填“增大”、“减小”或“不变”)。
(2)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g) ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10−3。请回答:
①若该反应是在恒容条件下进行,判断该反应达到平衡的标志为___________ 。
A.消耗1molN2同时生成1molO2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v正(N2)=v逆(NO)
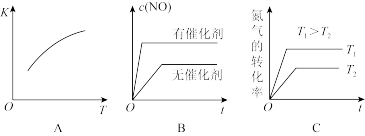
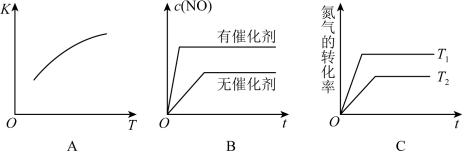
②将N2、O2的混合气体充入某密闭容器中,下图变化趋势正确的是___________ 。(填字母)。
③该温度下,在某时刻测得容器内N2、O2、NO的浓度分别为2.5×10−1mol/L、4.0×10−2mol/L和3.0×10−3mol/L,则此时反应___________ 移动(填“正向”“逆向”或“不”);
(3)已知:N2O4(g)⇌2NO2(g) ∆H=+52.70kJ/mol。
①在恒温、恒容的已达平衡的密闭容器中,再向容器内充入1molN2O4(g),并达新平衡,下列说法正确的___________
a.N2O4(g)的转化率增大 b.新平衡N2O4的百分含量比原平衡大
c.平衡常数K减小 d.新平衡透明容器的气体颜色比原平衡还要深
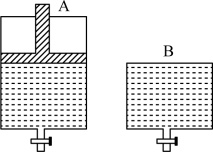
②一定温度下,若将3molN2O4气体置入开始体积为V但体积可变的等压密闭容器中(如图A),达平衡后容器体积增大至1.5V。若在另一个体积也为V但体积不变的密闭容器中(如图B)加入___________ molNO2,达平衡后A、B两容器的NO2百分含量相等。
(1)对于反应2NO(g)+O2(g)⇌2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如下图)。

①比较P1、P2的大小关系:P1
②该反应的平衡常数K的表达式为
(2)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g) ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10−3。请回答:
①若该反应是在恒容条件下进行,判断该反应达到平衡的标志为
A.消耗1molN2同时生成1molO2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v正(N2)=v逆(NO)
②将N2、O2的混合气体充入某密闭容器中,下图变化趋势正确的是

③该温度下,在某时刻测得容器内N2、O2、NO的浓度分别为2.5×10−1mol/L、4.0×10−2mol/L和3.0×10−3mol/L,则此时反应
(3)已知:N2O4(g)⇌2NO2(g) ∆H=+52.70kJ/mol。
①在恒温、恒容的已达平衡的密闭容器中,再向容器内充入1molN2O4(g),并达新平衡,下列说法正确的
a.N2O4(g)的转化率增大 b.新平衡N2O4的百分含量比原平衡大
c.平衡常数K减小 d.新平衡透明容器的气体颜色比原平衡还要深
②一定温度下,若将3molN2O4气体置入开始体积为V但体积可变的等压密闭容器中(如图A),达平衡后容器体积增大至1.5V。若在另一个体积也为V但体积不变的密闭容器中(如图B)加入

21-22高二上·辽宁大连·期中
类题推荐
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g)ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为___________ ,N2的转化率是___________ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下图变化趋势正确的是______ (填字母序号)。
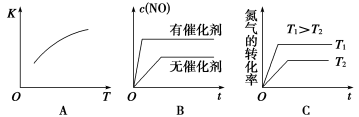
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数________ (填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应___________ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是___________ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
| A.消耗1molN2同时生成1molO2 | B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 | D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g) ΔH>0,已知该反应在240℃,平衡常数K=6.4×10-3。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率___________ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志___________。
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是___________ (填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数___________ 。(填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应___________ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是___________ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志___________。
| A.消耗1molN2同时生成1molO2 | B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 | D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2NO(g),
2NO(g),