填空题 适中0.65 引用1 组卷44
反应热产生的原因:以H2(g)+Cl2(g)=2HCl(g)为例说明_______ 。
21-22高二·全国·课前预习
类题推荐
回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。(填“A”或“B”)

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
则生成1mol水可以放出热量 _______ kJ
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:_______ (填序号)。
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
②乙中能量转化的主要形式为_______ 。
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是_______ ,当电路中转移0.25 mol电子时,消耗负极材料的质量为_______ g。
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
②乙中能量转化的主要形式为
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是
研究化学反应中的能量变化,有助于帮助我们更好地利用化学反应为生产和生活服务。
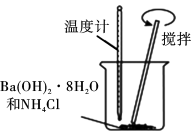
(1)某同学设计如图所示的实验探究化学反应中的能量变化。实验中发现反应后温度降低,该反应中反应物的总能量_______ (填“高于”、“等于”或“低于”)生成物的总能量。
(2)从断键和成键的角度分析反应 中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成
中能量的变化。断开1mol化学键需要的能量如表所示,则该反应生成
_______ (填“吸收”或“释放”)的能量为_______ kJ。
(3)利用Fe和 溶液的反应设计原电池,则正极材料为
溶液的反应设计原电池,则正极材料为_______ ,负极材料为_______ 。
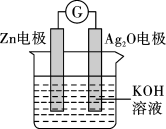
(4)银锌电池是一种常见的化学电源,反应原理为: ,其工作示意图如图所示。在装置中
,其工作示意图如图所示。在装置中 作
作_______ (填“正”或“负”)极,溶液中的 向
向_______ (填“Zn”或“ ”)电极移动;负极的电极反应式为
”)电极移动;负极的电极反应式为_______ 。
(1)某同学设计如图所示的实验探究化学反应中的能量变化。实验中发现反应后温度降低,该反应中反应物的总能量

(2)从断键和成键的角度分析反应
| 化学键 | H-H | O=O | H-O |
| 键能 | 436 | 496 | 463 |
(3)利用Fe和
(4)银锌电池是一种常见的化学电源,反应原理为:

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




