解答题-工业流程题 适中0.65 引用6 组卷699
金属回收与利用有利于环境保护,镉可用于制造体积小和电容量大的电池。铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质,湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
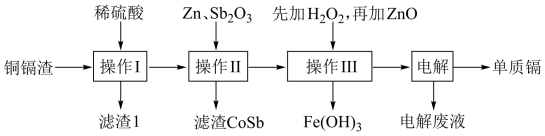
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
(1)滤渣Ⅰ可用硫酸酸化的双氧水浸取经结晶制取胆矾,试写出浸取过程离子方程式___________ 。
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:___________ 。
(3)操作Ⅲ加入ZnO控制反应液的pH范围为___________ ;若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以检验:___________ 。
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为___________ ;电解废液最好在___________ 加入循环利用。(选择“操作I”、“操作Ⅱ”、“操作Ⅲ”、“电解”工序名称填入横线上)
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为___________ ;如果用生石灰处理含Cd2+(2.88×10-4mol/L)的电解废液。常温下,当pH=10时,镉的去除率为___________ 。(用百分数表达,小数点后两位有效数字。已知常温下,Ksp[Cd(OH)2]=7.2×10-15)

下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.7 | 6.3 | 7.5 |
| 沉淀完全的pH | 2.8 | 8.4 | 9.3 |
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:
(3)操作Ⅲ加入ZnO控制反应液的pH范围为
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为
2021·甘肃金昌·模拟预测
类题推荐
铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
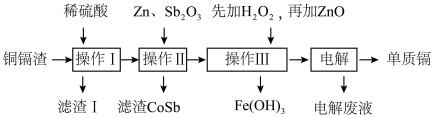
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol·L-1)。
(1)酸浸时粉碎铜镉渣的目的是_______ 。
(2)操作Ⅰ产生的滤渣Ⅰ的主要成分为_______ (填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为_______ 。
②再加入ZnO控制反应液的pH,pH范围为_______ 。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe2+。请设计实验方案加以鉴别:_______ 。
(4)处理含Cd2+废水时常向其中加入碳酸钙实现沉淀转化,该沉淀转化反应的离子方程式为_______ ;除去工业废水中的Cd2+时,若反应达到平衡后溶液中c(Ca2+)=0.1 mol·L-1,则溶液中c(Cd2+)=_______ mol·L-1[已知25℃,Ksp(CdCO3)=5.6×10-12,Ksp(CaCO3)=2.8×10-9]。

表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol·L-1)。
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是
(2)操作Ⅰ产生的滤渣Ⅰ的主要成分为
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为
②再加入ZnO控制反应液的pH,pH范围为
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe2+。请设计实验方案加以鉴别:
(4)处理含Cd2+废水时常向其中加入碳酸钙实现沉淀转化,该沉淀转化反应的离子方程式为
金属回收与利用有利于环境保护。以某废渣(主要含Cd,还含少量Zn、Cu、Fe、Co等单质)为原料回收Cd,工艺流程如图所示:

已知几种金属离子沉淀的pH如表所示。
请回答下列问题:
(1)“酸浸”中加入稀硫酸,充分反应后过滤得到滤渣1的主要成分是_______ (填化学式)。
(2)“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的离子方程式:_______ 。若将该反应设计成原电池,锌在_______ 极发生反应。
(3)“除铁”时,先加入KMnO4氧化Fe2+ ,后加ZnO调溶液pH。加入ZnO调节溶液pH的范围为_______ 。 过滤,得滤渣2为MnO2和_______ (填化学式)。
(4)“电解”过程中以石墨为电极得到粗镉的电解总反应的化学方程式为_______ 。
(5)已知:常温下,Ksp[Cd(OH)2]≈2.0×10-16.如果用生石灰处理含Cd2+的电解废液,当pH=10时,c(Cd2+)=_______ mol/L。

已知几种金属离子沉淀的pH如表所示。
| 离子 | Fe3+ | Fe2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 完全沉淀的pH | 3.3 | 9.9 | ? |
请回答下列问题:
(1)“酸浸”中加入稀硫酸,充分反应后过滤得到滤渣1的主要成分是
(2)“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的离子方程式:
(3)“除铁”时,先加入KMnO4氧化Fe2+ ,后加ZnO调溶液pH。加入ZnO调节溶液pH的范围为
(4)“电解”过程中以石墨为电极得到粗镉的电解总反应的化学方程式为
(5)已知:常温下,Ksp[Cd(OH)2]≈2.0×10-16.如果用生石灰处理含Cd2+的电解废液,当pH=10时,c(Cd2+)=
铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
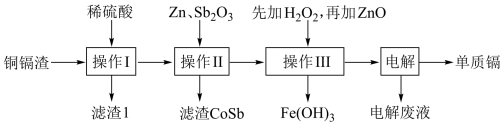
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
(1)酸浸时,粉碎铜镉渣的目的是_________ 。
(2)操作Ⅰ产生的滤渣Ⅰ主要成分为_________ (填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为_________ 。
②再加入ZnO控制反应液的pH,pH范围为_________ 。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以检验:_________ 。
(4)处理含镉(Cd2+)废水常用加入CaCO3实现沉淀转化,若反应达到平衡后,溶液中c(Ca2+)=0.1mol·L-1,溶液中c(Cd2+)=_________ mol·L-1[已知25℃,Ksp(CdCO3)=5.6×10-12,Ksp(CaCO3)=2.8×10-9]。

表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的Ph | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时,粉碎铜镉渣的目的是
(2)操作Ⅰ产生的滤渣Ⅰ主要成分为
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为
②再加入ZnO控制反应液的pH,pH范围为
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以检验:
(4)处理含镉(Cd2+)废水常用加入CaCO3实现沉淀转化,若反应达到平衡后,溶液中c(Ca2+)=0.1mol·L-1,溶液中c(Cd2+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


