多选题 较难0.4 引用1 组卷77
室温下,向20.00mL0.10mol·L-1HX溶液中滴加0.10mol·L-1NaOH溶液,溶液pH随 变化关系如图所示。下列说法正确的是
变化关系如图所示。下列说法正确的是
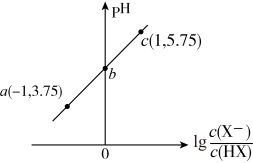

| A.室温下,HX的电离平衡常数Ka的数量级为10-5 |
| B.b点时,加入NaOH溶液的体积为10mL |
| C.c点溶液中:c(Na+)=10c(HX) |
| D.溶液中水的电离程度:c>b>a |
21-22高二上·湖南永州·期末
类题推荐
已知 。室温下,向20.00mL 0.10mol·L−1 HX溶液中逐滴滴加0.10mol·L−1 NaOH溶液,溶液pH随
。室温下,向20.00mL 0.10mol·L−1 HX溶液中逐滴滴加0.10mol·L−1 NaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
变化关系如图所示。下列说法错误的是
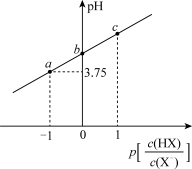

| A.当 |
| B.当 |
| C.当加入10.00mL NaOH溶液时:c(Na+)+c(OH-)=c(H+)+c(HX) |
| D.如图所示各点对应溶液中水电离出来的H+浓度:a<b<c |
已知:p[c(HX)/c(X-)]= -lg[c(HX)/c(X-)]。室温下,向0. 1 mol/LHX溶液中滴加0.1mol/L NaOH溶液,溶液pH随p[c(HX)/c(X-)]变化关系如图。下列说法不正确的是:
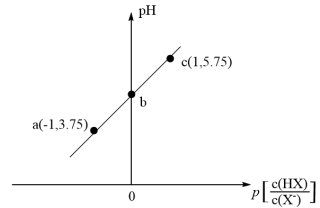

| A.溶液中水的电离程度:a>b>c | B.图中b点坐标为(0,4.75) |
| C.c点溶液中:c(Na+) =l0c(HX) | D.室温下HX的电离常数为10-4.75 |
常温下,在20 mL a mol·L−1的HX溶液中滴加0.1 mol·L−1的NaOH溶液,溶液中水电离出c(H+)的pH=−lgc(H+)水与所加NaOH溶液体积的关系如图所示(已知lg5=0.7):
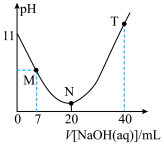
下列说法中不正确的是

下列说法中不正确的是
| A.a=0.1,Ka(HX)的数量级为10−5 |
| B.M点:c(X−)>c(Na+)>c(H+)>c(OH−) |
| C.在N点时,溶液的pH约为8.85 |
| D.T点对应的溶液中2c(Na+)=c(X−)+c(HX) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


