解答题-原理综合题 较易0.85 引用1 组卷76
某化学兴趣小组进行了实验:向2支试管中分别加入0.5 g Na2CO3固体和0.5 gNaHCO3固体,再分别加入30 mL 0.3 mol·L-1盐酸,充分反应后,用手触摸试管,明显感觉到加Na2CO3固体的试管变热了,加NaHCO3固体的试管变冷了。甲同学由此得出结论:CO (aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO
(aq) +2H+ (aq)=H2O(1) +CO2(g)△H1<0, HCO (aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq)=H2O(1) +CO2(g) △H2>0。回答下列问题:
(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?_____ (填“甲”或“乙”) ,理由是_______ 。
(2)查阅资料:
反应I :CO (aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
(aq) +2H+ (aq)=H2O(l) +CO2(g) △H1= -12.14kJ· mol-1;
反应II :HCO (aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
(aq) +H+ (aq)=H2O(l) +CO2(g) △H2= +12.64 kJ·mol-1。
向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
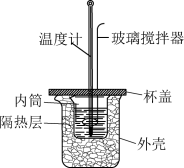
(3)该化学兴趣小组用如图所示装置设计了实验,验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。
表格一:
表格二:
表格三:
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是_______________ 。
②表格二对应实验得出的结论是________________ 。
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1______ (填“>”、“< ”或“=”,下同) △H3,△H2______ △H4。
(1)乙同学认为该实验不一定能得到甲同学的结论,你支持谁的观点?
(2)查阅资料:
反应I :CO
反应II :HCO
向V mLc mol· L-1碳酸钠溶液中,逐滴加入2V mLc mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是 (填标号)。
A.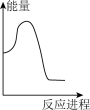 | B.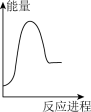 | C.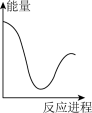 | D.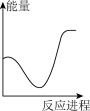 |

表格一:
试剂1 | 试剂2混合前温度/℃ | 混合后温度/℃ |
0.5 g Na2CO3 | 40mL HCl 19.0 | 21.7 |
0.5 g NaHCO3 | 40 mL HCl 19.0 | 18.1 |
表格二:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22. 3 | 19.0 | 10mL H2O 19.0 | 19.0 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL H2O 19.0 | 19.0 |
表格三:
试剂1 | 试剂2混合 前温度/℃ | 溶解后温 度/℃ | 静置后的 温度/℃ | 试剂3混合 前温度/℃ | 混合后 温度/℃ |
0.5 g Na2CO3 | 10 mL H2O19.0 | 22.3 | 19.0 | 10mL HCl 19.0 | 20.5 |
0.5 g NaHCO3 | 10 mL H2O19.0 | 17.5 | 19.0 | 10 mL HCl19.0 | 18.3 |
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是
②表格二对应实验得出的结论是
③反应III:Na2CO3(s) +2H+ (aq)=2Na+ (aq) +H2O(1) +CO2(g) △H3;
反应IV:NaHCO3(s)+ H+ (aq)=Na+ (aq) + H2O(l) +CO2(g) △H4。
则△H1
21-22高三上·福建莆田·阶段练习
类题推荐
A.为探究碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应,某化学兴趣小组进行如下实验。
查阅资料:反应Ⅰ:
 ;
;
反应Ⅱ:

(1)反应Ⅲ:向碳酸钠溶液中滴加少量盐酸生成碳酸氢钠的离子反应的热化学方程式为___________ 。
(2)向 碳酸钠溶液中,逐滴加入
碳酸钠溶液中,逐滴加入 稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是___________(填标号)。
稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是___________(填标号)。
B.实验探究:按表格所示用量,在量热器中将相应试剂混合后测定温度,验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。

表格1:
表格2:
表格3:
(3)表格1实验___________ (填“能”或“否”)验证
 ,
,
 。
。
(4)实验中玻璃搅拌器的使用方法是___________ 。(填标号)
A.顺时针搅拌 B.逆时针搅拌 C.上下拉动
(5)进行表格3操作的目的是___________ 。
(6)结合实验探究所得的结论进行分析判断。
反应Ⅳ:
 ;
;
反应Ⅴ:

则
___________  (填“>”、“<”或“=”,下同),
(填“>”、“<”或“=”,下同),
___________  。
。
查阅资料:反应Ⅰ:
反应Ⅱ:
(1)反应Ⅲ:向碳酸钠溶液中滴加少量盐酸生成碳酸氢钠的离子反应的热化学方程式为
(2)向
A.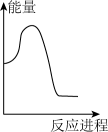 | B.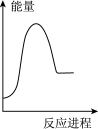 | C.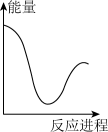 | D.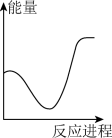 |
B.实验探究:按表格所示用量,在量热器中将相应试剂混合后测定温度,验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。

表格1:
| 试剂1 | 试剂2 | 试剂1和试剂2混合后温度 |
| 19.0℃的40 mL HCl | 21.7℃ | |
| 19.0℃的40 mL HCl | 18.1℃ |
| 试剂1 | 试剂2 | 试剂1溶解于试剂2后的温度 | 静置后混合液的温度 | 试剂3 | 静置后混合液再加入试剂3后的温度 |
| 19.0℃的 | 22.3℃ | 19.0℃ | 19.0℃的10 mL HCl | 20.5℃ | |
| 19.0℃的 | 17.5℃ | 19.0℃ | 19.0℃的10 mL HCl | 18.3℃ |
| 试剂1 | 试剂2 | 试剂1溶解于试剂2后的温度 | 静置后混合液的温度 | 试剂3 | 静置后混合液再加入试剂3后的温度 |
| 19.0℃的 | 22.3℃ | 19.0℃ | 19.0℃的 | 19.0℃ | |
| 19.0℃的 | 17.5℃ | 19.0℃ | 19.0℃的 | 19.0℃ |
(3)表格1实验
(4)实验中玻璃搅拌器的使用方法是
A.顺时针搅拌 B.逆时针搅拌 C.上下拉动
(5)进行表格3操作的目的是
(6)结合实验探究所得的结论进行分析判断。
反应Ⅳ:
反应Ⅴ:
则
碳酸钠和碳酸氢钠是中学化学常见的化合物,某化学兴趣小组对碳酸钠和碳酸氢钠与稀盐酸的反应进行了如下实验:
Ⅰ:验证 和
和 分别与稀盐酸反应的快慢
分别与稀盐酸反应的快慢
向2支具支试管中分别加入0.1 g碳酸钠和0.08 g碳酸氢钠粉末,2支注射器中各抽取5 mL 1 稀盐酸,如图所示,用注射器同压板同时按下注射器活塞,注入稀盐酸,观察现象。
稀盐酸,如图所示,用注射器同压板同时按下注射器活塞,注入稀盐酸,观察现象。
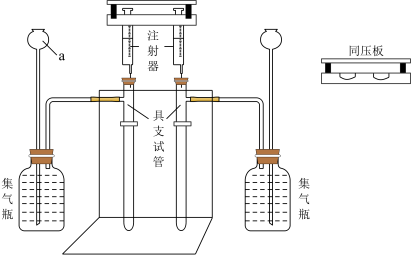
(1)仪器a的名称是_______ 。
(2)加入试剂前需_______ 。
(3)集气瓶中的试剂最优选择是_______ (填标号),使用同压板的优点有_______ (填一条即可)。
A.滴有红墨水的水
B.滴有红墨水的饱和碳酸钠溶液
C.滴有红墨水的饱和碳酸氢钠溶液
(4)为验证 和
和 分别与稀盐酸反应的快慢,需测量的数据是
分别与稀盐酸反应的快慢,需测量的数据是_______ 。
Ⅱ:探究 和
和 与稀盐酸反应的热效应(实验中所用盐酸浓度均为1.0
与稀盐酸反应的热效应(实验中所用盐酸浓度均为1.0  )
)
实验一:向试剂1中加入试剂2,搅拌、测温,记录结果如表所示。
实验二:向试剂3中加入试剂4,搅拌、测温,静置、测温,再加入试剂5,搅拌、测温,记录结果如表所示。
(5)通过实验一的数据计算:(可近似地认为实验中所用溶液的密度、比热容与水的相同,并忽略容器的比热容,水的比热容为 )
)
①

_______ (保留四位有效数字,下同) 。
。
②

_______  。
。
(6)分析实验二可知, 溶于水是
溶于水是_______ (填“放热”或“吸热”,下同)过程, 与稀盐酸的反应是
与稀盐酸的反应是_______ 反应。
(7)该小组同学通过查阅资料发现,实验中测得的 、
、 均偏小,排除实验中的误差,出现该结果的原因可能是
均偏小,排除实验中的误差,出现该结果的原因可能是_______ 。
Ⅰ:验证
向2支具支试管中分别加入0.1 g碳酸钠和0.08 g碳酸氢钠粉末,2支注射器中各抽取5 mL 1

(1)仪器a的名称是
(2)加入试剂前需
(3)集气瓶中的试剂最优选择是
A.滴有红墨水的水
B.滴有红墨水的饱和碳酸钠溶液
C.滴有红墨水的饱和碳酸氢钠溶液
(4)为验证
Ⅱ:探究
实验一:向试剂1中加入试剂2,搅拌、测温,记录结果如表所示。
| 试剂1 | 试剂2混合前的温度/℃ | 混合后最高或最低温度/℃ |
| 1.0 g | 20 mL HCl 22.0 | 25.5 |
| 1.0 g | 20 mL HCl 22.0 | 19.4 |
| 试剂3 | 试剂4温度/C | 溶解后温度/℃ | 静置后温度/℃ | 试剂5温度/℃ | 混合后温度/c |
| 1.0 g | 20 mL | 23.8 | 22.0 | 20 mL HCl 22.0 | 23.5 |
| 1.0 g | 20 mL | 19.5 | 22.0 | 20 mL HCl 22.0 | 21.4 |
①
②
(6)分析实验二可知,
(7)该小组同学通过查阅资料发现,实验中测得的
有这样一个实验:在两支试管中分别加入3mL某浓度的稀盐酸(足量),将两个各装有0.3g NaHCO3和 Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3和Na2CO3同时倒入试管中,观察到现象如右图:

(1)盛______________ (填化学式)的试管中气球变得更大, 大小气球(不计气球的弹力和气体温度影响) 体积之比约为(填最简单整数比)____________ 。
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3粉末的试管变热。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了如下热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3-(aq)+ H+(aq) →H2O(l)+ CO2(g) ΔH1;ΔH1>0
CO32-(aq)+ 2H+(aq) → H2O(l) + CO2(g) ΔH2 ;ΔH2<0
甲同学所作结论的方法是否正确?___________ (填“正确”或“不正确”)。
(3)为研究该反应是吸热还是放热反应,某研究小组以《NaHCO3、Na2CO3 和盐酸反应过程中热效应的研究》为研究课题,进行了如下实验(每次实验各做三次,取平均值):
请你帮助填写相关内容:
该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为______________ 和_______________ ;
(4)通过上述实验可以得出_____________ (填字母编号)。
(5)结论:影响NaHCO3固体与稀盐酸反应的反应热因素有________________________________________________________________________ 。

(1)盛
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3粉末的试管变热。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了如下热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3-(aq)+ H+(aq) →H2O(l)+ CO2(g) ΔH1;ΔH1>0
CO32-(aq)+ 2H+(aq) → H2O(l) + CO2(g) ΔH2 ;ΔH2<0
甲同学所作结论的方法是否正确?
(3)为研究该反应是吸热还是放热反应,某研究小组以《NaHCO3、Na2CO3 和盐酸反应过程中热效应的研究》为研究课题,进行了如下实验(每次实验各做三次,取平均值):
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高 或最低温度 |
| ① | 35mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 3.2 Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10ml水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为
(4)通过上述实验可以得出
| A.NaHCO3的溶解是吸热过程 |
| B.NaHCO3的饱和溶液和盐酸的反应是吸热反应 |
| C.Na2CO3的溶解是放热过程 |
| D.Na2CO3的饱和溶液和盐酸的反应是吸热反应 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


