单选题 较易0.85 引用3 组卷583
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
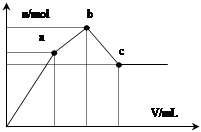
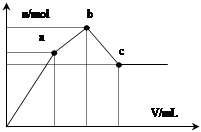
| A.a点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓ |
| B.b点消耗Ba(OH)2溶液体积为200mL |
| C.从a→b 、b→c点过程中发生反应的离子方程式依次为: NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+2H2O |
| D.沉淀的质量:a点>c点 |
12-13高三·河北唐山·阶段练习
类题推荐
向100mL0.1mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是


| A.a点时溶液中所含主要溶质为(NH4)2SO4 |
B.a→b段发生反应的离子方程式是 SO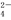 +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.b点为最大沉淀量,对应的纵坐标值为0.02 |
| D.c点加入Ba(OH)2溶液的体积为200 mL |
向100mL1mol·L-1NH4Al(SO4)2溶液中逐滴加入1mol·L-1Ba(OH)2溶液。沉淀总物质的量n随加入Ba(OH)2溶液体积V的变化如图。下列说法错误的是


| A.沉淀质量:b点>a点>c点 |
| B.a点到c点过程中,b点溶液中水的电离程度最小 |
| C.a点离子浓度的大小关系为:[NH |
| D.b点到c点过程中,发生的离子方程式为:Al(OH)3+OH-=AlO |
向100mL0.1mol/L硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol/L Ba(OH)2溶液.随着Ba(OH)2溶液体积V(横坐标)的变化,沉淀总物质的量n的变化如图所示
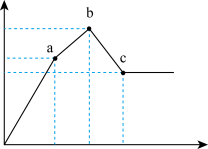
已知铝盐中滴加过量氨水能产生Al(OH)3沉淀,该沉淀遇强碱如NaOH溶液又可溶解。请回答下列问题:
(1)写出b c发生反应的离子方程式:
c发生反应的离子方程式:_______________________________ ;
(2)下列说法正确的是________
(3)写出a b发生反应的离子方程式:
b发生反应的离子方程式:__________________________________ ;
(4)滴加到c点共加入Ba(OH)2溶液的体积为__ mL,b、a两点沉淀的质量差为___ g(精确到0.001).

已知铝盐中滴加过量氨水能产生Al(OH)3沉淀,该沉淀遇强碱如NaOH溶液又可溶解。请回答下列问题:
(1)写出b
(2)下列说法正确的是
| A.a点的溶质为(NH4)2SO4 |
| B.b点溶液中一定存在:c(NH |
| C.b点沉淀为Al(OH)3和BaSO4 |
| D.C点溶液中一定存在:c(AlO |
(4)滴加到c点共加入Ba(OH)2溶液的体积为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


