解答题-工业流程题 较难0.4 引用1 组卷239
某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收镍制备硫酸镍晶体(NiS4·7H2O)。
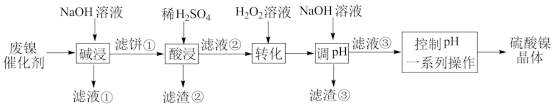
已知某些金属离子开始沉淀和沉淀完全的pH如下:
回答下列问题:
(1)提高“碱浸”速率的有效措施有_______ (任写一种即可);“滤液②”中含有的金属离子有_______ 。
(2)写出“转化”中发生反应的离子方程式_______ 。
(3)若“转化”后溶液中Ni2+浓度为1mol·L-1,则“调pH”应控制的范围为___ 。
(4)获得硫酸镍晶体时,需经过控制pH、_____ 、_____ 过滤等“一系列操作”。
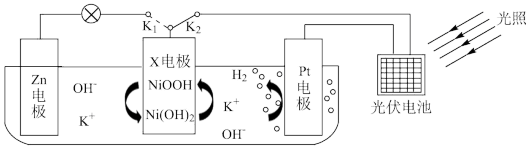
(5)硫酸镍可用来制备新型镍电池电极材料NiOOH,我国科研团队利用该电极材料设计了一种新型能量存储-转化装置(如图)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。供电时,X电极反应式为_______ 。

已知某些金属离子开始沉淀和沉淀完全的pH如下:
| 金属离子 | Ni2+ | A13+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)提高“碱浸”速率的有效措施有
(2)写出“转化”中发生反应的离子方程式
(3)若“转化”后溶液中Ni2+浓度为1mol·L-1,则“调pH”应控制的范围为
(4)获得硫酸镍晶体时,需经过控制pH、
(5)硫酸镍可用来制备新型镍电池电极材料NiOOH,我国科研团队利用该电极材料设计了一种新型能量存储-转化装置(如图)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。供电时,X电极反应式为

21-22高二上·山东滨州·期末
类题推荐
某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

25℃时,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)为了提高金属镍废料浸出的速率,在“碱浸”时可采取的措施有①适当升高温度;②搅拌;③_______ 等。
(2)滤液②中含有的金属离子是_______ 。
(3)“转化”中可替代H2O2的物质是_______ 。若工艺流程改为先“调pH”后 “转化”,即
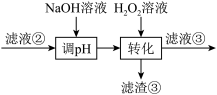 ,
,
则“滤液③”中可能含有的杂质离子为_______ 。
(4)利用上述表格数据,计算Ni(OH)2的Ksp=_______ (列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0mol/L,则“调pH”应控制的pH范围是_______ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。

25℃时,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | A13+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol/L)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)为了提高金属镍废料浸出的速率,在“碱浸”时可采取的措施有①适当升高温度;②搅拌;③
(2)滤液②中含有的金属离子是
(3)“转化”中可替代H2O2的物质是
 ,
,则“滤液③”中可能含有的杂质离子为
(4)利用上述表格数据,计算Ni(OH)2的Ksp=
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)利用上述表格数据,计算Ni(OH)2的Ksp=___ (列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0mol·L−1,则“调pH”应控制的pH范围是___ 。
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式___ 。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L−1)的pH 沉淀完全时(c=1.0×10−5mol·L−1)的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
(1)利用上述表格数据,计算Ni(OH)2的Ksp=
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
镍催化剂的主要成分为Ni,还含有一定量Al、Fe及氧化铁、少量其他不溶性物质,回收废镍催化剂制备硫酸镍晶体(NiSO4·7H2O)的工艺流程如下:
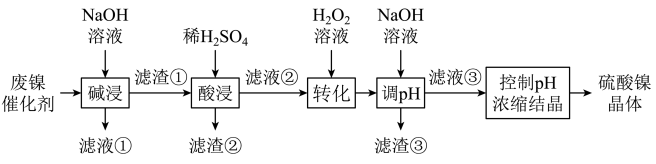
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)提高“碱浸”速率的措施是_______ (任写一点即可)。
(2)“碱浸”发生反应的离子方程式是_______ 。“滤液②”可能含有的金属离子是_______ 。
(3)“转化”步骤中加入H2O2的目的是_______ ,反应的离子方程式是_______ 。
(4)“调pH”时,最适宜的pH范围是_______ 。
(5)“控制pH浓缩结晶”步骤得到硫酸镍晶体(NiSO4·7H2O)的一系列操作是:_______ 、_______ 、过滤、洗涤、干燥;浓缩过程中需用稀硫酸控制pH的目的是_______ 。
(6)已知:NiSO4溶液在强碱性条件下用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH(黑色粉末),该反应的离子方程式为_______ 。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Ni2+ |
| 开始沉淀的pH(c=0.01mol·L-1) | 2.2 | 7.5 | 7.2 |
| 沉淀完全的pH(c=1.0×10-5mol·L-1) | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)提高“碱浸”速率的措施是
(2)“碱浸”发生反应的离子方程式是
(3)“转化”步骤中加入H2O2的目的是
(4)“调pH”时,最适宜的pH范围是
(5)“控制pH浓缩结晶”步骤得到硫酸镍晶体(NiSO4·7H2O)的一系列操作是:
(6)已知:NiSO4溶液在强碱性条件下用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH(黑色粉末),该反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


