解答题-工业流程题 适中0.65 引用1 组卷82
某钴矿石的主要成分有 、
、 、
、 、
、 、
、 和
和 等。由该矿石粉制备
等。由该矿石粉制备 固体的方法如图(部分催化剂已略)。
固体的方法如图(部分催化剂已略)。
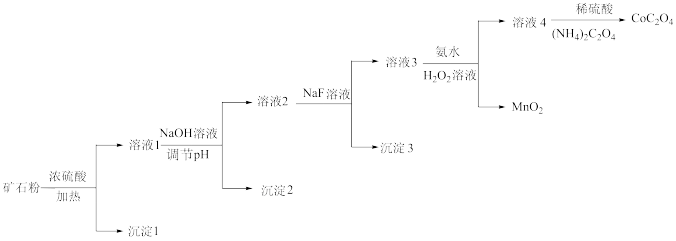
已知:金属离子沉淀的 :
:
(1) 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
(2)向溶液1中加入 溶液,将
溶液,将 转化为
转化为 沉淀,应调节
沉淀,应调节 至少大于
至少大于_______ 。
(3)向溶液2中加入 溶液,去除的离子是
溶液,去除的离子是_______ 。
(4)向溶液3中加入氨水和过氧化氢溶液,将 转化为
转化为 。该反应的离子方程式为:
。该反应的离子方程式为:_______ 。
(5)溶液4中,若将 全部转化为
全部转化为 沉淀,需要消耗
沉淀,需要消耗
_______  。
。
(6)关于上述流程,下列说法正确的是_______ (填序号)。
a.若矿石粉中存在少量 ,经上述流程也可制得纯度相同的
,经上述流程也可制得纯度相同的
b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离

已知:金属离子沉淀的
| 开始沉淀时 | 1.5 | 6.3 | 8.9 | 8.2 | 7.4 |
| 完全沉淀时 | 2.8 | 8.3 | 10.9 | 10.2 | 9.4 |
(2)向溶液1中加入
(3)向溶液2中加入
(4)向溶液3中加入氨水和过氧化氢溶液,将
(5)溶液4中,若将
(6)关于上述流程,下列说法正确的是
a.若矿石粉中存在少量
b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
21-22高三上·辽宁葫芦岛·期末
类题推荐
某含钴矿石的主要成分为Co2O3,含少量Fe2O3、MgO、CaO和SiO2等。由该矿石粉制备CoC2O4固体的方法如下(部分催化剂已略)。
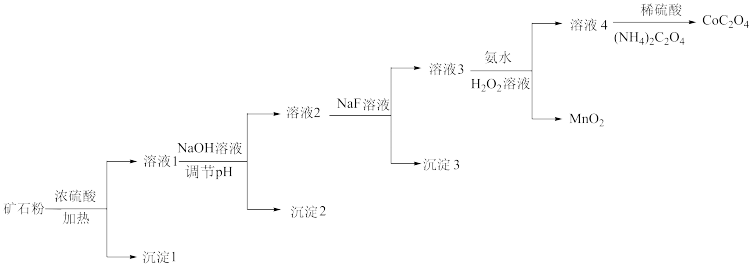
已知金属离子沉淀的pH:
(1)Co2O3溶于浓硫酸,生成Co2+和一种可使带火星的木条复燃的气体,写出该反应的化学方程式___________ 。列举沉淀1所含主要成分的一种用途___________ 。
(2)向溶液1中加入NaOH溶液,将Fe3+转化为Fe(OH)3沉淀,应调节pH范围为___________ 。
(3)向溶液2中加入NaF溶液除去钙、镁离子,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,则溶液3中c(Ca2+)=1.0×10-5mol·L-1时,c(Mg2+)=___________ mol·L-1。
(4)向溶液3中加入氨水和过氧化氢溶液,将Co2+转化为Co(NH3) 。补充下列离子方程式:
。补充下列离子方程式:________
______Co2++________H2O2+______NH3=_____Co(NH3) +_________。
+_________。
(5)溶液4中,若将1molCo(NH3) 全部转化为CoC2O4沉淀,需要消耗(NH4)2C2O4
全部转化为CoC2O4沉淀,需要消耗(NH4)2C2O4___________ mol。
(6)关于上述流程,下列说法正确的是___________ (填序号)。
a.流程中,仅通过调节溶液的pH也可将金属元素完全分离
b.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的CoC2O4
c.向溶液3中加入氨水,作用仅是调节溶液的pH
d.过滤所得CoC2O4晶体用H2C2O4溶液代替蒸馏水洗涤效果更好

已知金属离子沉淀的pH:
| Fe3+ | Mg2+ | Ca2+ | Co2+ | |
| 开始沉淀时 | 1.5 | 8.9 | 9.8 | 7.4 |
| 完全沉淀时 | 2.8 | 10.9 | 12.3 | 9.4 |
(2)向溶液1中加入NaOH溶液,将Fe3+转化为Fe(OH)3沉淀,应调节pH范围为
(3)向溶液2中加入NaF溶液除去钙、镁离子,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,则溶液3中c(Ca2+)=1.0×10-5mol·L-1时,c(Mg2+)=
(4)向溶液3中加入氨水和过氧化氢溶液,将Co2+转化为Co(NH3)
______Co2++________H2O2+______NH3=_____Co(NH3)
(5)溶液4中,若将1molCo(NH3)
(6)关于上述流程,下列说法正确的是
a.流程中,仅通过调节溶液的pH也可将金属元素完全分离
b.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的CoC2O4
c.向溶液3中加入氨水,作用仅是调节溶液的pH
d.过滤所得CoC2O4晶体用H2C2O4溶液代替蒸馏水洗涤效果更好
某钴矿石的主要成分有CoO、Co2O3、MnO、Fe2O3、MgO和SiO2,由该矿石粉制备CoC2O4固体的方法如下(部分催化剂已略)。
(1)原料钴矿石反应前需进行预处理,将钴矿石粉碎成粉末的作用是:_____ 。
(2)加入浓硫酸的目的是将金属氧化物转化为离子的形式,加热时发生的离子反应至少有_____ 个。
(3)沉淀1主要成分的化学式为:_____ 。
(4)向溶液1中加入NaOH溶液,将Fe3+转化为Fe(OH)3沉淀,应调节pH至少大于_____ 。
(5)向溶液2中加入NaF溶液,去除的离子是_____ 。
(6)向溶液3中加入氨水和过氧化氢溶液的目的是氧化,将Co2+转化为Co(NH3) 。其反应的离子方程式为:
。其反应的离子方程式为:_____ 。
(7)溶液4中,若将1molCo3+全部转化为CoC2O4沉淀,需要消耗(NH4)2C2O4_____ mol。
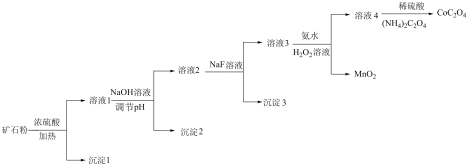
| Fe3+ | Fe2+ | Mg2+ | Mn2+ | Co2+ | |
| 开始沉淀时 | 1.5 | 6.3 | 8.9 | 8.2 | 7.4 |
| 完全沉淀时 | 2.8 | 8.3 | 10.9 | 10.2 | 9.4 |
(2)加入浓硫酸的目的是将金属氧化物转化为离子的形式,加热时发生的离子反应至少有
(3)沉淀1主要成分的化学式为:
(4)向溶液1中加入NaOH溶液,将Fe3+转化为Fe(OH)3沉淀,应调节pH至少大于
(5)向溶液2中加入NaF溶液,去除的离子是
(6)向溶液3中加入氨水和过氧化氢溶液的目的是氧化,将Co2+转化为Co(NH3)
(7)溶液4中,若将1molCo3+全部转化为CoC2O4沉淀,需要消耗(NH4)2C2O4
金属钴是一种非常稀缺的金属之一,具有耐高温、高压的特性,可应用于催化剂。电池方面,电子设备和航空设备中。某钴矿石的主要成分包括 、
、 、
、 和
和 。由该矿石制
。由该矿石制 固体的方法如图(部分分离操作省略):
固体的方法如图(部分分离操作省略):
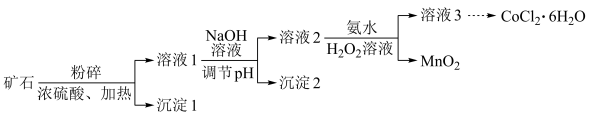
资料:25℃时有关金属离子沉淀的相关PH见下表
(1)上述矿石溶解过程中,粉碎的目的是___________ 。
(2) 溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括
溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括 、
、 和
和___________ 。
(3)沉淀2是___________ ,此时调节溶液的pH范围是___________ 。
(4)①已知:当c(Co2+)≤1×10-5mol/L时可认为 完全沉淀,则
完全沉淀,则
___________ 。
②溶液2中加入氨水和 溶液,发生反应的离子方程式为:
溶液,发生反应的离子方程式为:___________ 。
(5)溶液3中加入 溶液生成
溶液生成 沉淀,沉淀剂若选择
沉淀,沉淀剂若选择 ,所得到的沉淀中可能会混有
,所得到的沉淀中可能会混有___________ 。

资料:25℃时有关金属离子沉淀的相关PH见下表
| 离子 | |||
| 开始沉淀时的PH | 1.9 | 7.15 | 8.2 |
| 沉淀完全时的PH | 2.8 | 9.15 | 10.2 |
(1)上述矿石溶解过程中,粉碎的目的是
(2)
(3)沉淀2是
(4)①已知:当c(Co2+)≤1×10-5mol/L时可认为
②溶液2中加入氨水和
(5)溶液3中加入
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


