解答题-工业流程题 适中0.65 引用5 组卷1452
CoCl2 • 6H2O可用作油漆干燥剂,工艺上可用含钴废料(主要为Co,含少量Fe、Al,有机杂质)为原料来制取CoCl2• 6H2O,以下是制备该物质的一种新工艺流程:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)“焙烧”的目的是___________ 。
(2)①试剂a可选用___________ ;
②“酸浸”时Co转化为Co2+,反应的离子方程式为___________ 。
(3)“氧化”过程中,H2O2的作用:___________ 。
(4)①加入碳酸钠调节pH至b,b的范围是___________ ;
②“滤渣”中所含沉淀成分的化学式为___________ ;
③滤渣经洗涤后,洗涤液与滤液合并,检验滤渣洗涤干净的操作是___________ 。
(5)滤液需加盐酸,其目的是___________ 。
(6)操作I为___________ 、___________ ,过滤,洗涤,干燥。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7.5 | 7.6 | 3.8 |
| 完全沉淀 | 3.2 | 9.7 | 9.2 | 5.2 |
(1)“焙烧”的目的是
(2)①试剂a可选用
②“酸浸”时Co转化为Co2+,反应的离子方程式为
(3)“氧化”过程中,H2O2的作用:
(4)①加入碳酸钠调节pH至b,b的范围是
②“滤渣”中所含沉淀成分的化学式为
③滤渣经洗涤后,洗涤液与滤液合并,检验滤渣洗涤干净的操作是
(5)滤液需加盐酸,其目的是
(6)操作I为
21-22高三上·广东惠州·期末
类题推荐
多彩水泥的添加剂是CoCl2-6H2O。工定是以含钴废料(含少量Fe、Al等杂质制取CoCl2·6H2O的一种新工艺流程如下图:
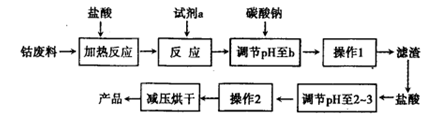
已知:①钴与盐酸反应的化学方程式为:Co+2HCl CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110℃~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)上述流程中的试剂a可能为________ ;其作用是___________________________ ;
(2)加入碳酸钠调节pH至b,b的范围是________________ ;
(3)操作1是_____________ ;滤渣的成分为________________ ;
(4)操作2的过程为蒸发浓缩、______________ 和过滤。
(5)制得的CoCl2·6H2O需减压烘干的原因是____________________________________ 。

已知:①钴与盐酸反应的化学方程式为:Co+2HCl CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110℃~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)上述流程中的试剂a可能为
(2)加入碳酸钠调节pH至b,b的范围是
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
(3)操作1是
(4)操作2的过程为蒸发浓缩、
(5)制得的CoCl2·6H2O需减压烘干的原因是
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
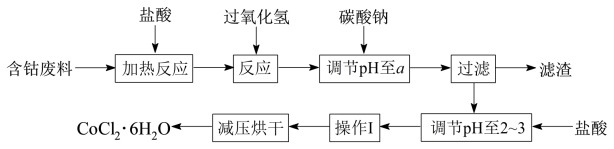
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)加入过氧化氢的作用是(用离子方程式表示)____________________________________ 。
(2)加入碳酸钠调节pH至a得到的滤渣可部分溶于氢氧化钠溶液, a的范围是__________ 。
(3)操作Ⅰ包含3个基本实验操作,它们是__________________________________________ 。
(4)制得的CoCl2·6H2O需减压烘干的原因是_______________________________________ 。

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)加入过氧化氢的作用是(用离子方程式表示)
(2)加入碳酸钠调节pH至a得到的滤渣可部分溶于氢氧化钠溶液, a的范围是
(3)操作Ⅰ包含3个基本实验操作,它们是
(4)制得的CoCl2·6H2O需减压烘干的原因是
CoCl2•6H2O是一种饲料营养强化剂。可由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取,其工艺流程如下:
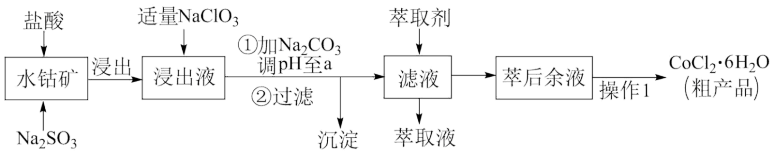
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
③CoCl2•6H2O熔点为86℃,加热至110﹣120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出水钴矿过程中,Fe2O3发生反应的化学方程式为________________________ 。
(2)向浸出液中加入适量NaClO3目的是______________________________________ 。
(3)“加Na2CO3调pH至a”,a=______ ;过滤所得沉淀的主要成分为_________ (填化学式)。
(4)萃取剂对金属离子的萃取与溶液pH的关系如下图所示,向“滤液”中加入该萃取剂的目的是__________ ,使用该萃取剂的最佳pH范围是_____ (填选项字母)
A. 5.0﹣5.5 B. 4.0﹣4.5 C. 3.0﹣3.5 D. 2.0﹣2.5
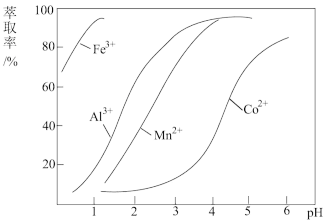
(5)实验操作“操作1”为_______________ 、_________ 、过滤和减压烘干;制得的CoCl2•6H2O在烘干时需减压烘干的原因是________________________ 。

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2•6H2O熔点为86℃,加热至110﹣120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出水钴矿过程中,Fe2O3发生反应的化学方程式为
(2)向浸出液中加入适量NaClO3目的是
(3)“加Na2CO3调pH至a”,a=
(4)萃取剂对金属离子的萃取与溶液pH的关系如下图所示,向“滤液”中加入该萃取剂的目的是
A. 5.0﹣5.5 B. 4.0﹣4.5 C. 3.0﹣3.5 D. 2.0﹣2.5

(5)实验操作“操作1”为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


