填空题 适中0.65 引用13 组卷348
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,以达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如下图。
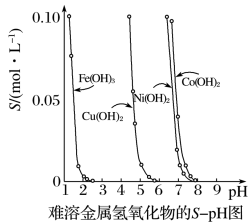
(1)pH=3时溶液中铜元素的主要存在形式是___________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___________ 。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,___________ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___________ 。
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式___________ 。
(5)已知一些难溶物的溶度积常数如下表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___________ 除去它们。(选填序号)
A.NaOH B.FeS C.Na2S

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式
(5)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
11-12高二上·辽宁锦州·期末
类题推荐
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。
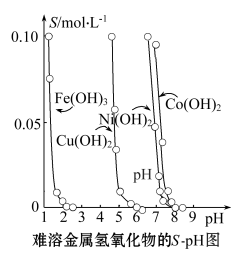
(1)pH=3时溶液中铜元素的主要存在形式是____ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液pH范围在____ 。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,____ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是____ 。
(4)已知一些难溶物的溶度积常数如表。
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的____ (填选项)。
A.NaOH B.FeS C.Na2S
(5)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20。在25℃时,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____ (填化学式)沉淀。
(6)已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K=
Fe3++3H2O的平衡常数K=____ 。
(7)优化反应条件是研究化学反应的重要方向。以硫代硫酸钠与硫酸的反应Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+2H2O为例,探究外界条件对化学反应速率的影响,实验方案如表所示。
表中,a为____ ,b为____ 。实验表明,实验III的反应速率最快,支持这一结论的实验现象为____ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液pH范围在
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表。
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-35 | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 |
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
(5)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20。在25℃时,向浓度均为0.1mol•L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
(6)已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,该温度下反应Fe(OH)3+3H+
(7)优化反应条件是研究化学反应的重要方向。以硫代硫酸钠与硫酸的反应Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+2H2O为例,探究外界条件对化学反应速率的影响,实验方案如表所示。
| 实验序号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | 温度/℃ | ||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | ||
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | 10 | 20 |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 9 | a |
| Ⅲ | 0.1 | b | 0.1 | 1.5 | 9 | 30 |
表中,a为
Ⅰ.金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示。
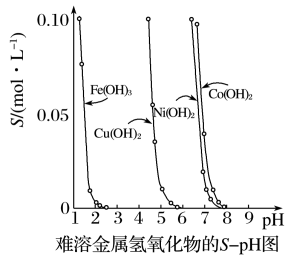
(1)pH=3时溶液中铜元素的主要存在形式是___ (写化学式)。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为___ 。
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是___ 。
(4)已知一些难溶物的溶度积常数如表:
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的___ 除去它们。
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:
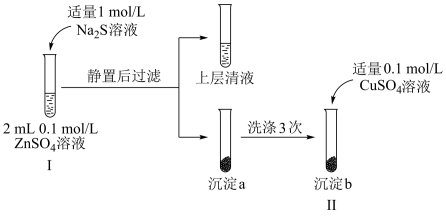
(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:___ 。
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释___ 。
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明___ 。

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.3左右 B.4左右 C.2左右
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,
(4)已知一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
Ⅱ.某小组同学进行如图实验探究:

(5)预通过实验Ⅰ和实验Ⅱ证明Ksp(ZnS)<Ksp(CuS),实验Ⅰ中加入1mol•L-1Na2S的体积范围为:
| 难溶电解质 | 颜色 | Ksp的数值(18~25℃) |
| ZnS | 白色 | 1.6×10-24 |
| CuS | 黑色 | 1.3×10-36 |
| FeS | 黑色 | 6.3×10-18 |
(6)试管Ⅱ中观察到白色沉淀转化为黑色沉淀。请结合化学用语,从平衡移动的角度进行解释
(7)若将沉淀a洗涤3次后,加适量0.1mol/LFeSO4溶液,是否能看到白色沉淀转化为黑色沉淀,请结合计算予以说明
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



