解答题-原理综合题 适中0.65 引用2 组卷208
尿素[CO(NH2)2],又称碳酰胺,是目前含氨量较高的氮肥,适用于各种土壤和植物。
已知:
①
②
③
(1)请写出由N2、H2和CO2合成尿素的热化学方程式:_______ 。
(2)相比③,若②的反应速率更快,下列示意图_______(填标号)最能体现②③反应过程的能量变化。
(3)在某温度下,将NH3和CO2以物质的量之比2∶1置于一恒容密闭容器中反应: ,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
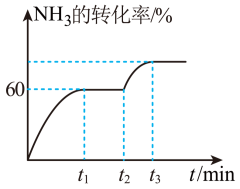
①下列说法能判断该反应达到平衡状态的是_______ (填标号)。
A.容器压强不变
B.消耗1 mol CO2时,生成1 mol H2O
C.容器内n(C)与n(N)的比值不发生变化
D.混合气体的平均摩尔质量不变
②t1时反应达到平衡,CO2的体积分数为_______ (保留三位有效数字),c(NH3):c(CO2):c(H2O)=_______ ;平衡常数Kp=_______  (Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
③向平衡后的反应体系中再通入2 molNH3,Kp将_______ (填“增大”、“减小”或“不变”)。
④图中t2时,NH3的转化率发生改变,此时改变的反应条件是_______ (请写出任意一条)。
已知:
①
②
③
(1)请写出由N2、H2和CO2合成尿素的热化学方程式:
(2)相比③,若②的反应速率更快,下列示意图_______(填标号)最能体现②③反应过程的能量变化。
A.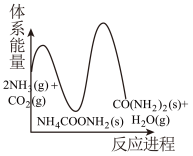 | B.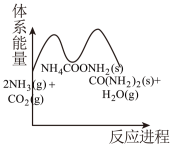 |
C.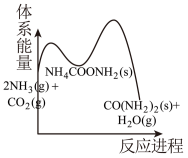 | D.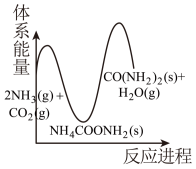 |

①下列说法能判断该反应达到平衡状态的是
A.容器压强不变
B.消耗1 mol CO2时,生成1 mol H2O
C.容器内n(C)与n(N)的比值不发生变化
D.混合气体的平均摩尔质量不变
②t1时反应达到平衡,CO2的体积分数为
③向平衡后的反应体系中再通入2 molNH3,Kp将
④图中t2时,NH3的转化率发生改变,此时改变的反应条件是
21-22高二上·河北保定·期末
类题推荐
CO2综合利用是降低碳排放的有效手段,有利于实现碳中和目标。下列是CO2综合利用的化学方法,回答下列问题:
(1)用氨水吸收CO2制化肥(NH4HCO3)。
①已知:NH3·H2O(aq)= (aq)+OH-(aq) ΔH1=akJ·mol-1
(aq)+OH-(aq) ΔH1=akJ·mol-1
CO2(g)+H2O(l)=H2CO3(aq) ΔH2=bkJ·mol-1
H2CO3(aq)+OH-(aq)= (aq)+H2O(l) ΔH3=ckJ·mol-1
(aq)+H2O(l) ΔH3=ckJ·mol-1
则利用NH3·H2O吸收CO2制备NH4HCO3的热化学方程式为_______ 。
②已知常温下相关数据如表:
则反应 +
+ +H2O⇌NH3·H2O+H2CO3的平衡常数K=
+H2O⇌NH3·H2O+H2CO3的平衡常数K=_______ 。
③分别用不同pH的吸收剂吸收烟气中的CO2,CO2脱除效率与吸收剂的pH关系如图1所示,若烟气中CO2的含量(体积分数)为15%,烟气通入氨水的流量为0.065m3·h-1(标准状况),用pH为12.81的氨水吸收烟气30min,则脱除的CO2的物质的量最多为_______ (精确到0.01)。

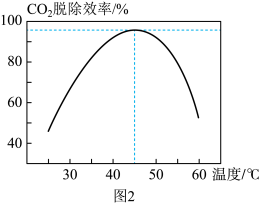
④CO2脱除效率与温度的关系如图2所示,高于45℃时,CO2脱除效率降低的原因可能是_______ (答出一条即可)。
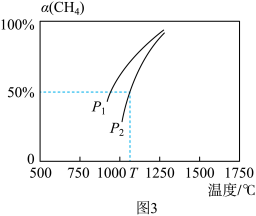
(2)用CO2和天然气可以制备CO和H2:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)。密闭容器中浓度均为0.1mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图3所示,则压强p1_______ p2(填“>”或“<”)。若p2=3MPa,则T℃时该反应的平衡常数Kp=_______ MPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)CO2和H2在一定条件下合成甲醇。在2L恒容密闭容器中充入总物质的量为6mol的CO2和H2,发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),改变氢碳比[n(H2)/n(CO2)],在不同温度下反应达到平衡状态,测得的实验数据如下表。
①氢碳比为1.5,温度为500K,判断该可逆反应达到平衡状态的依据是_______ (填标号)。
A.在相同时间段内,CH3OH的生成速率和CO2的消耗速率相等
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.CH3OH、H2O、CO2、H2的浓度都不再发生变化
②在700K、氢碳比为3.0条件下,若5min时反应达到平衡状态,则0~5min内用H2表示的平均反应速率为_______ 。
(1)用氨水吸收CO2制化肥(NH4HCO3)。
①已知:NH3·H2O(aq)=
CO2(g)+H2O(l)=H2CO3(aq) ΔH2=bkJ·mol-1
H2CO3(aq)+OH-(aq)=
则利用NH3·H2O吸收CO2制备NH4HCO3的热化学方程式为
②已知常温下相关数据如表:
| Kb(NH3·H2O) | 2.0×10-5 |
| Ka1(H2CO3) | 5.0×10-7 |
| Ka2(H2CO3) | 4.0×10-11 |
则反应
③分别用不同pH的吸收剂吸收烟气中的CO2,CO2脱除效率与吸收剂的pH关系如图1所示,若烟气中CO2的含量(体积分数)为15%,烟气通入氨水的流量为0.065m3·h-1(标准状况),用pH为12.81的氨水吸收烟气30min,则脱除的CO2的物质的量最多为

④CO2脱除效率与温度的关系如图2所示,高于45℃时,CO2脱除效率降低的原因可能是

(2)用CO2和天然气可以制备CO和H2:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)。密闭容器中浓度均为0.1mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图3所示,则压强p1

(3)CO2和H2在一定条件下合成甲醇。在2L恒容密闭容器中充入总物质的量为6mol的CO2和H2,发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),改变氢碳比[n(H2)/n(CO2)],在不同温度下反应达到平衡状态,测得的实验数据如下表。
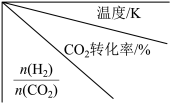 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 40 | 22 |
①氢碳比为1.5,温度为500K,判断该可逆反应达到平衡状态的依据是
A.在相同时间段内,CH3OH的生成速率和CO2的消耗速率相等
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.CH3OH、H2O、CO2、H2的浓度都不再发生变化
②在700K、氢碳比为3.0条件下,若5min时反应达到平衡状态,则0~5min内用H2表示的平均反应速率为
碳能源一直是人类赖以生存的主要能源。
I.已知:C(s)的燃烧热(△H)为-393.5kJ·mol-1;CO(g)的燃烧热(△H)为-283.0kJ·mol-1
(1)反应: △H=
△H=___________ kJ·mol-1,在___________ (填“较高”或“较低”)温度下有利于该反应的自发进行。
II.高温下,向容积为2L的恒容密闭容器中加入一定量的CO2和足量的C,发生反应: ,CO2和CO的物质的量n随时间t的变化关系如图所示:
,CO2和CO的物质的量n随时间t的变化关系如图所示:
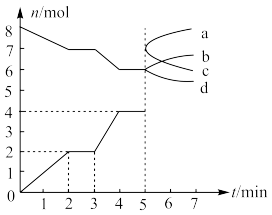
(2)下列叙述能说明该反应已达到平衡状态的是___________(填标号)。
(3)0~2min内,用CO表示的平均反应速率为___________ mol·L-1·min-1
(4)2~3min内,该反应的平衡常数K=___________ mol·L-1
(5)3min末改变的条件是_______ ,再次达到平衡时测得容器内总压强为3MPa,此时,该反应的平衡常数Kp=________ MPa(Kp为用平衡分压代替浓度的平衡常数,分压=总物质的量分数)。
(6)5min时再充入一定量的CO,则表示CO2和CO的物质的量变化的曲线分别为___________ 和___________ (填标号)。
(7)7min时若再加入一定量的C,则CO2的平衡转化率将___________ (填“增大”、“减小”或“不变”,下同),若再充入一定量的CO2,则CO2的平衡转化率将___________ 。
I.已知:C(s)的燃烧热(△H)为-393.5kJ·mol-1;CO(g)的燃烧热(△H)为-283.0kJ·mol-1
(1)反应:
II.高温下,向容积为2L的恒容密闭容器中加入一定量的CO2和足量的C,发生反应:

(2)下列叙述能说明该反应已达到平衡状态的是___________(填标号)。
| A.容器内压强保持不变 |
| B.CO2(g)与CO(g)的物质的量之比为1:2 |
| C.气体的密度保持不变 |
| D.气体的平均相对分子质量保持不变 |
(4)2~3min内,该反应的平衡常数K=
(5)3min末改变的条件是
(6)5min时再充入一定量的CO,则表示CO2和CO的物质的量变化的曲线分别为
(7)7min时若再加入一定量的C,则CO2的平衡转化率将
在工业上,常用CO和H2合成甲醇,其相关的反应原理方程式为:CO(g)+2H2(g) CH3OH(g) △H
CH3OH(g) △H
已知:①CO(g)+ O2(g)= CO2(g) △H1= a kJ/mol
O2(g)= CO2(g) △H1= a kJ/mol
②H2(g)+ O2(g)=H2O(g) △H2= b kJ/mol
O2(g)=H2O(g) △H2= b kJ/mol
③CH3OH(g)+ O2(g)=CO2(g)+ 2H2O(g) △H3= c kJ/mol
O2(g)=CO2(g)+ 2H2O(g) △H3= c kJ/mol
回答下列问题:
(1)△H=___________ kJ/mol 。
(2)能说明反应CO(g)+2H2(g) CH3OH(g)已达平衡状态的是___________(填字母)。
CH3OH(g)已达平衡状态的是___________(填字母)。
(3)在T1℃时,体积为2L的恒容容器中充人物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图1所示。

①当起始 =2,经过5min达到平衡,CO的转化率为60%,则0~5min内平均反应速率v(H2)
=2,经过5min达到平衡,CO的转化率为60%,则0~5min内平均反应速率v(H2)___________ 。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将___________ (选填“增大”、“减小”或“不变”);
②当起始 =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的___________ 点(选填“D”、“E”或“F”) 。
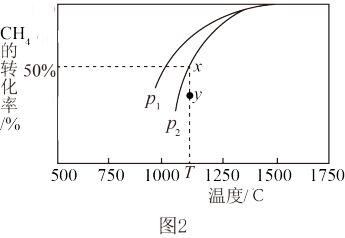
(4)已知CO2(g)+CH4(g) 2CO(g)+2H2(g)。在密闭容器中有浓度均为0.1mol•L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图2,则压强P1
2CO(g)+2H2(g)。在密闭容器中有浓度均为0.1mol•L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图2,则压强P1___________ P2(选填“>” “<” 或“=”);当压强为P2时,在y点:v(正)___________ v(逆)(选填“大于”、“小于”或“等于”)。若P2=3MPa且在恒压体系中发生,则T℃时该反应的平衡常数Kp = ___________ MPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
已知:①CO(g)+
②H2(g)+
③CH3OH(g)+
回答下列问题:
(1)△H=
(2)能说明反应CO(g)+2H2(g)
| A.单位时间内生成1mol CH3OH(g)的同时消耗了1mol CO(g) |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.在恒温恒压的容器中,气体的平均摩尔质量不再变化 |

①当起始
②当起始
(4)已知CO2(g)+CH4(g)

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


