解答题-原理综合题 适中0.65 引用1 组卷26
回答下列问题
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
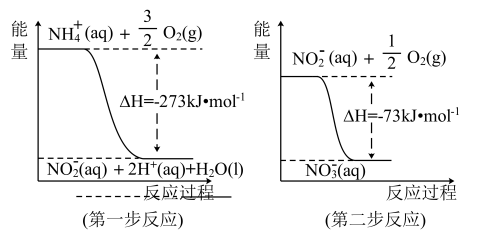
①第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
②1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
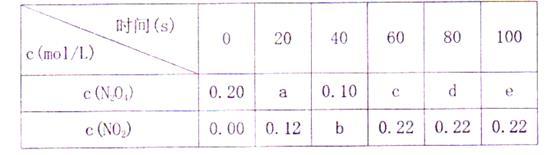
(2)在80℃时,将0.4mol的N2O4(无色)气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。该反应的化学方程式为N2O4⇌2NO2。
①0~20s内N2O4的平均反应速率为_______ 。
②在80℃时N2O4的转化率为_______ 。
③写出恒温恒容下,能判断该反应达到平衡状态的依据_______ 。(写出1条即可)
(1)在微生物作用的条件下,NH

①第一步反应是
②1 mol NH
(2)在80℃时,将0.4mol的N2O4(无色)气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
①0~20s内N2O4的平均反应速率为
②在80℃时N2O4的转化率为
③写出恒温恒容下,能判断该反应达到平衡状态的依据
21-22高二上·内蒙古通辽·期中
类题推荐
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。该反应的化学方程式为N2O4 2NO2。
2NO2。
①0~20s内N2O4的平均反应速率为______________ 。
②该反应的平衡常数表达式K=______________ ,在80℃时该反应的平衡常数K值为____ (保留2位小数)。
③下列说法正确的是_____________ 。
A.温度越高,K值越大,N2O4的转化率越高
B.加压,平衡逆向移动,气体颜色变浅
C.增大N2O4的浓度,新平衡建立过程中正反应速率不断加快
D.起始条件相同,将等量的N2O4分别在A、B两个相同的容器中反应建立平衡,A保持恒温、恒容;B保持恒温、恒压,达到平衡后,A中的N2O4平衡转化率小于B
④写出恒温恒容下,能判断该反应达到平衡状态的依据_____________ 、_____________ 。(写出2条即可)
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。该反应的化学方程式为N2O4
 2NO2。
2NO2。①0~20s内N2O4的平均反应速率为
②该反应的平衡常数表达式K=
③下列说法正确的是
A.温度越高,K值越大,N2O4的转化率越高
B.加压,平衡逆向移动,气体颜色变浅
C.增大N2O4的浓度,新平衡建立过程中正反应速率不断加快
D.起始条件相同,将等量的N2O4分别在A、B两个相同的容器中反应建立平衡,A保持恒温、恒容;B保持恒温、恒压,达到平衡后,A中的N2O4平衡转化率小于B
④写出恒温恒容下,能判断该反应达到平衡状态的依据
在80℃时,将0.40 mol的四氧化二氮气体充入2 L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100 s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为_______ 。
(2)20 s时,N2O4的浓度为_______ mol·L-1,0-20 s内N2O4的平均反应速率为_______ 。
(3)该反应的平衡常数表达式K=_______ ,在80℃时该反应的平衡常数K值为_______ (保留两位小数)。
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L-1 | 0.20 | a | 0.10 | c | d | e |
| c(NO2)/mol·L-1 | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100 s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为
(2)20 s时,N2O4的浓度为
(3)该反应的平衡常数表达式K=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网