解答题-结构与性质 较难0.4 引用8 组卷654
硅烷SiH4可用于制造高纯硅。采用硅化镁法制备SiH4的化学方程式如下:Mg2Si+4NH4Cl+8NH3=SiH4+2MgCl2·6NH3
(1)硅在元素周期表中的位置是___________ ,基态硅原子占据的最高能级的符号是___________ 。
(2)①SiH4的电子式是___________ 。
②SiH4的沸点比CH4的___________ 。(填“高”或“低”),原因是___________ 。
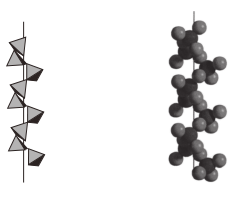
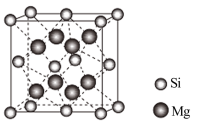
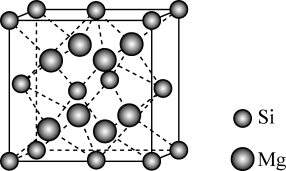
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于___________ 晶体(填晶体类型),一种SiO2晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链(如图)。其中Si原子的杂化轨道类型是___________ 。___________ 个紧邻的Mg原子。已知Mg2Si的晶胞边长为acm,阿伏加德罗常数的值为NA,则Mg2Si晶体的密度为___________ g·cm-3。
(1)硅在元素周期表中的位置是
(2)①SiH4的电子式是
②SiH4的沸点比CH4的
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于
21-22高三上·北京西城·期末
类题推荐
I.硅烷SiH4可用于制造高纯硅。采用硅化镁法制备SiH4的化学方程式如下:Mg2Si+4NH4Cl+8NH3==SiH4+2MgCl2·6NH3。
(1)基态硅原子占据的最高能级的符号是____ 。
(2)①SiH4的电子式是____ 。
②SiH4的沸点比CH4的_____ (填“高”或“低”),原因是____ 。
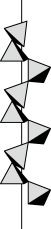
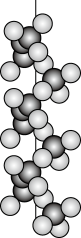
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于____ 晶体(填晶体类型),一种SiO2晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链(如图)。其中Si原子的杂化轨道类型是____ 。
II.W、X、Y、Z为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为3s23p4,X的电离能数据如表所示。
(4)Y元素在元素周期表中的位置是____ ,X元素的最高正化合价是____ 。
(5)下列事实能用元素周期律解释的是____ (填字母序号)。
a.W可用于制备活泼金属钾
b.Y的气态氢化物的稳定性小于H2O
c.将Z单质通入Na2S溶液中,溶液变浑浊
d.Y的氧化物对应的水化物H2YO4的酸性比H2SiO3强
(1)基态硅原子占据的最高能级的符号是
(2)①SiH4的电子式是
②SiH4的沸点比CH4的
(3)Mg2Si可由Mg和SiO2反应制得。晶体SiO2属于


II.W、X、Y、Z为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为3s23p4,X的电离能数据如表所示。
| 电离能 | I1 | I2 | I3 | I4 | … |
| Ia/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | … |
(5)下列事实能用元素周期律解释的是
a.W可用于制备活泼金属钾
b.Y的气态氢化物的稳定性小于H2O
c.将Z单质通入Na2S溶液中,溶液变浑浊
d.Y的氧化物对应的水化物H2YO4的酸性比H2SiO3强
火星岩石含有大量氧化物,如Fe2O3、Al2O3,MgO、CaO、Na2O、SiO2、H2O等。
(1)表中的氧化物中偏向共价晶体的过渡晶体是____ (填化学式)。
(2)基态铁元素的原子最高能级电子云轮廓为____ 形。
(3)Al2O3与NaOH溶液反应生成的[Al(OH)4]-离子中Al的杂化类型是____ ;Al和O构成的空间构型是____ 。
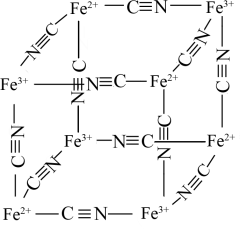
(4)4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]↓(普鲁士蓝),该反应可检验溶液中Fe3+,如图是普鲁士蓝 晶胞的结构,与CN-形成配位键的是
晶胞的结构,与CN-形成配位键的是____ (填Fe2+或Fe3+);CN-离子中σ键与π键的个数比是___ ;晶胞中与一个Fe3+距离相等的N有____ 个。
(5)一种SiO2晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链如图所示。其中Si原子的杂化轨道类型是____ 。

(6)写出SiCl4的电子式:____ ,H2还原气态SiCl4可制得纯硅,1100℃时每生成0.56kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___ 。
(1)表中的氧化物中偏向共价晶体的过渡晶体是
| 氧化物 | Na2O | MgO | Al2O3 | SiO2 |
| 离子键的百分数 | 62% | 50% | 41% | 33% |
(3)Al2O3与NaOH溶液反应生成的[Al(OH)4]-离子中Al的杂化类型是
(4)4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]↓(普鲁士蓝),该反应可检验溶液中Fe3+,如图是普鲁士蓝

(5)一种SiO2晶体的结构中有顶角相连的硅氧四面体形成螺旋上升的长链如图所示。其中Si原子的杂化轨道类型是

(6)写出SiCl4的电子式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

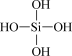 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。

