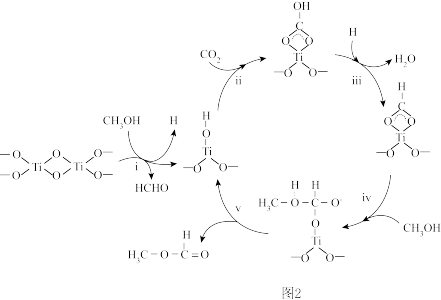
(1)合成氨。一种合成氮的新工艺如图所示,工作时,使用熔融的电解质通过两步铁基循环实现氨的合成。
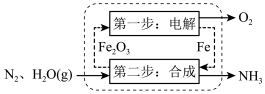
“合成”步骤的化学反应方程式为
(2)氮氧化物制备。将氨催化氧化后,生成
当改变压强、温度时,
| 压强 | 温度 | |||
| 1 | 30 | 12.4 | 248 | 2830 |
| 90 | 25.3 | 508 | 5760 | |
| 8 | 30 | 0.19 | 3.88 | 36.6 |
| 90 | 0.59 | 7.86 | 74 | |
①增大压强,总反应速率
②升高温度,总反应速率
(3)已知
①代表
②假设平衡时体系的总压为
(4)硝酸制备。已知
(1)在一定温度下,氨气溶于水的过程及其平衡常数为:
其中P为
(2)氨在催化氧化反应时发生如下反应:
I.
II.
III.
①反应I在常压下自发进行的条件是
②将一定比例的
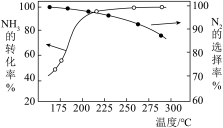
下列说法正确的是
A.其他条件不变,升高温度,
B.其他条件不变,在175~300℃范围,随温度的升高,出口处
C.催化氧化除去尾气中的
D.随温度的升高,
(3)
I.
II.
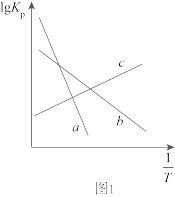
已知:i.决定
ii.
①请在图中画出

②某工业制硝酸流程中,进入反应塔的混合气体中
| 压强 | 温度/℃ | |||
| 50% | 90% | 98% | ||
| 1.0 | 30 | 12 | 250 | 2830 |
| 90 | 25 | 510 | 5760 | |
硝酸是基本化学工业的重要产品之一、
(1)已知:N2(g)+O2(g)=2NO(g);ΔH=+180.5kJ·mol-1
2H2(g)+O2(g)=2H2O(g);ΔH=-483.6kJ·mol-1
N2(g)+3H2(g)=2NH3(g);ΔH=-92.4kJ·mol-1
则4NH3(g)+5O2(g)=4NO(g)+6H2O(g)的ΔH=
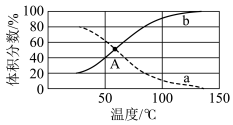
(2)生产硝酸的第二步反应是2NO+O2=2NO2,在0.1MPa和0.8MPa压强下,NO的平衡转化率α随温度的变化如图所示,反应在400℃、0.8Mpa时的α=
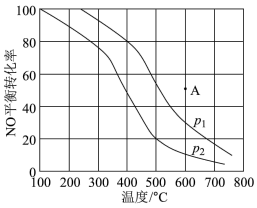
(3)将amolNO,bmolO2通入反应器中,在温度T,压强P条件下进行反应。平衡时,若NO的转化率为m,则NO2的分压为
(4)研究表明NO和O2的反应分两步进行
①2NO=(NO)2ΔH<0
②(NO)2+O2=2NO2ΔH<0
NO和O2反应速率公式为v=k·K·p2(NO)·p(O2),K为反应①的平衡常数,k为反应②速率常数(k随温度T升高而增大)。当其他条件不变时,研究NO达到一定转化率时,温度与时间的关系如下表所示。
压强/(×105pa) | 温度/℃ | NO达到一定转化率所需时间/s | ||
50% | 90% | 98% | ||
1 | 30 | 12.4 | 248 | 2830 |
90 | 25.3 | 508 | 5760 | |
8 | 30 | 0.19 | 3.88 | 36.4 |
90 | 0.59 | 7.86 | 74 | |
根据信息,对于反应:2NO+O2=2NO2,当其他条件一定时,温度对反应速率的影响是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网