填空题 适中0.65 引用2 组卷182
2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是84消毒液,可以说化学让生活更美好。下图为84消毒液说明书。请回答下列问题。
(1)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25g·L-1计算,该消毒液的NaClO的物质的量浓度是___________ 。
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:___________ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___________ ,从氧化还原角度分析Cl2表现了___________ 性。
(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)___________ (已知酸性:H2CO3>HClO>HCO )。
)。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会___________ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g·L-1~60.00g·L-1 | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1∶200水溶液 餐饮具、瓜果等1∶100水溶液 |
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:
(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
21-22高一上·湖南湘潭·阶段练习
类题推荐
新冠肺炎使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。图为84消毒液说明书,请回答下列问题。
(1)①洁厕剂主要成分为稀盐酸,用化学方程式解释注意事项中“不可与洁厕剂混合使用”的原因 _______ 。
②Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉或84消毒液,主要目的_______ 。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.提高氯的质量分数,有利于漂白、消毒
(2)某小组在实验室制备84消毒液,并进行性质探究。
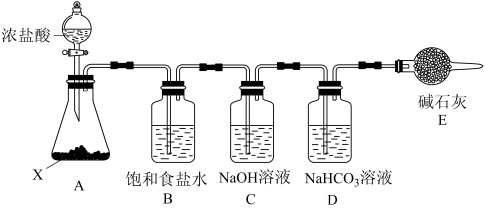
①装置 的名称是
的名称是_______ 。
②能否撤去装置B并说明理由_______ 。
③已知酸性:H2CO3>HClO>HCO ,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式
,已知氯气与NaHCO3溶液反应的氧化产物中Cl为+1价,请写出该反应的化学方程式_______ 。
(3)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25 g/L计算,该消毒液的NaClO的物质的量浓度是_______ mol·L-1。
| 84消毒液说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00 g/L~60.00 g/L | |
| 注意事项 | 不可与洁厕剂或其他消毒液混合使用 | |
| 用法用量 | 稀释后洗刷白色衣物、浴缸等1:200水溶液,餐饮具,瓜果等1:100水溶液 |
②Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉或84消毒液,主要目的
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.提高氯的质量分数,有利于漂白、消毒
(2)某小组在实验室制备84消毒液,并进行性质探究。

①装置
②能否撤去装置B并说明理由
③已知酸性:H2CO3>HClO>HCO
(3)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25 g/L计算,该消毒液的NaClO的物质的量浓度是
2020年突如其来的“新冠病毒”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉、二氧化氯都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84“消毒液,可以说化学让生活更美好。
图为“84”消毒液说明书。
请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式_______ , 若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO 和NaClO3的混合液。当混合液中Cl-和 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为_______ 。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目_______ 。
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐( ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是_______ (填字母)。
a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为: +FeS2+H+
+FeS2+H+  ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式_______ 。
图为“84”消毒液说明书。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~ 60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1: 200水溶液餐饮具,瓜果等1: 100 水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(
a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为:
“84消毒液”是一种以NaClO为有效成分的高效消毒剂,在新冠肺炎防治中被广泛用于宾馆、旅游、医院、家庭等的卫生消毒。
Ⅰ.如表为“84”消毒液说明书,请回答下列问题。
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式___ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___ ,从氧化还原角度分析Cl2表现了___ 性。
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是___ (用离子方程式表达)。(已知:酸性:H2CO3>HClO>HCO ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是___ 。
Ⅱ.某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
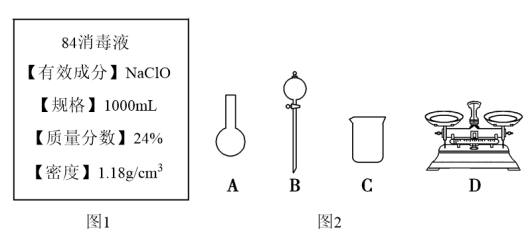
(3)此“84消毒液”的物质的量浓度约为___ mol·L-1。(计算结果保留一位小数)
(4)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL该消毒液。
①如图2所示的仪器中配制溶液需要使用的是___ 。(填仪器序号),还缺少的玻璃仪器是___ 。
②请计算该同学配制此溶液需用托盘天平称量NaClO固体的质量为___ g。
(5)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是___ (填字号)。
Ⅰ.如表为“84”消毒液说明书,请回答下列问题。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1:200水溶液餐饮具,瓜果等1:100水溶液 |
(1)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
Ⅱ.某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(3)此“84消毒液”的物质的量浓度约为
(4)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL该消毒液。
①如图2所示的仪器中配制溶液需要使用的是
②请计算该同学配制此溶液需用托盘天平称量NaClO固体的质量为
(5)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是
| A.定容时俯视制度线 | B.转移前,容量瓶内有蒸馏水 |
| C.未冷至室温就转移定容 | D.定容时水多用胶头滴管吸出 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


