解答题-原理综合题 适中0.65 引用2 组卷234
回答下列问题
(1)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇(CH3OH)。
①该法利用CO2制取甲醇的有关化学反应如下:
CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH1=-178 kJ·mol-1
2CO (g) + O2(g) = 2CO2 (g) ΔH2=-566 kJ·mol-1
2H2 (g) + O2(g) = 2 H2O (g) ΔH3=-483.6 kJ·mol-1
由此计算CO (g) +2H2 (g) = CH3OH(g) ΔH=___________ kJ/mol。
②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
2CH3OH(l) + 3O2(g) = 2CO2(g) +4H2O (l) ΔH1=-a kJ·mol-1
2CH3OH(g) + 3O2(g) = 2CO2(g) + 4H2O (l) ΔH1=-b kJ·mol-1
CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O (l) ΔH1=-c kJ·mol-1
CH3OH(l) +O2(g) = CO(g) + 2 H2O (l) ΔH1=-d kJ·mol-1
由此知,a、b、c、d由小到大排序为___________ 。
③将甲醇完全燃烧生成液态水的反应设计成原电池,以KOH为电解质。工作时负极的电极反应式___________ 。
(2)某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:
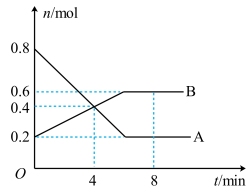
①该反应的化学方程式为___________ 。
②若降低温度,则该反应的正反应速率___________ (填“加快”“减慢”或“不变”,下同),逆反应速率___________ 。
③平衡时A的转化率为___________ 。
④反应达到平衡,此时体系内压强与开始时的压强之比为___________ 。
(1)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇(CH3OH)。
①该法利用CO2制取甲醇的有关化学反应如下:
CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH1=-178 kJ·mol-1
2CO (g) + O2(g) = 2CO2 (g) ΔH2=-566 kJ·mol-1
2H2 (g) + O2(g) = 2 H2O (g) ΔH3=-483.6 kJ·mol-1
由此计算CO (g) +2H2 (g) = CH3OH(g) ΔH=
②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
2CH3OH(l) + 3O2(g) = 2CO2(g) +4H2O (l) ΔH1=-a kJ·mol-1
2CH3OH(g) + 3O2(g) = 2CO2(g) + 4H2O (l) ΔH1=-b kJ·mol-1
CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O (l) ΔH1=-c kJ·mol-1
CH3OH(l) +O2(g) = CO(g) + 2 H2O (l) ΔH1=-d kJ·mol-1
由此知,a、b、c、d由小到大排序为
③将甲醇完全燃烧生成液态水的反应设计成原电池,以KOH为电解质。工作时负极的电极反应式
(2)某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:

①该反应的化学方程式为
②若降低温度,则该反应的正反应速率
③平衡时A的转化率为
④反应达到平衡,此时体系内压强与开始时的压强之比为
20-21高一下·辽宁盘锦·期中
类题推荐
2018年5月9日科技网报道,最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇。
(1)甲醇燃烧时发生如下反应(a、b、c、d均大于0):
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) △H1=-akJ·mol-1
②2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1) △H2=-bkJ·mol-1
③CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(1) △H3=-ckJ·mol-1
④CH3OH(1)+O22(g)=CO (g)+2H2O(1) △H4=-dkJ·mol-1
由此知,a、b、c、d由小到大排序为_______ 。
(2)工业上,通常采用氢气还原CO2法制备甲醇CO2(g)+3H2(g) CH3OH(g)+H2O(1) △H
CH3OH(g)+H2O(1) △H
已知几种化学键的键能数据如下:
根据键能数据估算上述反应中△H=____________ kJ·mol-1。
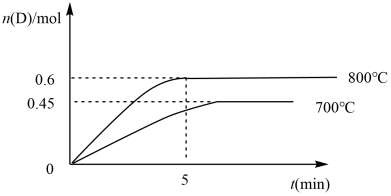
(3)在2L恒容密闭容器中充入2 mol CO2和6.5mlH2,在一定温度下反应,测得混合气体中c(CH3OH)与时间的关系如图1所示。
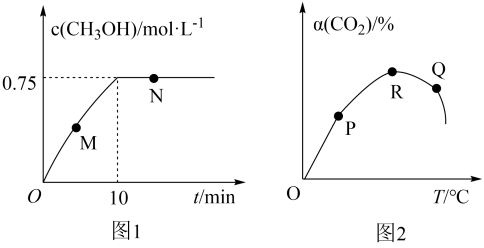
①M点CO2的正反应速率___________ N点CO2的逆反应速率(选填“大于”“小于”或“等于”)。
②0~10min内H2的平均反应速率v(H2)=___________ mol·L-1·min-1。
③在该温度下,该反应平衡常数K为________ 。(结果保留两位小数并要求带单位)
(4)在密闭容器中充入一定量CO2和H2,在含铂催化剂作用下反应,测得单位时间内CO2的转化率与温度关系如图2所示。
①R点对应的CO2转化率最大,其原因是_________________ 。
②在Q点时CO2的转化率突变的原因可能是_________________ 。
(5)以石墨为电极,甲醇/空气碱性(KOH溶液为电解质溶液)燃料电池的能量转化效率高。当KOH恰好完全转化成KHCO3时停止放电,此时负极的电极反应式为_____________ 。
(1)甲醇燃烧时发生如下反应(a、b、c、d均大于0):
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) △H1=-akJ·mol-1
②2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1) △H2=-bkJ·mol-1
③CH3OH(1)+3/2O2(g)=CO2(g)+2H2O(1) △H3=-ckJ·mol-1
④CH3OH(1)+O22(g)=CO (g)+2H2O(1) △H4=-dkJ·mol-1
由此知,a、b、c、d由小到大排序为
(2)工业上,通常采用氢气还原CO2法制备甲醇CO2(g)+3H2(g)
 CH3OH(g)+H2O(1) △H
CH3OH(g)+H2O(1) △H已知几种化学键的键能数据如下:
| 共价键 | C=O | H-H | C-O | C-H | H-O |
| 键能/kJ·mol-1 | 803 | 436 | 326 | 414 | 464 |
根据键能数据估算上述反应中△H=
(3)在2L恒容密闭容器中充入2 mol CO2和6.5mlH2,在一定温度下反应,测得混合气体中c(CH3OH)与时间的关系如图1所示。

①M点CO2的正反应速率
②0~10min内H2的平均反应速率v(H2)=
③在该温度下,该反应平衡常数K为
(4)在密闭容器中充入一定量CO2和H2,在含铂催化剂作用下反应,测得单位时间内CO2的转化率与温度关系如图2所示。
①R点对应的CO2转化率最大,其原因是
②在Q点时CO2的转化率突变的原因可能是
(5)以石墨为电极,甲醇/空气碱性(KOH溶液为电解质溶液)燃料电池的能量转化效率高。当KOH恰好完全转化成KHCO3时停止放电,此时负极的电极反应式为
2018年5月9日科技网报道,《自然纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化为清洁液态燃料—甲醇。
(1)甲醇完全燃烧时发生如下反应(a、b、c均大于0):
2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH1=-akJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1) ΔH2=-bkJ/mol
CH3OH(1)+ O2(g)=CO2(g)+2H2O(1) ΔH3=-ckJ/mol
O2(g)=CO2(g)+2H2O(1) ΔH3=-ckJ/mol
由此知,a、b、c由大到小的排序为_____ 。
(2)工业上可采用氢气还原CO2法制备甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(1) ΔH=-46kJ/mol。
CH3OH(g)+H2O(1) ΔH=-46kJ/mol。
①一定条件下,将1molCO2与3molH2的混合气体在催化剂作用下充分反应生成甲醇气体和液态水,放出的热量____ 46kJ(选填“大于”“小于”或“等于”)。
②对于该可逆反应来说,铂作催化剂能加快反应速率的主要原因是____ 。
A.活化分子能量明显增加
B.降低活化分子的能量
C.增加活化分子百分数
D.增加反应活化能
(3)工业上一般以CO和H2为原料合成甲醇,反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g) ΔH。
CH3OH(g) ΔH。
已知几种化学键的键能数据如表:
已知CO的结构式为C≡O,根据键能数据计算上述反应中ΔH=_____ kJ/mol。
(1)甲醇完全燃烧时发生如下反应(a、b、c均大于0):
2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(1) ΔH1=-akJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1) ΔH2=-bkJ/mol
CH3OH(1)+
由此知,a、b、c由大到小的排序为
(2)工业上可采用氢气还原CO2法制备甲醇:CO2(g)+3H2(g)
①一定条件下,将1molCO2与3molH2的混合气体在催化剂作用下充分反应生成甲醇气体和液态水,放出的热量
②对于该可逆反应来说,铂作催化剂能加快反应速率的主要原因是
A.活化分子能量明显增加
B.降低活化分子的能量
C.增加活化分子百分数
D.增加反应活化能
(3)工业上一般以CO和H2为原料合成甲醇,反应的热化学方程式为:CO(g)+2H2(g)
已知几种化学键的键能数据如表:
| 共价键 | C≡O | H-H | C-O | C-H | H-O |
| 键能/kJ•mol-l | 1072 | 436 | 351 | 413 | 463 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网