解答题-工业流程题 适中0.65 引用1 组卷167
目前我国利用海洋资源获取溴、碘等元素已成规模。
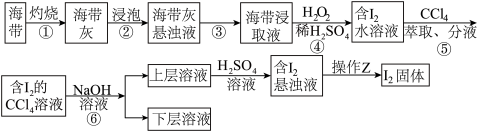
Ⅰ.某研究性学习小组设计以下实验,从海带中提取碘:
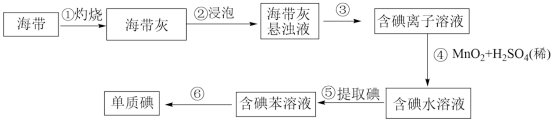
(1)步骤①中高温灼烧海带时,除需要三脚架、泥三角、酒精灯、玻璃棒外,还需要用的实验仪器是__ 。
(2)步骤④反应的离子方程式为__ 。
(3)步骤⑤的名称为__ 。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL苯加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
该实验操作顺序是:_____→_____→_____→A→_____→G→E→F(用上述编号字母填写)__ ;E步骤中操作应注意__ 。
Ⅱ.另一小组设计了如图实验装置,模拟空气吹出法从浓缩的海水中提取溴。
(4)实验步骤如下:
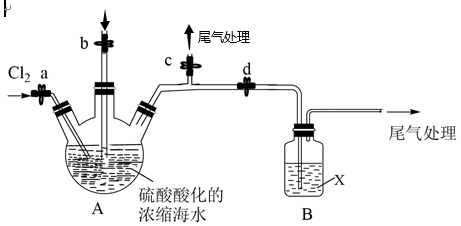
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭活塞a、c,打开活塞__ ,向A中鼓入足量__ ;
③关闭活塞b,打开活塞__ ,再通过A向B中通入足量Cl2;
④取B中所得溶液进行蒸馏,收集液溴。
(5)X试剂可选择__ (填字母),步骤②B中发生反应的离子方程式为__ 。
A.H2O B.饱和食盐水 C.饱和Na2SO3溶液 D.酸性KMnO4溶液
Ⅰ.某研究性学习小组设计以下实验,从海带中提取碘:

(1)步骤①中高温灼烧海带时,除需要三脚架、泥三角、酒精灯、玻璃棒外,还需要用的实验仪器是
(2)步骤④反应的离子方程式为
(3)步骤⑤的名称为
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL苯加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
该实验操作顺序是:_____→_____→_____→A→_____→G→E→F(用上述编号字母填写)
Ⅱ.另一小组设计了如图实验装置,模拟空气吹出法从浓缩的海水中提取溴。
(4)实验步骤如下:

①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭活塞a、c,打开活塞
③关闭活塞b,打开活塞
④取B中所得溶液进行蒸馏,收集液溴。
(5)X试剂可选择
A.H2O B.饱和食盐水 C.饱和Na2SO3溶液 D.酸性KMnO4溶液
21-22高二上·山东威海·期中
类题推荐
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
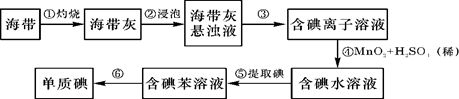
(1)从上述步骤中可知,海带中含有的碘元素的主要存在形式是_________ (填化学式)。
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是________ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A烧杯 B表面皿 C坩埚 D酒精灯 E干燥器
(3)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指列实验装置中的错误之处。
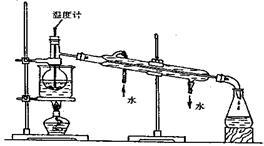
①_________________ ;② ________________ ;③ ________________ ;
进行上述蒸馏操作时,使用水浴的原因是_________________ ;最后晶态碘在_____________ 里聚集。
(4)步骤④反应的离子方程式是______________________ 。若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I—,写出反应的离子方程式____________________ 。
(5)检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是___________ 。
(6)步骤⑤中,某学生选择用苯来提取碘,其实验操作可分解为如下几步:
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空:
正确操作步骤的顺序是________ →__________ →___________ →A→G→_________ →E→F

(1)从上述步骤中可知,海带中含有的碘元素的主要存在形式是
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是
A烧杯 B表面皿 C坩埚 D酒精灯 E干燥器
(3)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指列实验装置中的错误之处。

①
进行上述蒸馏操作时,使用水浴的原因是
(4)步骤④反应的离子方程式是
(5)检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是
(6)步骤⑤中,某学生选择用苯来提取碘,其实验操作可分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空:
正确操作步骤的顺序是
分海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋植物中提取碘的流程如下:

某化学兴趣小组将上述流程②③设计成如图所示:


已知氯水中含有Cl2,②中发生反应的化学方程式为Cl2+2KI=2KCl+I2。
回答下列问题:
(1)写出提取过程①③中实验操作的名称:①________________ ,③________________ 。
(2)F中的现象是________________________ 。
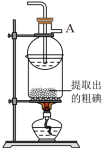
(3)从碘的四氯化碳溶液中得到单质碘还需进行的操作是________ 。实验装置如右图所示,该实验采用的加热方式为_____________ ,仪器A的名称为__________________ 。
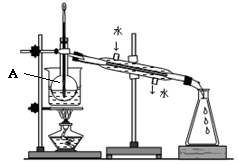
(4)在灼烧过程中,将使用到的(除泥三角外)实验仪器有____________ 。
A试管 B瓷坩埚 C坩埚钳 D蒸发皿 E酒精灯
(5)现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
完成下列填空:
①正确操作步骤的顺序是:(用上述各操作的编号字母填写)
________ →________ →________ →A→_________ →G→E→F
②上述G步骤操作的目的是___________________________ 。

某化学兴趣小组将上述流程②③设计成如图所示:


已知氯水中含有Cl2,②中发生反应的化学方程式为Cl2+2KI=2KCl+I2。
回答下列问题:
(1)写出提取过程①③中实验操作的名称:①
(2)F中的现象是
(3)从碘的四氯化碳溶液中得到单质碘还需进行的操作是

(4)在灼烧过程中,将使用到的(除泥三角外)实验仪器有
A试管 B瓷坩埚 C坩埚钳 D蒸发皿 E酒精灯
(5)现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50mL碘水和15mL CCl4加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置,分层。
完成下列填空:
①正确操作步骤的顺序是:(用上述各操作的编号字母填写)
②上述G步骤操作的目的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网