解答题-原理综合题 适中0.65 引用2 组卷181
丙烯是化工合成的重要原料,其制备工艺主要有如下两种:
工艺1:丙烷无氧脱氢工艺:
工艺2:丙烷氧化脱氢工艺:

回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的
______  ,与工艺1相比,工艺2的优点是
,与工艺1相比,工艺2的优点是___________ (从能源角度)。
(2)若提高工艺1丙烷的平衡转化率,下列措施不可行的是___________(填字母)。
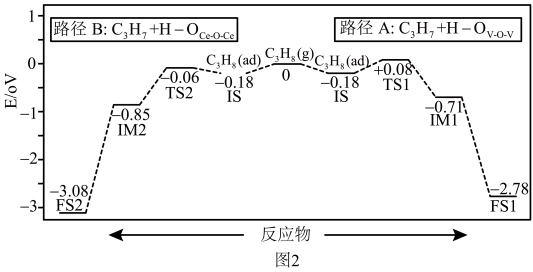
(3)工艺1脱氢时以CeO2/VO3为催化剂,脱第1个氢原子的反应历程有两种情况(Ts表示过渡态):
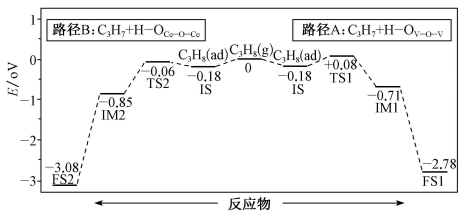
用图中数据可知,脱第1个氢原子时,最有可能按路径____ (填A或B),其原因是______ 。
(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:_______ ,若恒容反应容器中C3H8(g)的浓度为 ,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=
,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=_____ [结果保留两位有效数字,丙烯的选择性 ]。
]。
工艺1:丙烷无氧脱氢工艺:
工艺2:丙烷氧化脱氢工艺:
回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的
| 物质 | C3H8(g) | C3H6(g) | H2(g) |
| 燃烧热( | 2217.8 | 2058.0 | 285.8 |
(2)若提高工艺1丙烷的平衡转化率,下列措施不可行的是___________(填字母)。
| A.适当的升高温度 |
| B.增大压强 |
| C.提高恒容反应容器中丙烷的初始浓度 |
| D.向恒压反应容器中的丙烷掺入水蒸气(水蒸气不参与反应) |

用图中数据可知,脱第1个氢原子时,最有可能按路径
(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:
21-22高三上·湖北·阶段练习
类题推荐
丙烯是重要的化工原料,工业上主要通过高纯丙烷直接脱氢及CO2辅助脱氢两种方法制备(产物中还含有CH、C2H4等气体)。以丙烷为原料直接脱氢制丙烯的主要反应为:C3H8(g)⇌C3H6(g)+H2(g) △H1=+124kJ/mol ①
(1)该反应在工业生产中适宜选择的条件是___________;
(2)引入CO2辅助脱氢后还将发生:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2 ②,若想通过盖斯定律计算反应②的反应热△H2,除了需知道水煤气反应(即:C(s)+H2O(g)⇌CO(g)+H2(g)的ΔH外,还至少需知道___________ 的反应热(用化学方程式回答);
(3)科研人员就丙烷直接脱氢和CO2辅助脱氢做了一系列研究得出如下数据。容器:恒压密闭容器。催化剂:GaN。
数据表明:随温度的升高,无论是丙烷直接脱氢制丙烯,还是CO2辅助脱氢制丙烯,丙烯的选择性都随温度的升高而下降,除了因温度升高积碳造成催化剂表面失活外,还可能是由于___________ ;从表中数据还可发现:相同温度,CO2辅助脱氢制丙烯能有效提高丙烷的转化率,其原因可能是___________ (答出两点原因)。
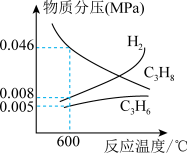
(4)在600℃、恒压条件下,测得丙烷直接脱氢制丙烯反应中主要物质对应的平衡分压如图所示,请根据图中所给数据计算反应C3H8(g)⇌C3H6(g)+H2(g)在该温度下的Kp=___________ MPa(结果保留2位有效数字)。
(1)该反应在工业生产中适宜选择的条件是___________;
| A.较高的温度、较高的压强 | B.较高的温度、较低的压强 |
| C.较低的温度、较低的压强 | D.合适的催化剂 |
(3)科研人员就丙烷直接脱氢和CO2辅助脱氢做了一系列研究得出如下数据。容器:恒压密闭容器。催化剂:GaN。
| 温度 | 550 | 600 | 650 | 700 | |
| 丙烯选择性 | 无CO2参与 | 86.5 | 69.1 | 40.0 | 31.1 |
| 有CO2参与 | 95 | 87.3 | 45.7 | 36.4 | |
| 丙烷转化率 | 无CO2参与 | 8.3 | 8.2 | 12.1 | 27.3 |
| 有CO2参与 | 10.2 | 9.0 | 15.5 | 32.8 | |
数据表明:随温度的升高,无论是丙烷直接脱氢制丙烯,还是CO2辅助脱氢制丙烯,丙烯的选择性都随温度的升高而下降,除了因温度升高积碳造成催化剂表面失活外,还可能是由于
(4)在600℃、恒压条件下,测得丙烷直接脱氢制丙烯反应中主要物质对应的平衡分压如图所示,请根据图中所给数据计算反应C3H8(g)⇌C3H6(g)+H2(g)在该温度下的Kp=

丙烯是制造一次性医用口罩的重要原料。丙烷催化脱氢是工业生产丙烯的重要途径,丙烷催脱氢技术主要分为氧化脱氢和直接脱氢两种。回答下列问题:
(1)丙烷催化氧化脱氢法主要反应如下:
2C3H8(g)+O2(g) 2C3H6(g)+2H2O(g) △H1=-236kJ·mol-1(i)
2C3H6(g)+2H2O(g) △H1=-236kJ·mol-1(i)
反应过程中消耗的C3H8和 生成的C3H6的物质的量随温度的变化关系见下表。
①反应i中反应物的总能量_______ 生成物的总能量(填“大于”“小于”或“等于”)。
②分析表中数据得到丙烯的选择性随温度的升高而______ (填写“不变”“升高”“降 低”); 出现此结果的原因除生成乙烯等副产物外还可能是 _________ 。(C3H6的选择性= ×100%)
×100%)
(2)丙烷催化直接脱氢反应: C3H8(g) ⇌C3H6(g)+ H2(g) △H2=+124. 3kJ•mol -1 ( ii ) 副反应:C3H8 (g) ⇌C2H4 (g) + CH4(g) △H3(iii)
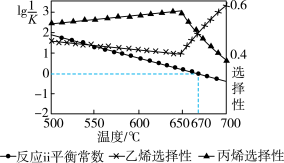
①反应 ii 的平衡常数、产物丙烯选择性、副产物乙烯选择性与温度关系如图所示, 分析工业生产中采用的温度为 650°C 左右的原因是_________ 。
②温度为 670°C 时,若在 1L 的容器中投入 8 molC3H8,充分反应后,平衡混合气体中有 2molCH4和一定量C3H8、C3H6、H2、C2H4,计算该条件下C3H6的选择性为___ %。
③欲使丙烯的产率提高,下列措施可行的是______ ( 填写序号 )
a.恒压条件下向原料气中掺杂水蒸气 b.增大氢气与丙烷的投料比 c.选择对脱氢反应更好选择性的催化剂 d.大压强
(3)科学家探索出利用无机膜催化丙烷脱氢制丙烯的新工艺,该工艺利用特定功能膜将生成的氢气从反应区一侧有选择性的及时移走,从平衡角度分析该工艺的优点______ 。
(1)丙烷催化氧化脱氢法主要反应如下:
2C3H8(g)+O2(g)
反应过程中消耗的C3H8和 生成的C3H6的物质的量随温度的变化关系见下表。
| 反应温度/℃ n(消耗)或n(生成)/mol | 535 | 550 | 575 |
| C3H8 | 6 | 13 | 33 |
| C3H6 | 4 | 8 | 17 |
①反应i中反应物的总能量
②分析表中数据得到丙烯的选择性随温度的升高而
(2)丙烷催化直接脱氢反应: C3H8(g) ⇌C3H6(g)+ H2(g) △H2=+124. 3kJ•mol -1 ( ii ) 副反应:C3H8 (g) ⇌C2H4 (g) + CH4(g) △H3(iii)

①反应 ii 的平衡常数、产物丙烯选择性、副产物乙烯选择性与温度关系如图所示, 分析工业生产中采用的温度为 650°C 左右的原因是
②温度为 670°C 时,若在 1L 的容器中投入 8 molC3H8,充分反应后,平衡混合气体中有 2molCH4和一定量C3H8、C3H6、H2、C2H4,计算该条件下C3H6的选择性为
③欲使丙烯的产率提高,下列措施可行的是
a.恒压条件下向原料气中掺杂水蒸气 b.增大氢气与丙烷的投料比 c.选择对脱氢反应更好选择性的催化剂 d.大压强
(3)科学家探索出利用无机膜催化丙烷脱氢制丙烯的新工艺,该工艺利用特定功能膜将生成的氢气从反应区一侧有选择性的及时移走,从平衡角度分析该工艺的优点
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网