解答题-结构与性质 较易0.85 引用5 组卷289
由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
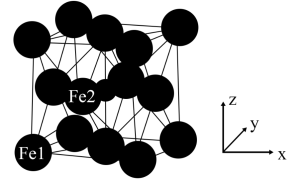
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(

21-22高三上·河北石家庄·阶段练习
类题推荐
铁在史前就为人们所知,铁及其化合物推动了人类文明的发展。回答下列问题:
(1)Fe元素位于元素周期表的_______ 区,基态Fe2+的核外电子排布式为_______ 。
(2)复盐NH4Fe(SO4)2·12H2O俗称铁铵矾,可用于鞣革。铁铵矾中,所含N、O、S三种非金属元素第一电离能由小到大的顺序是_______ ,H2O的VSEPR模型为_______ 。 的键角比NH3的键角
的键角比NH3的键角_______ (填“大”或“小”)。
(3)三价铁的强酸盐溶于水后经水解可以生成如图所示的二聚体,其中Fe3+的配位数为_______ , 过渡元素的s、p、d轨道可以参与杂化,含s、p、d轨道的杂化类型有:①dsp2、 ②sp3d、③sp3d2,该二聚体中Fe采取的杂化类型为_______ (填标号)。

(4)三种化合物的熔点如下表所示:
试解释其熔点差异的原因:_______ 。
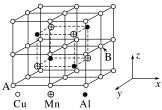
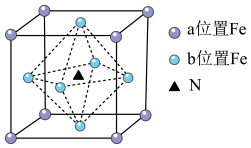
(5)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某立方FexNy的晶胞如图所示,晶胞参数为apm,该晶体密度为_______ g·cm-3 (设NA为阿伏加德罗常数的值,写出表达式),Cu完全替代该晶体中b位置Fe,形成Cu替代型产物Fe(x-n)CunNy, n:y=_______ 。

(1)Fe元素位于元素周期表的
(2)复盐NH4Fe(SO4)2·12H2O俗称铁铵矾,可用于鞣革。铁铵矾中,所含N、O、S三种非金属元素第一电离能由小到大的顺序是
(3)三价铁的强酸盐溶于水后经水解可以生成如图所示的二聚体,其中Fe3+的配位数为

(4)三种化合物的熔点如下表所示:
| 化合物 | FeCl3 | NaCl | MgO |
| 熔点/℃ | 308 | 801 | 2852 |
(5)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某立方FexNy的晶胞如图所示,晶胞参数为apm,该晶体密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网