解答题-实验探究题 适中0.65 引用1 组卷258
铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
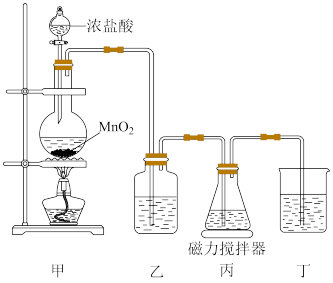
I.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:
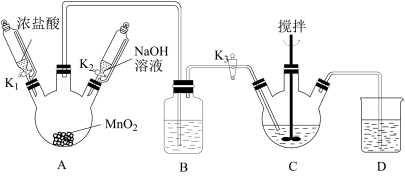
(1)C中盛放Bi(OH)3与NaOH的混合物,与Cl2反应生成NaBiO3,反应的化学方程式为_______ ,B装置的作用是_______ 。
(2)当观察到_______ (填现象)时,可以初步判断C中反应已经完成。
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭_______ ;打开_______ 。
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有_______ 、过滤、洗涤、干燥。
II.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为_______ 。
III.产品纯度的测定
(6)取上述NaBiO3产品a g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmol·L-l的H2C2O4标准溶液滴定生成的MnO (已知:H2C2O4+MnO
(已知:H2C2O4+MnO —CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗c mL标准溶液。该产品的纯度为
—CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗c mL标准溶液。该产品的纯度为_______ %(用含a、b、c的代数式表示)。
I.制取铋酸钠。制取装置如图(加热和夹持仪器已略去),部分物质性质如下:

| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水;浅黄色 | 难溶于水;白色 |
(2)当观察到
(3)拆除装置前必须先除去残留的Cl2,以免污染空气。除去烧瓶A中残留Cl2的操作是:关闭
(4)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有
II.铋酸钠的应用——检验Mn2+
(5)往待检液中加入铋酸钠晶体,加硫酸酸化,生成Bi3+,且溶液变为紫红色,证明待检液中存在Mn2+。产生紫红色现象的离子方程式为
III.产品纯度的测定
(6)取上述NaBiO3产品a g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用bmol·L-l的H2C2O4标准溶液滴定生成的MnO
21-22高三上·山东·阶段练习
类题推荐
铋酸钠(NaBiO3)是分析化学中的重要试剂。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
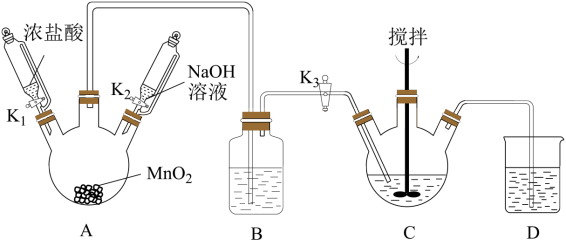
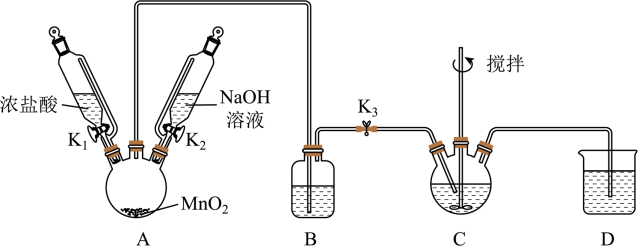
Ⅰ、制取铋酸钠:制取装置如图(加热和夹持仪器已略去)。
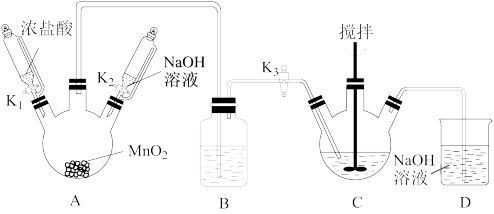
部分物质性质如下:
(1)反应开始时,打开K1和K3,写出A中反应的化学方程式_______ 。B装置的作用是_______ 。
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为_______ 。反应过程中观察到C中的主要现象是_______ 。
(3)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是_______ ,过滤、洗涤、干燥。
(4)拆除装置前须先除去A中残留的Cl2以免污染空气,除去Cl2的操作是关闭_______ ,打开_______ 。
Ⅱ、铋酸钠的应用——检验Mn2+
(5)向待测液中加入铋酸钠晶体,加入硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+(铋酸钠转变为Bi3+),产生紫红色现象的离子方程式为_______ 。
Ⅰ、制取铋酸钠:制取装置如图(加热和夹持仪器已略去)。

部分物质性质如下:
| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为
(3)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是
(4)拆除装置前须先除去A中残留的Cl2以免污染空气,除去Cl2的操作是关闭
Ⅱ、铋酸钠的应用——检验Mn2+
(5)向待测液中加入铋酸钠晶体,加入硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+(铋酸钠转变为Bi3+),产生紫红色现象的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网