解答题-实验探究题 适中0.65 引用1 组卷269
纯碱是重要的生活用碱和化工原料,用途广泛。请同学们按要求回答问题。
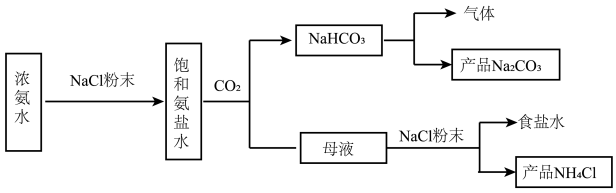
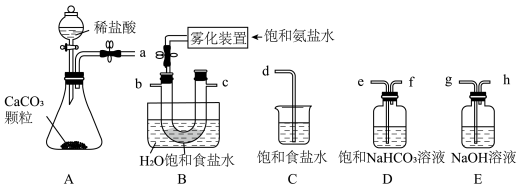
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。
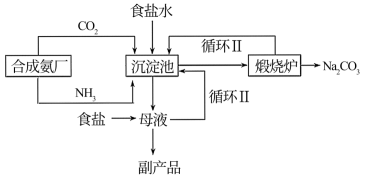
(1)请写出煅烧炉中发生反应的化学方程式:___________ 。
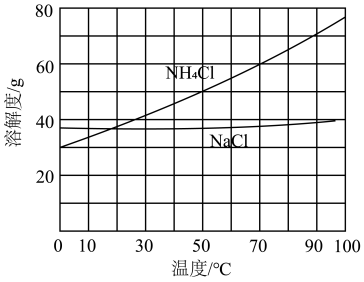
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为___________ ,循环Ⅰ中物质的主要成分是___________ 。(本小题涉及到的物质均写化学式)
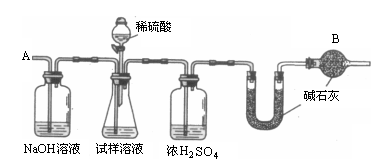
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。
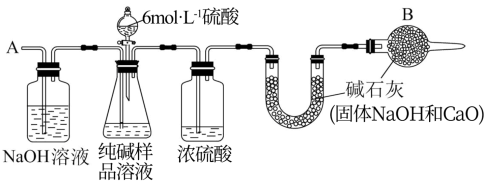
主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是___________ 。
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将___________ (填“偏高”、“偏低”或“不变”)。
(5)步骤⑤的目的是___________ 。
(6)步骤⑦的目的是___________ 。
(7)该样品中纯碱的质量分数的计算式为___________ 。
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是___________ 。
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。

(1)请写出煅烧炉中发生反应的化学方程式:
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。

主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将
(5)步骤⑤的目的是
(6)步骤⑦的目的是
(7)该样品中纯碱的质量分数的计算式为
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
21-22高一上·黑龙江大庆·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网