单选题 适中0.65 引用3 组卷288
氮气是一种重要的化工原料,工业上常用氮气合成氨、制硝酸。合成氨、制取硝酸的转化过程如图所示。下列说法正确的是
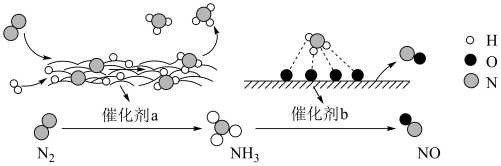

| A.催化剂a与催化剂b表面均有极性键形成 |
| B.催化剂a可加快合成氨的反应速率并提高平衡转化率 |
| C.图示中氮元素在转化过程中均被氧化 |
| D.不使用催化剂,上述转化不能发生 |
20-21高一上·甘肃兰州·期中
类题推荐
哈伯法合成氨的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。将上述合成氨反应设计成燃料电池,工作原理如图所示。其中溶有
,新研制的催化剂可使该反应在常温、常压下进行,以氮气和氢气为反应物的燃料电池是利用氮气的一种新方法。将上述合成氨反应设计成燃料电池,工作原理如图所示。其中溶有 的稀的A溶液为电解质。下列说法不正确的是
的稀的A溶液为电解质。下列说法不正确的是


| A.b电极为负极 |
| B.a电极发生的反应为 |
| C.A溶液中所含溶质为 |
| D.可用蒸发结晶的方法分离出A |
细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示,下列说法错误的是
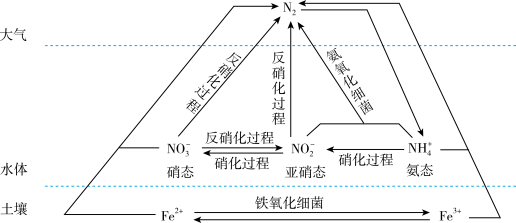
| A.上图所示氮循环中,N2转化为氨态氮属于氮的固定 |
| B.氨气是生产氮肥的主要原料,工业上用氮气和氢气合成氨 |
| C.反硝化过程中,含氮物质发生氧化反应 |
| D.硝化过程中,含氮物质发生氧化反应 |
工业上用氢气和氮气直接合成氨: ,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是
,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是
| A.使用催化剂是为了加快反应速率 |
| B. |
| C.为了提高 |
| D.达到平衡时, |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


