解答题-原理综合题 适中0.65 引用1 组卷135
氢气是重要的化工原料,研究氢气的高效利用具有深远的意义。回答下列问题。
Ⅰ.合成氨工业中,H2与N2在铁触媒的作用下反应历程为:
①化学吸附:N2(g)→2N*(*表示吸附态,下同)、H2(g) 2H*;
2H*;
②表面吸附:N*+H* NH*、NH*+H*
NH*、NH*+H* NH2*、NH2*+H*
NH2*、NH2*+H* NH3*。
NH3*。
③脱附:NH3* NH3(g)。其中脱附决定合成氨的整体反应速率。
NH3(g)。其中脱附决定合成氨的整体反应速率。
(1)根据题意,铁触媒在合成氨中的作用为___________ 。
(2)实际生产中,原料气中H2和N2的物质的量之比为2.8∶1,N2适度过量的理由除了原料易得、可提高H2的转化率外,还有___________ 。
(3)已知:Ka1(H2SO3)>Kb(NH3·H2O)>Ka2(H2SO3)。工业上用氨水处理硫酸厂尾气中的SO2,恰好生成(NH4)2SO3时,溶液显___________ 性(填“酸”“中”或“碱”,下同);继续吸收SO2恰好生成NH4HSO3时,溶液显___________ 性。
Ⅱ.在一定条件下,H2可以用于治理氮氧化物污染。
(4)有关键能如下表,则2H2(g)+2NO(g) N2(g)+2H2O(g)该反应正反应与逆反应活化能之差为
N2(g)+2H2O(g)该反应正反应与逆反应活化能之差为___________
(5)向两个容积为2 L的刚性容器中均充入2 mol H2和2 mol NO,分别在220℃和300℃发生反应:2H2(g)+2NO(g) N2(g)+2H2O(g)。测得两容器中H2与H2O的物质的量随时间的变化关系如图所示,曲线Ⅰ平衡后气体的总压强为p1kPa,曲线Ⅱ平衡后气体的总压强为p2kPa。
N2(g)+2H2O(g)。测得两容器中H2与H2O的物质的量随时间的变化关系如图所示,曲线Ⅰ平衡后气体的总压强为p1kPa,曲线Ⅱ平衡后气体的总压强为p2kPa。
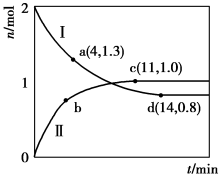
①220℃条件下的变化曲线为___________ (填“Ⅰ”或“Ⅱ”);ad段N2的平均反应速率为___________ mol/(L·min)。
②a、c、d三点的逆反应速率由大到小的顺序为___________ (用a、c、d表示);曲线Ⅱ代表的温度下,该反应的Kp=___________ (Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
Ⅰ.合成氨工业中,H2与N2在铁触媒的作用下反应历程为:
①化学吸附:N2(g)→2N*(*表示吸附态,下同)、H2(g)
②表面吸附:N*+H*
③脱附:NH3*
(1)根据题意,铁触媒在合成氨中的作用为
(2)实际生产中,原料气中H2和N2的物质的量之比为2.8∶1,N2适度过量的理由除了原料易得、可提高H2的转化率外,还有
(3)已知:Ka1(H2SO3)>Kb(NH3·H2O)>Ka2(H2SO3)。工业上用氨水处理硫酸厂尾气中的SO2,恰好生成(NH4)2SO3时,溶液显
Ⅱ.在一定条件下,H2可以用于治理氮氧化物污染。
(4)有关键能如下表,则2H2(g)+2NO(g)
| 化学键 | H—H | NO | N2 | H—O |
| 键能/(kJ·mol−1) | 436 | 632 | 946 | 464 |
(5)向两个容积为2 L的刚性容器中均充入2 mol H2和2 mol NO,分别在220℃和300℃发生反应:2H2(g)+2NO(g)

①220℃条件下的变化曲线为
②a、c、d三点的逆反应速率由大到小的顺序为
2021·全国·模拟预测
类题推荐
I.研究氮和碳的化合物对工业生产和防治污染有重要意义,回答下列问题:
(1)化学键键能数据如下:
合成氨反应 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的活化能Ea1=254 kJ·mol-1,由此计算氨分解反应NH3(g)
NH3(g)的活化能Ea1=254 kJ·mol-1,由此计算氨分解反应NH3(g) 
 N2(g)+
N2(g)+ H2(g)的活化能Ea2=
H2(g)的活化能Ea2=___________ kJ·mol-1。
(2)利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H<0。某研究小组将2 mol NH3、3 mol NO和一定量的O2充入2 L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:
5N2(g)+6H2O(g) △H<0。某研究小组将2 mol NH3、3 mol NO和一定量的O2充入2 L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:
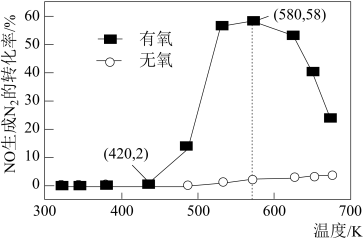
①温度从420K升高到580K用时4min,则此时段内NO的平均反应速率v(NO)=___________ ;
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是___________ 。
II.目前有一种新的循环利用方案处理航天员呼吸产生的CO2,是用Bosch反应CO2(g)+2H2(g) C(s)+2H2O(g) △H<0,再电解水实现O2的循环利用。
C(s)+2H2O(g) △H<0,再电解水实现O2的循环利用。
(3)若要此反应自发进行___________ (填“高温”或“低温”)更有利。
(4)350℃时,向体积为2 L的恒容密闭容器中通入8 mol H2和4 mol CO2发生以上反应,若反应起始和平衡时温度相同(均为350℃),测得反应过程中压强随时间的变化如表所示:
①350℃时Bosch反应的Kp=___________ (Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)。
②Bosch反应的速率方程:v正=k正·c(CO2)·c2(H2),v逆=k逆·c2(H2O)(k是速率常数,只与温度有关)。20min时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下(NH4)2SO3溶液的酸碱性并说明判断依据:___________ 。(已知:NH3·H2O的K=1.8×10-5;H2SO3的Ka1=1.3×10-2,Ka2=6.3×10-8)
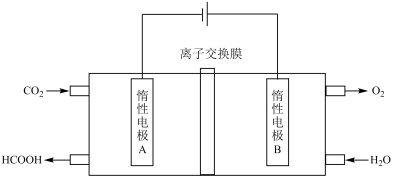
(6)通过电化学方法可有效实现以CO2和水为原料合成甲酸,其原理示意图图所示,则A极的电极反应式为___________ 。
(1)化学键键能数据如下:
| 化学键 | H-H | N≡N | N-H |
| E/(kJ/mol) | 436 | 946 | 391 |
(2)利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g)

①温度从420K升高到580K用时4min,则此时段内NO的平均反应速率v(NO)=
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是
II.目前有一种新的循环利用方案处理航天员呼吸产生的CO2,是用Bosch反应CO2(g)+2H2(g)
(3)若要此反应自发进行
(4)350℃时,向体积为2 L的恒容密闭容器中通入8 mol H2和4 mol CO2发生以上反应,若反应起始和平衡时温度相同(均为350℃),测得反应过程中压强随时间的变化如表所示:
| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强 | 6.00P0 | 5.60 P0 | 5.30 P0 | 5.15 P0 | 5.06 P0 | 5.00 P0 | 5.00 P0 |
②Bosch反应的速率方程:v正=k正·c(CO2)·c2(H2),v逆=k逆·c2(H2O)(k是速率常数,只与温度有关)。20min时,
(5)工业上常用氨水吸收二氧化硫,通过计算判断常温下(NH4)2SO3溶液的酸碱性并说明判断依据:
(6)通过电化学方法可有效实现以CO2和水为原料合成甲酸,其原理示意图图所示,则A极的电极反应式为

氮及其化合物的研究对于生态环境保护和工农业生产发展非常重要。
(1)已知:2NH3(g) N2(g)+3H2(g),活化能Ea1=600 kJ/mol,合成氨有关化学键的键能如下表:
N2(g)+3H2(g),活化能Ea1=600 kJ/mol,合成氨有关化学键的键能如下表:
则合成氨反应:N2(g)+3H2(g) 2NH3(g)的活化能Ea2=
2NH3(g)的活化能Ea2=___________ 。
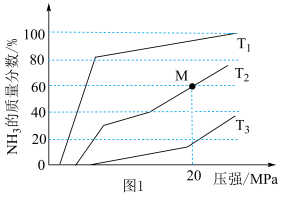
(2)在一定条件下,向某反应容器中投入1 mol N2、3mol H2在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。___________ , M点N2的转化率为___________ 。
(3)采用催化剂存在下臭氧氧化—碱吸收法同时脱除SO2和NO。
反应I:NO(g)+O3(g) NO2(g)+O2(g)
NO2(g)+O2(g)  = -200.9 kJ/mol
= -200.9 kJ/mol
反应II:SO2(g)+O3(g) SO3(g)+O2(g)
SO3(g)+O2(g)  =-241.6 kJ/mol
=-241.6 kJ/mol
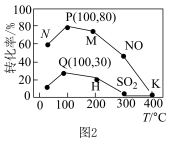
一定条件下,向容积为2 L的反应器充如2.0 mol NO、2.0molSO2的模拟烟气和4.0molO3,升高温度,体系中NO和SO2的转化率随温度T变化如图2所示。___________ 。
A.温度越高,脱除SO2和NO的效果越好
B.相同温度下, NO的转化率远高于SO2
C.可根据不同温度下的转化率选择最佳温度脱除SO2和NO
(4)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g) N2(g)+2CO2(g)
N2(g)+2CO2(g)  H=-746.8 kJ/mol。
H=-746.8 kJ/mol。
实验测得:v正=k正p2(NO)·p2(CO),v逆=k逆p(N2)。p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k正增大的倍数___________ (选填“大于”“小于”或“等于”) k逆增大的倍数。
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0 kPa.达平衡时压强为0.9p0 kPa,则 =
=___________ 。
(5)氮的氧化物脱除可用电化学原理处理,如图3装置可同时吸收SO2和NO。直流电源的正极为__________ (选填“a”或“b”),阳极的电极反应式___________ 。该电解装置选择___________ (选填“阳”或“阴")离子交换膜。
(1)已知:2NH3(g)
| 化学键 | H-H | N≡N | N-H |
| 键能/kJ/mol | 436 | 946 | 391 |
(2)在一定条件下,向某反应容器中投入1 mol N2、3mol H2在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。
(3)采用催化剂存在下臭氧氧化—碱吸收法同时脱除SO2和NO。
反应I:NO(g)+O3(g)
反应II:SO2(g)+O3(g)
一定条件下,向容积为2 L的反应器充如2.0 mol NO、2.0molSO2的模拟烟气和4.0molO3,升高温度,体系中NO和SO2的转化率随温度T变化如图2所示。
A.温度越高,脱除SO2和NO的效果越好
B.相同温度下, NO的转化率远高于SO2
C.可根据不同温度下的转化率选择最佳温度脱除SO2和NO
(4)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)
实验测得:v正=k正p2(NO)·p2(CO),v逆=k逆p(N2)。p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k正增大的倍数
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0 kPa.达平衡时压强为0.9p0 kPa,则
(5)氮的氧化物脱除可用电化学原理处理,如图3装置可同时吸收SO2和NO。直流电源的正极为

研究氮及其化合物参与的反应,对于提高含氮物质的平衡转化率和产品产率都具有重要的意义。回答下列问题:
(1)已知:Ka1(H2SO3)>Kb(NH3·H2O)>Ka2(H2SO3)。工业上用氨水吸收硫酸厂尾气中的SO2,恰好生成(NH4)2SO3时,溶液显_______ 性(填酸、中或碱);继续吸收SO2恰好生成NH4HSO3时,溶液显________ 性(填酸、中或碱)。
(2)在α-Fe(III)铁原子簇表面,以N2和H2为原料合成氨的反应机理如下:
①H2(g)=2H(g) ∆H1②N2(g)+2H(g)⇌2(NH)(g) ∆H2
③(NH)(g)+H(g)⇌(NH2)(g) ∆H3④(NH2)(g)+H(g)⇌NH3(g) ∆H4
总反应:N2(g)+3H2(g)⇌2NH3(g) ∆H。则∆H4=_______ (用含∆H1、∆H2、∆H3、∆H的式子表示)。
(3)660K在恒容容器中,2NO(g)+O2(g)⇌2NO2(g)的速率方程为:v=k·cm(NO)·cn(O2),k是该反应在660K时的速率常数。NO和O2的初始浓度为c(NO)和c(O2),反应的初始速率v如下表所示。
①m=______ ,k=_____ (只写数值,不写单位)。
②第1组达平衡时,n(NO)+n(O2)=n(NO2),平衡常数K=_____ (保留一位小数)。
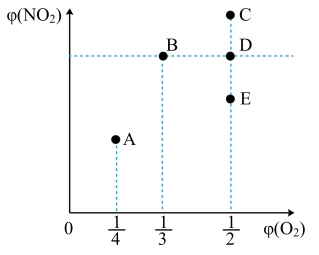
③一定温度下,向恒容容器中充入NO和O2,O2初始的体积分数[ (O2)]与平衡时NO2的体积分数[
(O2)]与平衡时NO2的体积分数[ (NO2)]关系如上图所示。
(NO2)]关系如上图所示。 (O2)=
(O2)= 时,
时, (NO2)可能为
(NO2)可能为_______ 点(填C、D或E)。
(1)已知:Ka1(H2SO3)>Kb(NH3·H2O)>Ka2(H2SO3)。工业上用氨水吸收硫酸厂尾气中的SO2,恰好生成(NH4)2SO3时,溶液显
(2)在α-Fe(III)铁原子簇表面,以N2和H2为原料合成氨的反应机理如下:
①H2(g)=2H(g) ∆H1②N2(g)+2H(g)⇌2(NH)(g) ∆H2
③(NH)(g)+H(g)⇌(NH2)(g) ∆H3④(NH2)(g)+H(g)⇌NH3(g) ∆H4
总反应:N2(g)+3H2(g)⇌2NH3(g) ∆H。则∆H4=
(3)660K在恒容容器中,2NO(g)+O2(g)⇌2NO2(g)的速率方程为:v=k·cm(NO)·cn(O2),k是该反应在660K时的速率常数。NO和O2的初始浓度为c(NO)和c(O2),反应的初始速率v如下表所示。
| 编号 | c(NO)/mol·L-1 | c(O2)/ mol·L-1 | v/ mol·L-1·s-1 |
| Ⅰ | 0.10 | 0.10 | 0.3 |
| Ⅱ | 0.10 | 0.20 | 0.6 |
| Ⅲ | 0.20 | 0.20 | 2.40 |
②第1组达平衡时,n(NO)+n(O2)=n(NO2),平衡常数K=
③一定温度下,向恒容容器中充入NO和O2,O2初始的体积分数[

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


