解答题-原理综合题 适中0.65 引用1 组卷115
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
(1)已知:

则表示1mol气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(2)CO和H2为原料合成甲醇,下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
(3) 时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入
时,CO和H2为原料合成甲醇,在体积为2L的密闭容器中加入 和
和 。CO(g)的物质的量随时间的变化如表:
。CO(g)的物质的量随时间的变化如表:
根据表中数据回答:
①氢气平衡转化率为___________ 。
② 时,该反应的平衡常数为
时,该反应的平衡常数为___________ 。
③保持其它条件不变,向平衡体系中充入1molCO(g)、 、
、 。此时
。此时
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
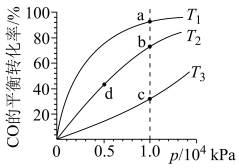
(4)CO和H2为原料合成甲醇,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,下列说法正确的是___________
(1)已知:
则表示1mol气态甲醇完全燃烧生成
(2)CO和H2为原料合成甲醇,下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
| A.随时将CH3OH与反应混合物分离 | B.降低反应温度 |
| C.增大体系压强 | D.便用高效催化剂 |
| 时间/s | 0 | 2 | 5 | 10 | 20 | 40 | 80 |
| 物质的量(mol) | 1.00 | 0.50 | 0.375 | 0.25 | 0.20 | 0.20 | 0.20 |
根据表中数据回答:
①氢气平衡转化率为
②
③保持其它条件不变,向平衡体系中充入1molCO(g)、
(4)CO和H2为原料合成甲醇,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,下列说法正确的是___________

| A.温度:T1>T2>T3 |
| B.正反应速率:v(a)>v(c)、v(b)>v(d) |
| C.反应速率:v正(d)<v逆(c) |
| D.平均摩尔质量:M(a)>M(c)、M(b)<M(d) |
21-22高二上·黑龙江双鸭山·期中
类题推荐
“Cl化学”是指以碳单质或分子中含1个碳原子的物质(如CO、 、
、 、
、 等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。工业上一般以CO和
等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。工业上一般以CO和 为原料合成甲醇,该反成的热化学方程式为:
为原料合成甲醇,该反成的热化学方程式为:
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
(2)已知:

则表示1mol气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(3) 时,在体积为2L的密闭容器中加入
时,在体积为2L的密闭容器中加入 和
和 。CO(g)的物质的量随时间的变化如表:
。CO(g)的物质的量随时间的变化如表:
根据表中数据回答:
①氢气平衡转化率为___________ 。
② 时,该反应的平衡常数为
时,该反应的平衡常数为___________ 。
③保持其它条件不变,向平衡体系中充入1mol CO(g)、 、
、 。此时
。此时
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
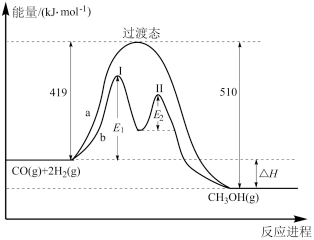
(4)反应 ,其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是___________。(填字母)。
,其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是___________。(填字母)。
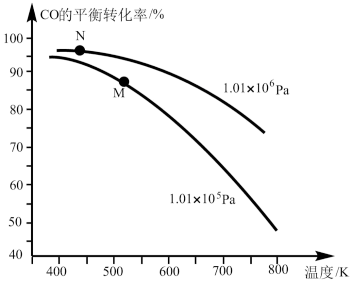
(5)工业实际合成 中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由
中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由___________ 。
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________(填字母)。
| A.随时将 | B.降低反应温度 |
| C.增大体系压强 | D.便用高效催化剂 |
则表示1mol气态甲醇完全燃烧生成
(3)
| 时间/s | 0 | 2 | 5 | 10 | 20 | 40 | 80 |
| 物质的量(mol) | 1.00 | 0.50 | 0.375 | 0.25 | 0.20 | 0.20 | 0.20 |
①氢气平衡转化率为
②
③保持其它条件不变,向平衡体系中充入1mol CO(g)、
(4)反应

| A.a反应正反应的活化能为 |
| B.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应 |
| C.b过程使用催化剂后降低了反应的活化能和 |
| D.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段 |

甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(g) ∆H1=-116kJ•mol-1
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是_______ 。
(2)已知:CO(g)+ O2(g)=CO2(g) ∆H2=-283kJ•mol-1
O2(g)=CO2(g) ∆H2=-283kJ•mol-1
H2(g)+ O2(g)=H2O(g) ∆H3=-242kJ•mol-1
O2(g)=H2O(g) ∆H3=-242kJ•mol-1
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为_______ 。
(3)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下:
回答下列问题:
①该反应的化学平衡常数表达式为K=_______ 。
②该反应_______ 反应(选填吸热、放热)。
③能判断该反应是否达到化学平衡状态的依据是_______ 。
④某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为_______ ℃。
⑤800℃时,发生上述反应,某一时刻测得容器内物质的浓度分别为:CO2为2mol•L-1,H2为1.5mol•L-1,CO为1mol•L-1,H2O为3mol•L-1,则此时反应向_______ (填“正反应方向”或“逆反应方向”)进行。
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是
a.随时将CH3OH与反应混合物分离 b.降低反应温度
c.增大体系压强 d.使用高效催化剂
(2)已知:CO(g)+
H2(g)+
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为
(3)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=
②该反应
③能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
④某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为
⑤800℃时,发生上述反应,某一时刻测得容器内物质的浓度分别为:CO2为2mol•L-1,H2为1.5mol•L-1,CO为1mol•L-1,H2O为3mol•L-1,则此时反应向
甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________。
(2)在一定体积的密闭容器中,进行如下化学反应: 其化学平衡常数K和温度t的关系如下:
其化学平衡常数K和温度t的关系如下:
回答下列问题:
①该反应___________ 反应(选填吸热、放热),平衡常数表达式K=___________ 。
②能判断该反应是否达到化学平衡状态的依据是___________ 。
a.容器中压强不变 b.混合气体中c(CO)不变
c. v正(H2)=v逆(H2O) d. c(CO2)=c(CO)
③830℃时,若起始时加入CO2、H2均为0.05mol,该温度下达到平衡时CO2转化率是___________ 。
(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是___________。
| A.随时将CH3OH与反应混合物分离 | B.降低反应温度 |
| C.增大体系压强 | D.使用高效催化剂 |
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应
②能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c. v正(H2)=v逆(H2O) d. c(CO2)=c(CO)
③830℃时,若起始时加入CO2、H2均为0.05mol,该温度下达到平衡时CO2转化率是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


