解答题-结构与性质 适中0.65 引用1 组卷285
回答下列问题
(1)基态Cr原子的核外电子排布式为___ 。
(2)基态S原子电子占据最高能级的电子云轮廓图为__ 形。
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式___ 。
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为___ 。
(5)下列状态的镁中,电离最外层一个电子所需能量最大的是___ 。
(6)利用CO可以合成化工原料COCl2,其中COCl2分子的结构式为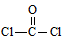 ,则COCl2分子内含有
,则COCl2分子内含有___ 。
(7)已知元素M的气态原子逐个失去第1至第4个电子所需能量如表所示:
元素M的常见化合价是___ 。
(1)基态Cr原子的核外电子排布式为
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(5)下列状态的镁中,电离最外层一个电子所需能量最大的是
A.[Ne]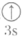 | B.[Ne]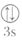 | C.[Ne] | D.[Ne]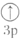 |
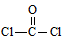 ,则COCl2分子内含有
,则COCl2分子内含有| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
| I1 | I2 | I3 | I4 | |
| 电离能/(kJ•mol-1) | 578 | 1817 | 2745 | 11578 |
元素M的常见化合价是
| A.+1 | B.+2 | C.+3 | D.+4 |
21-22高二上·辽宁沈阳·阶段练习
类题推荐
决定物质性质的重要因素是物质结构。请回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为______________ 。
(2)已知元素M是组成物质 的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号
的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示:
元素M化合态常见化合价是_________ 价,其基态原子电子排布式为_______
(3) 的中心原子的杂化方式为
的中心原子的杂化方式为__________ ,键角为____________
(4) 中非金属元素电负性由大到小的顺序为
中非金属元素电负性由大到小的顺序为_____________
(5)下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能: B.共价键的极性:
B.共价键的极性:
C.晶格能: D.热稳定性:
D.热稳定性:
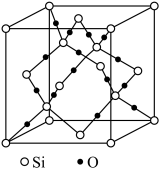
(6)如图是 晶胞,构成二氧化硅晶体结构的最小环是由
晶胞,构成二氧化硅晶体结构的最小环是由________ 个原子构成。已知晶胞参数为 ,则其晶胞密度为
,则其晶胞密度为________  。
。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)已知元素M是组成物质
| 电离能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是
(3)
(4)
(5)下列元素或化合物的性质变化顺序正确的是
A.第一电离能:
C.晶格能:
(6)如图是

决定物质性质的重要因素是物质结构。请回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______ nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据最高能层的符号是________ ,占据该能层电子的电子云轮廓图形状为________________ 。
(3)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
元素M化合态常见化合价是________ 价,其基态原子电子排布式为____________
(4)PO43-的中心原子的杂化方式为__________ ,键角为_______________
(5)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为________________
(6)下列元素或化合物的性质变化顺序正确的是__________________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
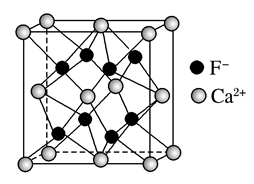
(7)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为_____________ ;已知Ca2+和F-半径分别为a cm、b cm,阿伏加 德罗常数为NA,M为摩尔质量,则晶体密度为___________________ g·cm-3(不必化简)。
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据最高能层的符号是
(3)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
(4)PO43-的中心原子的杂化方式为
(5)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为
(6)下列元素或化合物的性质变化顺序正确的是
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
(7)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为

回答下列问题
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
(2)Fe成为阳离子时首先失去_______ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为_______ 。
(3)Cu2+基态核外电子排布式为_______ 。
(4)Mn位于元素周期表中第四周期_______ 族,基态Mn原子核外未成对电子有_______ 个。
(5)基态Cl原子有_______ 种空间运动状态的电子,基态原子价电子排布式_______ ,属于_______ 区(填“s”或“p”或“d”或“f”)
(6)LiBH4由Li+和BH 构成,与BH
构成,与BH 互为等电子体的分子为
互为等电子体的分子为_______ ,Li、Be、B元素的电离能由大到小排列顺序为_______ 。
(7)1 mol HCHO分子中含有σ键的数目为_______ NA,CS2分子中,存在_______ 个 键和
键和_______ 个 键。
键。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A.[Ne] 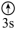 | B.[Ne] 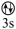 | C.[Ne]  | D.[Ne] 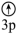 |
(3)Cu2+基态核外电子排布式为
(4)Mn位于元素周期表中第四周期
(5)基态Cl原子有
(6)LiBH4由Li+和BH
(7)1 mol HCHO分子中含有σ键的数目为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


