解答题-实验探究题 较易0.85 引用1 组卷128
研究小组探究Na2O2与水反应。向1.56gNa2O2粉末中加入40mL水,充分反应得溶液A(溶液体积变化忽略不计),进行实验。
实验1:向2mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为___ 。溶液A中NaOH溶液的物质的量浓度为___ 。
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末___ (填化学式),快速产生了能使带火星木条复燃的气体。
②实验3:向2mL物质的量浓度为___ mol/LNaOH溶液中滴入1滴酚酞,溶液变红色,10分钟后溶液褪色。向褪色的溶液中加入___ ,溶液变红色。
【得出结论】
③由以上实验可得出的结论是___ 。
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为___ 、___ ,但课本上没有写出中间产物H2O2,可能的原因是___ 。
实验1:向2mL溶液A中滴入1滴酚酞,溶液变红色,20秒后褪色。
(1)Na2O2与H2O反应的化学方程式为
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1:Na2O2与H2O反应可能生成了H2O2
猜想2:生成的NaOH浓度太大
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末
②实验3:向2mL物质的量浓度为
【得出结论】
③由以上实验可得出的结论是
【反思与评价】
(3)分析实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为
21-22高一上·北京丰台·期中
类题推荐
某同学通过实验研究Na2O2与水的反应。
为了探究溶液变为无色的原因,该同学按照科学的程序,进行了如下实验:
【推理与假设】
Na2O2与H2O反应的化学方程式_____ 。向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪色。由此提出如下的假设:
假设A:O2有漂白性 假设B:NaOH有漂白性 假设C:O2和NaOH共同作用有漂白性
【实验与观察】
(2)请完成下表:
【查阅资料】
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【推理与假设】
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
【实验与观察】
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末____ (填化学式),快速产生了能使带火星木条复燃的气体。该同学进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案:取少量溶液a于试管中,_____ 。
【解释与结论】
(4)由以上实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为_____ ;但课本上没有写出中间产物H2O2,可能的原因是___ 。
| 操作 | 现象 |
| 向盛有少量Na2O2的试管中加入蒸馏水,得到溶液a | 反应剧烈,产生能使带火星木条复燃的气体 |
| 然后向溶液a中滴入两滴酚酞 | 溶液先变红,再逐渐变浅,约10分钟溶液变为无色 |
【推理与假设】
Na2O2与H2O反应的化学方程式
假设A:O2有漂白性 假设B:NaOH有漂白性 假设C:O2和NaOH共同作用有漂白性
【实验与观察】
(2)请完成下表:
| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 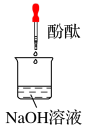 | 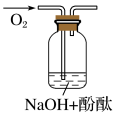 | 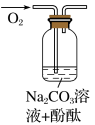 |
| 实验假设 (填“A”、“B”或“C”) | 假设 | 假设 | 假设 |
| 实验现象 | 溶液变红后10分钟均无变化 | ||
| 实验结论 | |||
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【推理与假设】
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
【实验与观察】
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末
【解释与结论】
(4)由以上实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为
为进一步研究过氧化钠与水的反应,某活动小组进行了如下研究。
(1)把一定量的水滴入盛有少量过氧化钠固体的试管中,反应的化学方程式为___________ 。
(2)向反应后的溶液中滴入酚酞,一段时间后,发现溶液颜色逐渐变浅,最后颜色消失。同学们为了探究酚酞褪色的原因,进行实验Ⅰ(环境温度为30℃),实验结果如下:
结合表中数据,判断下列说法正确的是___________ 。(填写字母)
a.其他条件相同时,NaOH溶液浓度越大褪色越快
b.溶液褪色可能是NaOH溶液浓度过大导致的
c.当NaOH溶液浓度大于或等于1.0 mol/L时,对溶液颜色变化有明显颖茜
(3)为进一步探究溶液的褪色原因,活动小组接着做了以下实验:
i.取1.56gNa2O2粉末加入到40mL水中,充分反应得溶液A(溶液体积几乎无变化),则所得溶液的物质的量浓度为________ 。
ii.实验2操作和现象如下:
下列说法不正确的是________ 。
A.由②中现象i可知,Na2O2与水反应有H2O2生成
B.由③、④可知,②中溶液红色褪去是因为c(OH-)大
C.由②、③、④可知,①中溶液红色褪去的主要原因不是c(OH-)大
D.向①中褪色后的溶液中滴加5滴6mol/L盐酸,溶液最终变为红色
(1)把一定量的水滴入盛有少量过氧化钠固体的试管中,反应的化学方程式为
(2)向反应后的溶液中滴入酚酞,一段时间后,发现溶液颜色逐渐变浅,最后颜色消失。同学们为了探究酚酞褪色的原因,进行实验Ⅰ(环境温度为30℃),实验结果如下:
| NaOH溶液浓度/mol·L-1 | 10.0 | 2.0 | 1.0 | 0.10 | 0.010 |
| 滴入酚酞时现象 | 深紫红色 | 深红色 | 深红色 | 深红色 | 深红色 |
| 溶液变为浅红色时间 | 2-3s | 26-30s | 54-60 s | 6-7min | 45min内稳定不变 |
| 溶液完全褪色时间 | 7-8 s | 50-54s几乎无色 | 100-110s几乎无色 | 20min后仍为浅红色 | 2h后略变浅 |
| 最终溶液是否褪色 | 褪色 | 褪色 | 褪色 | 不褪色 | 不褪色 |
a.其他条件相同时,NaOH溶液浓度越大褪色越快
b.溶液褪色可能是NaOH溶液浓度过大导致的
c.当NaOH溶液浓度大于或等于1.0 mol/L时,对溶液颜色变化有明显颖茜
(3)为进一步探究溶液的褪色原因,活动小组接着做了以下实验:
i.取1.56gNa2O2粉末加入到40mL水中,充分反应得溶液A(溶液体积几乎无变化),则所得溶液的物质的量浓度为
ii.实验2操作和现象如下:
| 编号 | ① | ② | ③ | ④ |
| 操作 |  |  | 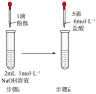 |  |
| 现象 | 溶液变红色,20秒后褪色 | i.产生大量能使带火星木条复燃的气体; ii.溶液变红色,10分钟后褪色。 | i.溶液变红色,10分钟后溶液褪色; ii.变红色。 | 溶液变红色,2小时后无明显变化 |
A.由②中现象i可知,Na2O2与水反应有H2O2生成
B.由③、④可知,②中溶液红色褪去是因为c(OH-)大
C.由②、③、④可知,①中溶液红色褪去的主要原因不是c(OH-)大
D.向①中褪色后的溶液中滴加5滴6mol/L盐酸,溶液最终变为红色
某同学通过实验研究Na2O2与水的反应的实质。
为了探究溶液变为无色的原因,该同学按照科学的程序,进行了如下实验:
【推理与假设】
(1)Na2O2与H2O反应的化学方程式:_______ 。
向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪色。由此提出如下的假设:
假设A:O2有漂白性
假设B:NaOH有漂白性
假设C:O2和NaOH共同作用有漂白性
【实验与观察】
(2)请完成下表:
【查阅资料】
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【推理与假设】
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
【实验与观察】
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末_______ (填化学式),快速产生了能使带火星木条复燃的气体。该同学进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案:取少量溶液a于试管中,_______ 。
【解释与结论】
(4)由以上实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为_______ ,_______ 。
| 操作 | 现象 |
| 向盛有少量Na2O2的试管中加入蒸馏水,得到溶液a | 反应剧烈,产生能使带火星木条复燃的气体 |
| 然后向溶液a中滴入两滴酚酞 | 溶液先变红,再逐渐变浅,约10分钟溶液变为无色 |
【推理与假设】
(1)Na2O2与H2O反应的化学方程式:
向溶液a中滴加酚酞本应只会变红,而实验中发现酚酞变红后又褪色。由此提出如下的假设:
假设A:O2有漂白性
假设B:NaOH有漂白性
假设C:O2和NaOH共同作用有漂白性
【实验与观察】
(2)请完成下表:
| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 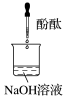 |  | 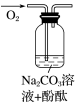 |
| 验证假设 | 假设 | 假设 | 假设 |
| 实验现象 | 溶液变红后10分钟均无变化 | ||
| 实验结论 | |||
【查阅资料】
该同学查阅资料:H2O2是一种在碱性条件下不稳定、具有漂白性的物质。
【推理与假设】
该同学认为褪色的原因可能是溶液a中存在H2O2,H2O2漂白了酚酞。
【实验与观察】
(3)通过实验证实了H2O2的存在:取少量溶液a,加入黑色粉末
【解释与结论】
(4)由以上实验结果可知,Na2O2与H2O反应的化学方程式如果分两步书写,应为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


