解答题-原理综合题 较难0.4 引用1 组卷317
丙烯是重要的化工原料,可以用于生产丙醇,卤代烃和塑料。因此生产丙烯具有重要的经济效益和社会价值。用二氧化碳氧化丙烷可以制丙烯,丙烷经催化脱氢也可制备丙烯:C3H8 C3H6+H2。
C3H6+H2。
(1)用二氧化碳氧化丙烷制丙烯主要反应如下:
I.C3H8(g)+CO2(g) C3H6(g)+CO(g)+H2O(g) ∆H1=+47 kJ/mol
C3H6(g)+CO(g)+H2O(g) ∆H1=+47 kJ/mol
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=-76 kJ/mol
CO(g)+H2O(g) ∆H2=-76 kJ/mol
III.丙烷经催化脱氢制丙烯的热化学方程式为:___________ 。
(2)将一定浓度的CO2与固定浓度的C3H8通过含催化剂的恒容反应器,在600℃时经相同时间,流出的C3H6、CO和H2浓度随初始CO2浓度的变化关系如图。
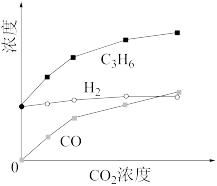
根据上图分析,如果只根据反应III C3H8(g) C3H6(g)+H2(g),生成的C3H6、H2的浓度随CO2浓度变化趋势应该是一致的,但是氢气的变化不明显,反而是CO与C3H6的变化趋势是一致的,推测可能的原因:
C3H6(g)+H2(g),生成的C3H6、H2的浓度随CO2浓度变化趋势应该是一致的,但是氢气的变化不明显,反而是CO与C3H6的变化趋势是一致的,推测可能的原因:___________ ;其他条件不变,投料比c(C3H8)/c(CO2)越大,C3H8转化率___________ (填“越大”,“越小”,“无影响”),该反应的平衡常数___________ (填“增大”,“减小”,“不变”)。
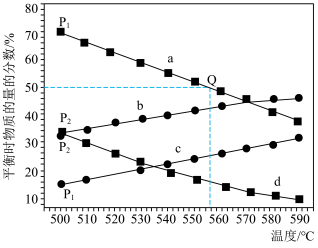
(3)C3H8(g) C3H6(g)+H2(g)在不同温度下达到平衡,在总压强分别为P1和P2时,测得丙烷及丙烯的物质的量分数如图所示:
C3H6(g)+H2(g)在不同温度下达到平衡,在总压强分别为P1和P2时,测得丙烷及丙烯的物质的量分数如图所示:
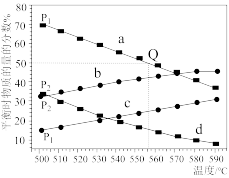
图中a,b,c,d代表丙烷或丙烯,则a,d代表___________ ,P1___________ P2(填“大于”“小于”“等于”);若P1=0.2MPa,起始时充入一定量的丙烷在恒压条件下发生反应,计算Q点对应温度下丙烷的转化率为___________ (保留一位小数),该反应的平衡常数KP=___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
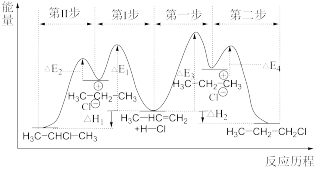
(4)丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示。其中正确的说法是___________。
(1)用二氧化碳氧化丙烷制丙烯主要反应如下:
I.C3H8(g)+CO2(g)
II.CO2(g)+H2(g)
III.丙烷经催化脱氢制丙烯的热化学方程式为:
(2)将一定浓度的CO2与固定浓度的C3H8通过含催化剂的恒容反应器,在600℃时经相同时间,流出的C3H6、CO和H2浓度随初始CO2浓度的变化关系如图。

根据上图分析,如果只根据反应III C3H8(g)
(3)C3H8(g)

图中a,b,c,d代表丙烷或丙烯,则a,d代表
(4)丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示。其中正确的说法是___________。

| A.丙烯与HCl发生的反应是放热反应,所以能自发进行 |
| B.合成CH3CHClCH3的反应中,第I步反应为整个反应的决速步骤 |
| C.从能量角度看,较稳定的产物是CH3CHClCH3 |
| D.总反应CH2=CH-CH3(g)+HCl(g)=CH3CH2CH2Cl(g)的∆H=∆E3-∆E4 |
21-22高三上·全国·期中
类题推荐
丙烯是重要的化工原料,可用于生产丙醇、卤代经和塑料。
(1)工业上用丙烯加成法制备1,2—二氯丙烷,主要副产物为3—氯丙烯。反应原理为:
①
②
已知: 的活化能Ea(逆)为164kJ/mol,则该反应的活化能Ea(正)为
的活化能Ea(逆)为164kJ/mol,则该反应的活化能Ea(正)为_______ kJ/mol。
(2)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前180min内平均反应速率v(
,则反应①前180min内平均反应速率v( )=
)=_______ kPa/min(保留2位小数)。
(3) 在不同温度下达到平衡,在总压强分别为p1和p2时,测得丙烷及丙烯的物质的量分数如图1所示。
在不同温度下达到平衡,在总压强分别为p1和p2时,测得丙烷及丙烯的物质的量分数如图1所示。
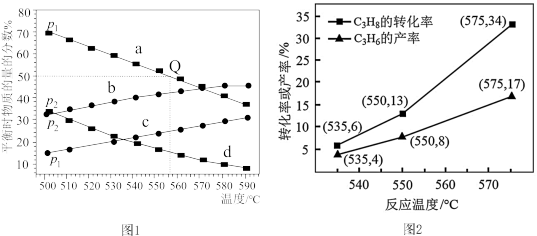
则a、d代表_______ ,p1_______ p2(填“大于”“小于”或“等于”);若p1=0.2MPa,起始时充入一定量的丙烷,在恒压条件下发生反应,Q点对应温度下丙烷的转化率为_______ (保留1位小数),该反应的平衡常数Kp=_______ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)丙烷氧化脱氢法制备丙烯还生成CO、 等副产物,制备丙烯的反应:
等副产物,制备丙烯的反应: ,在催化剂作用下,
,在催化剂作用下, 的转化率和
的转化率和 的产率随温度变化关系如图2所示。
的产率随温度变化关系如图2所示。 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是_______ 。
(1)工业上用丙烯加成法制备1,2—二氯丙烷,主要副产物为3—氯丙烯。反应原理为:
①
②
已知:
(2)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
(3)

则a、d代表
(4)丙烷氧化脱氢法制备丙烯还生成CO、
丙烯是重要的有机化工原料,丙烷脱氢制丙烯具有显著的经济价值和社会意义,其反应为:C3H8(g) C3H6(g)+H2(g) ΔH。
C3H6(g)+H2(g) ΔH。
(1)已知相关物质的燃烧热数据如表所示:
ΔH=___ kJ·mol-1。
(2)一定温度下,向10L恒容密闭容器中充入2molC3H8发生反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.75倍。则0~10min内丙烯的生成速率v(C3H6)=___ ,C3H8的平衡转化率为___ 。
(3)总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示:

①压强:P1___ P2(填“>”或“<”)。
②为提高反应速率和反应物的转化率,可采取的措施是___ 。
③若P1=0.1MPa,起始时充入一定量的丙烷在恒压条件下发生反应,计算Q点对应温度下该反应的平衡常数KP=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④工业生产中,在0.1MPa、527℃条件下,向反应器中通入丙烷和稀有气体,发生丙烷脱氢反应,随着 的增加,丙烷脱氢转化率逐渐增大。试解释原因
的增加,丙烷脱氢转化率逐渐增大。试解释原因___ 。
(4)高温下,丙烷脱氢反应在初始阶段的速率方程为:r=k×c(C3H8),其中k为反应速率常数。对于处于初期阶段的该反应,下列说法正确的是___ 。
(1)已知相关物质的燃烧热数据如表所示:
| 物质 | C3H8(g) | C3H6(g) | H2(g) |
| 燃烧热ΔH/(kJ·mol-1) | -2217.8 | -2058.3 | -285.8 |
(2)一定温度下,向10L恒容密闭容器中充入2molC3H8发生反应,经过10min达到平衡状态,测得平衡时气体压强是开始的1.75倍。则0~10min内丙烯的生成速率v(C3H6)=
(3)总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示:

①压强:P1
②为提高反应速率和反应物的转化率,可采取的措施是
③若P1=0.1MPa,起始时充入一定量的丙烷在恒压条件下发生反应,计算Q点对应温度下该反应的平衡常数KP=
④工业生产中,在0.1MPa、527℃条件下,向反应器中通入丙烷和稀有气体,发生丙烷脱氢反应,随着
(4)高温下,丙烷脱氢反应在初始阶段的速率方程为:r=k×c(C3H8),其中k为反应速率常数。对于处于初期阶段的该反应,下列说法正确的是
| A.增加丙烷浓度,r增大 | B.增加H2浓度,r增大 |
| C.丙烯的生成速率逐渐增大 | D.降低反应温度,k减小 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网