解答题-实验探究题 适中0.65 引用7 组卷646
(一)
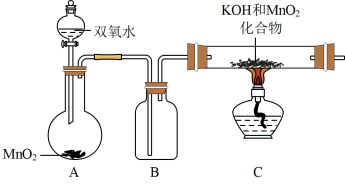
步骤Ⅰ.先利用下图所示装置制备
(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成
步骤Ⅱ.由
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的
⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得
(4)过程②向滤液中通入足量
(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸
(5)写出
(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①
21-22高三上·河北邢台·阶段练习
类题推荐
KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。
(一)KMnO4的制备,分步骤I、II两步进行。
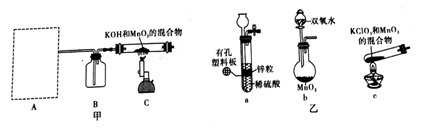
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用______ (填a、b或c)。
(2)装置B中所盛试剂的名称为______ 。
(3)装置C处反应生成K2MnO4的化学方程式为______ 。
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为______ ;
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
(5)为完成实验目的,H2C2O4溶液的物质的量浓度不低于______ 。
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=______ 。
(一)KMnO4的制备,分步骤I、II两步进行。
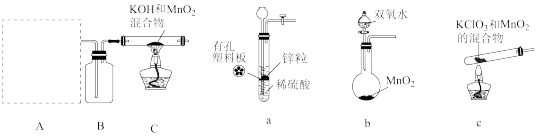
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成K2MnO4的化学方程式为
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 一定浓度mol·L-1 H2C2O4溶液 | H2O | 0.05 mol·L-1 KMnO4溶液 | 3 mol·L-1稀硫酸 | ||
| 1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
| 2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
| 3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网