解答题-原理综合题 较易0.85 引用2 组卷256
载人航天器中,可将航天员呼出的CO2转化为 H2O,再通过电解 H2O 获得 O2,实现 O2的再 生,同时还能制备 CH4.已知:
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于_______ (填“吸热”或“放热”)反应。
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =_______ kJ/mol。
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
①已知2CH4(g)=C2H4(g)+2H2(g) ΔH =+167kJ/mol,则a=_______ 。
②已知5C2H4(g)+12 (aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为
(aq)+36H+ (aq)=12Mn2+ (aq)+10CO2 (g)+28H2O(l) ΔH =-m kJ·mol-1,当放出的热量为n kJ时,该反应转移电子的物质的量为_______ mol。(用含m、n 的代数式表示)
③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图
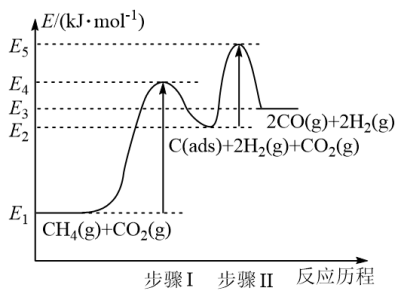
E4-E1表示步骤Ⅰ正反应的_______ ,制备合成气反应可在_______ (填“高温” 或“低温”)下自发进行。
①CO2(g)+4H2(g)=CH4(g)+2H2O(l) ∆H =-252.9kJ/mol
②2H2O(l)=2H2(g)+O2(g) ∆H =571.6kJ/mol
请回答下列问题:
(1)反应①属于
(2)反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H =
(3)利用 CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5C2H4(g)+12
③制备合成气反应历程分两步,步骤Ⅰ:CH4(g)⇌ C(ads)+2H2(g);步骤Ⅱ:C(ads)+ CO2(g)⇌ 2CO(g)。上述反应中 C(ads)为吸附性活性炭,反应历程的能量变化如图

E4-E1表示步骤Ⅰ正反应的
21-22高二上·湖北·期中
类题推荐
化学反应过程伴随有热量的变化。
(1)下列反应中属于吸热反应的有_______ 。
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败
(2)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
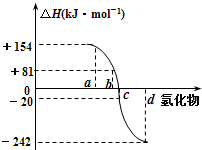
①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为______ 。
②硫化氢发生分解反应的热化学方程式为_____________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知2CH4(g) = C2H4(g) + 2H2(g) ΔH= +167 kJ/mol,则a=____ 。
②已知5C2H4(g)+12MnO (aq)+36H+(aq)=12Mn2+ (aq)+10CO2(g)+28H2O(l) ΔH= —m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+ (aq)+10CO2(g)+28H2O(l) ΔH= —m kJ·mol-1,当放出的热量为n kJ时,该反应转移的电子数为________ 。(用含m、n的代数式表示)
③ 制备合成气反应历程分两步,步骤 Ⅰ:CH4(g) C(ads) +2H2(g);步骤Ⅱ:C(ads) + CO2(g)
C(ads) +2H2(g);步骤Ⅱ:C(ads) + CO2(g) 2CO(g)。上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
2CO(g)。上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
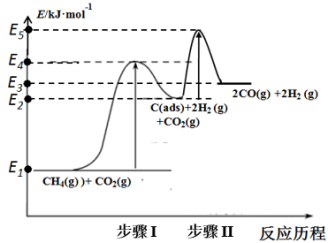
E4 – E1表示步骤①正反应的__________ ,决定制备合成气反应速率的是_________ (填“步骤 Ⅰ”或“步骤Ⅱ”);该反应可在___________ (填“高温”或“低温”)下自发进行。
(1)下列反应中属于吸热反应的有
①燃烧木炭取暖 ②C与H2O(g)反应制取水煤气 ③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌 ⑤食物因氧化而腐败
(2)一定条件下,由稳定单质反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为
②硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
①已知2CH4(g) = C2H4(g) + 2H2(g) ΔH= +167 kJ/mol,则a=
②已知5C2H4(g)+12MnO
③ 制备合成气反应历程分两步,步骤 Ⅰ:CH4(g)

E4 – E1表示步骤①正反应的
化学反应过程伴随有热量的变化。
(1)下列反应中属于吸热反应的有___________ 。(填序号)
①C与H2O(g)反应制取水煤气
②食物因氧化而腐败
③煅烧石灰石(主要成分是CaCO3)制生石灰
④燃烧木炭取暖
⑤氯化铵晶体和 混合搅拌
混合搅拌
(2)已知在298K、101kPa下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
)。图为ⅥA族元素氢化物a、b、c、d的生成热数据示意图。
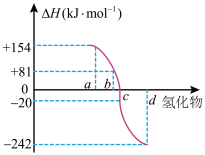
硫化氢发生分解反应的热化学方程式为___________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
①已知 ,则
,则
___________ 。
②已知 ,当放出的热量为
,当放出的热量为 时,该反应转移电子的物质的量为
时,该反应转移电子的物质的量为___________ 。(用含m、n的代数式表示)
③制备合成气反应历程分两步,步骤Ⅰ: ;步骤Ⅱ:
;步骤Ⅱ: 。
。
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
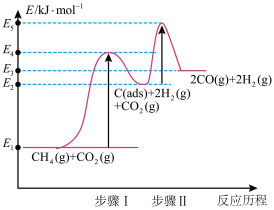
步骤Ⅱ正反应的活化能为___________ ,决定制备合成气反应速率的是___________ (填“步骤Ⅰ”或“步骤Ⅱ”)。
(1)下列反应中属于吸热反应的有
①C与H2O(g)反应制取水煤气
②食物因氧化而腐败
③煅烧石灰石(主要成分是CaCO3)制生石灰
④燃烧木炭取暖
⑤氯化铵晶体和
(2)已知在298K、101kPa下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(

硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如下表:
| 化学键 | ||||
②已知
③制备合成气反应历程分两步,步骤Ⅰ:
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:

步骤Ⅱ正反应的活化能为
化学反应过程伴随有热量的变化。
(1)下列过程中属于放热反应的有___________ 。
①燃烧木炭取暖②C与H2O(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌⑤金属腐蚀⑥浓硫酸稀释
(2)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。
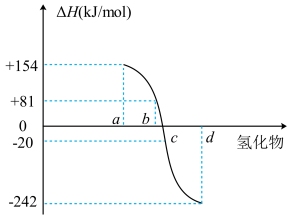
①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为___________ 。
②硫化氢发生分解反应的热化学方程式为___________ 。
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
①已知2CH4(g)=CH2=CH2(g)+2H2(g) ΔH=+167kJ/mol,则a=___________ 。
②已知5C2H4(g)+12MnO (aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) ΔH=-mkJ·mol-1,当放出的热量为nkJ时,该反应转移的电子数为
(aq)+36H+(aq)=12Mn2+(aq)+10CO2(g)+28H2O(l) ΔH=-mkJ·mol-1,当放出的热量为nkJ时,该反应转移的电子数为___________ 。(用含m、n的代数式表示)
③制备合成气反应历程分两步(步骤I、步骤II),反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
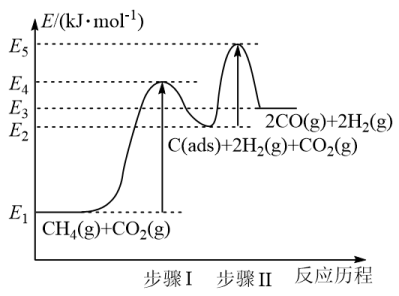
步骤I反应的焓变ΔH1为___________ kJ/mol(选用E1~E5的关系式表示)
④反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的焓变为ΔH2,与步骤Ⅰ反应的焓变ΔH1相比,ΔH1___________ ΔH2(填“>”或“<”)
(1)下列过程中属于放热反应的有
①燃烧木炭取暖②C与H2O(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO3)制生石灰④氯化铵晶体和Ba(OH)2·8H2O混合搅拌⑤金属腐蚀⑥浓硫酸稀释
(2)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(ΔH)。图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。

①非金属元素氢化物的稳定性与氢化物的生成热ΔH的关系为
②硫化氢发生分解反应的热化学方程式为
(3)利用CH4可制备乙烯及合成气(CO、H2)。有关化学键键能(E)的数据如表:
| 化学键 | H-H | C=C | C-C | C-H |
| E(kJ/mol) | 436 | a | 348 | 413 |
②已知5C2H4(g)+12MnO
③制备合成气反应历程分两步(步骤I、步骤II),反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:

步骤I反应的焓变ΔH1为
④反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的焓变为ΔH2,与步骤Ⅰ反应的焓变ΔH1相比,ΔH1
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


