填空题 适中0.65 引用1 组卷229
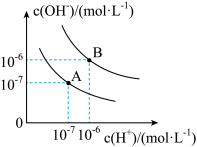
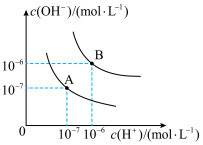
已知水在25 ℃和95 ℃时的电离平衡曲线如图所示。
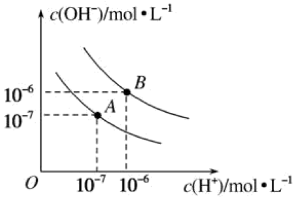
(1)25 ℃时水的电离平衡曲线应为_______ (填“A”或“B”)。25 ℃时,将pH=9的 NaOH 溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则 NaOH 溶液与 H2SO4溶液的体积比为 _______ 。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是_______ 。
(3)在曲线 A 所对应的温度下,pH=2的 HCl溶液和pH=11的某BOH 溶液中,若水的电离程度分别用α1、α2表示,则α1_______ α2(填“大于”“小于”“等于”“无法确定”)
(4)在曲线B所对应的温度下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=_______
(5)已知 HClO 的 Ka=2.98×10-8,CH3COOH 的 Ka=1.75×10-5,下列有关说法不正确的是

(1)25 ℃时水的电离平衡曲线应为
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(3)在曲线 A 所对应的温度下,pH=2的 HCl溶液和pH=11的某BOH 溶液中,若水的电离程度分别用α1、α2表示,则α1
(4)在曲线B所对应的温度下,将0.02mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=
(5)已知 HClO 的 Ka=2.98×10-8,CH3COOH 的 Ka=1.75×10-5,下列有关说法不正确的是
| A.在pH=2的醋酸溶液中加入少量0.01mol·L-1的稀盐酸,溶液的pH 不变 |
| B.在pH=2的醋酸溶液中加少量水,能促进醋酸的电离平衡,但是溶液的pH 会变大 |
| C.100mL pH=2的新制氯水中:n(OH- )+n(ClO-)+n(HClO)=0.001mol |
| D.由电离平衡常数分析,CH3COOH 溶液的pH 一定比 HClO 溶液的pH 小 |
21-22高二上·湖北·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网