填空题 适中0.65 引用1 组卷402
(1)很多金属或它们的化合物在灼烧的时候都会使火焰呈现出特征颜色,化学上把这种定性分析操作称为焰色实验,下列有关叙述中正确的是_______。
| A.焰色实验时可以用洁净的铜丝来代替铂丝进行实验 |
| B.用某样品做焰色实验时,直接观察到火焰呈黄色,可以确定该样品中不含钾元素 |
| C.节日燃放的五彩缤纷的烟花,就是利用了锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽的色彩 |
| D.焰色实验是元素的一种物理性质,属于物理变化 |
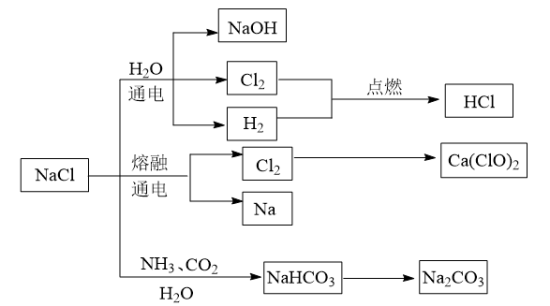
(3)工业制漂白粉的化学反应方程式为
(4)侯氏制碱法的原理是在饱和的食盐水中先通
(5)在实验室制备氯气时,可以用
(6)某研究性学习小组的同学在一次探究活动中,对一份纯碱样品(含有少量
21-22高一上·重庆渝中·期中
类题推荐
A~F六种物质的转化关系如图所示(部分反应物、产物和反应条件未写出),其中A为单质,B常用来作为潜水艇和呼吸面具中氧气来源,物质A到F的焰色试验均呈黄色。回答下列问题:
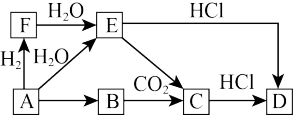
(1)该转化过程中A→B可以在热坩埚中进行,其现象为_______ ,化学反应方程式为_______ 。
(2)写出A→E的化学方程式并用单线桥标出电子转移的方向和数目_______ 。
(3)C的化学式为_______ ,向C的饱和溶液中通入足量 ,可观察到的现象是
,可观察到的现象是_______ 。
(4)F→E的化学方程式为_______ ,其中氧化剂是_______ (填化学式)。
(5)下列关于焰色试验说法错误的是_______(填标号)

(1)该转化过程中A→B可以在热坩埚中进行,其现象为
(2)写出A→E的化学方程式并用单线桥标出电子转移的方向和数目
(3)C的化学式为
(4)F→E的化学方程式为
(5)下列关于焰色试验说法错误的是_______(填标号)
| A.焰色试验时可以用洁净的铜丝来代替铂丝进行实验 |
| B.某样品做焰色试验时,直接观察到火焰呈黄色,可以确定该样品中不含钾元素 |
| C.节日燃放的五彩缤纷的烟花,就是锂、钠、钾、锶、钡等金属化合物所呈现的各种艳丽的色彩 |
| D.焰色试验是元素的一种物理性质,属于物理变化 |
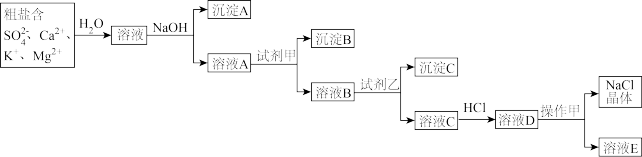
某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体( )和水处理剂高铁酸钾(
)和水处理剂高铁酸钾( )。
)。

请回答:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧胆矾时,铜的焰色为_______(填字母)。
(2)试剂X是_______ 。步骤I涉及到的分离操作是_______ 。
(3)在步骤II时,若用大理石与浓盐酸制取 并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是
并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体减少,可采取的改进措施是_______ 。
(4)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化_______ 。由溶液E制取 时,不同的温度下,不同质量浓度的
时,不同的温度下,不同质量浓度的 对
对 生成率有以下影响,由图可知工业生产中最佳条件(温度和
生成率有以下影响,由图可知工业生产中最佳条件(温度和 的质量浓度)为
的质量浓度)为_______ ,工业上制备 可用
可用 和
和 在碱性条件下制备,写出该反应的离子方程式
在碱性条件下制备,写出该反应的离子方程式_______ 。

(5)在固体F中加入稀硫酸和 来制备
来制备 溶液是一种环保工艺,该反应的总的化学方程式为
溶液是一种环保工艺,该反应的总的化学方程式为_______ 。

请回答:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧胆矾时,铜的焰色为_______(填字母)。
| A.黄色 | B.红色 | C.紫色 | D.绿色 |
(3)在步骤II时,若用大理石与浓盐酸制取
(4)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化

(5)在固体F中加入稀硫酸和
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网