单选题 适中0.65 引用2 组卷318
在一定条件下, 分解的化学方程式:
分解的化学方程式: ,
, 。学习小组研究浓度、温度、催化剂对
。学习小组研究浓度、温度、催化剂对 分解速率的影响,得到实验数据和图象:
分解速率的影响,得到实验数据和图象:
实验1:t℃无催化剂下,浓度对 分解速率的影响:
分解速率的影响:
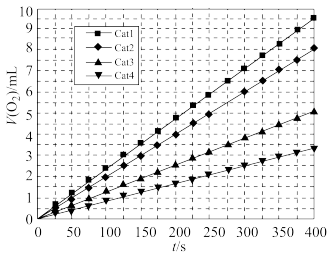
实验2:t℃下不同催化剂下生成 体积(V)与分解时间(t)的关系如图。下列说法正确的是
体积(V)与分解时间(t)的关系如图。下列说法正确的是
实验1:t℃无催化剂下,浓度对
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |

| A.增大 |
| B.保持温度不变,缩小反应容器的体积, |
| C.t℃无催化剂下生成 |
| D.其它条件相同下,用Cat1催化 |
21-22高三上·浙江·阶段练习
类题推荐
氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:I.
II.
III.
回答下列问题:
(1)写出 H2NCOONH4 分解生成 NH3 与 CO2 气体的热化学方程式:___________ 。
(2)在一定温度下,向 0.5L 密闭容器中,加入 0.1mol H2NCOONH4,实验测得 CO2 物质的量变化如下表所示:
从反应开始到 2min,用 NH3 的浓度变化表示的化学反应速率为___________ ;平衡后,H2NCOONH4 的转化率为___________ 。
(3)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
(4)对该反应,改变某一条件,对化学反应速率的影响及解释不正确的是___________。
已知:I.
II.
III.
回答下列问题:
(1)写出 H2NCOONH4 分解生成 NH3 与 CO2 气体的热化学方程式:
(2)在一定温度下,向 0.5L 密闭容器中,加入 0.1mol H2NCOONH4,实验测得 CO2 物质的量变化如下表所示:
t/min | 0 | 1 | 2 | 3 | 4 |
n/mol | 0 | a | b | c | c |
(3)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
| A.NH3 的浓度不再改变 | B. |
| C.容器体积不再改变 | D.容器内密度不再改变 |
| A.升高温度,使单位体积内活化分子百分数增加,反应速率加快 |
| B.增加反应物的量,使活化分子百分数增加,有效碰撞增多,反应速率加快 |
| C.使用催化剂能降低反应活化能,使单位体积内活化分子百分数增加,反应速率加快 |
| D.反应达平衡后,压缩体积增大压强,v 正 仍等于 v逆 |
Ⅰ.研究氮的氧化物解对环境保护有重要意义。
(1)已知反应 ,
, ,1mol
,1mol 、1mol
、1mol 分子中化学键断裂时分别需要吸收945kJ、498kJ的能量,则2mol
分子中化学键断裂时分别需要吸收945kJ、498kJ的能量,则2mol 分子中化学键断裂时需要吸收的能量为
分子中化学键断裂时需要吸收的能量为_______ kJ。
(2)实验1:在t℃时,无催化剂的恒容容器中,反应 起始压强为p0的部分实验数据如下:
起始压强为p0的部分实验数据如下:
①在0-30min 时段,反应速率 为
为_______  。
。
②若 起始浓度c0为
起始浓度c0为 ,则反应至50min时
,则反应至50min时 的转化率α=
的转化率α=_______ 。比较不同起始浓度时 的分解速率:
的分解速率:
_______  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③在该温度下,反应的平衡常数Kp=_______ (用p0表示,列计算式即可)。
④在t℃时,不同催化剂下产生氧气的体积 与分解时间的关系如下图,下列说法正确的是
与分解时间的关系如下图,下列说法正确的是_______ 。
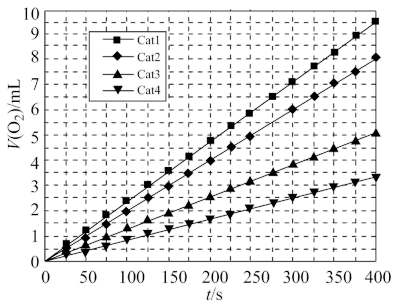
A.其他条件不变时,增大 的浓度,提高了单位体积
的浓度,提高了单位体积 的活化分子数,
的活化分子数, 的分解速率加快
的分解速率加快
B.保持温度不变,缩小反应容器的体积, 分解的速率加快
分解的速率加快
C.由上图可知,Catl催化效率最高
D.其他条件相同时,Catl催化分解 的活化能比用Cat4催化分解
的活化能比用Cat4催化分解 的活化能小。
的活化能小。
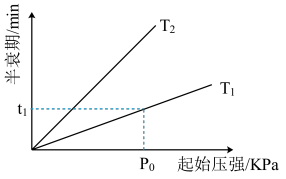
⑤不同温度(T)下, 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
_______  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
Ⅱ.科学家利用反应对汽车尾气进行无害化处理,发生如下反应: 。CO的平衡转化率与温度、起始投料比m的关系如图所示,图中起始投料比
。CO的平衡转化率与温度、起始投料比m的关系如图所示,图中起始投料比 。
。

(3)图中 与
与 大小关系是
大小关系是_______ 。
(4)a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是_______ 。
(5)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为_______ 。
(1)已知反应
(2)实验1:在t℃时,无催化剂的恒容容器中,反应
| 反应时间 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.010 |
①在0-30min 时段,反应速率
②若
③在该温度下,反应的平衡常数Kp=
④在t℃时,不同催化剂下产生氧气的体积

A.其他条件不变时,增大
B.保持温度不变,缩小反应容器的体积,
C.由上图可知,Catl催化效率最高
D.其他条件相同时,Catl催化分解
⑤不同温度(T)下,

Ⅱ.科学家利用反应对汽车尾气进行无害化处理,发生如下反应:

(3)图中
(4)a、b、c三点对应的平衡常数
(5)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为
氨是人科学技术发史上的一项重大突,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
常温下,大气固氮的倾向___________ 工业固氮(填“大于”或“小于”)
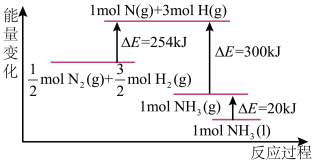
(2) 与
与 反应的能量变化如图所示,则
反应的能量变化如图所示,则 与
与 反应制备
反应制备 的热化学方程式为:
的热化学方程式为:___________ ;
(3)有关工业固氮的说法正确的是___________(选填序号)。
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位: )与催化剂的对应关系如表所示。
)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是_______ (填化学式)
(5)对于合成氨反应 ,下列研究结果和示意图相符的是
,下列研究结果和示意图相符的是_____ 。
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 0.1 | 1.847 | 0.504 | 0.152 | ||
常温下,大气固氮的倾向
(2)

(3)有关工业固氮的说法正确的是___________(选填序号)。
| A.使用催化剂可提高反应物的转化率 |
| B.循环使用 |
| C.温度控制在 |
| D.增大压强有利于加快反应速率,所以压强大越好 |
| 催化剂 | ||||||
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是
(5)对于合成氨反应
| 选项 | A | B | C | D |
| 研究结果 | 压强对反应的影响 | 温度对反应的影响 | 平衡体系增加 | 催化剂对反应的影响 |
| 图示 | 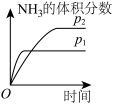 | 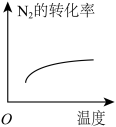 | 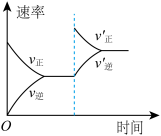 |  |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


