解答题-原理综合题 较难0.4 引用3 组卷232
乙烯是合成多种塑料的单体,我国科学家开发的特殊催化剂还原 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。
反应原理:
主反应:

副反应:

(1)已知: 、
、 的燃烧热(
的燃烧热( )分别是
)分别是 、
、 。
。

 。
。


______  。
。
(2)在一定温度下,向恒容密闭容器中充入 和
和 ,若只发生主反应,下列情况不能说明主反应达到平衡的是
,若只发生主反应,下列情况不能说明主反应达到平衡的是______ (填标号)。
A.混合气体密度保持不变B.混合气体总压强保持不变
C.乙烯体积分数保持不变D.气体平均摩尔质量保持不变
达到平衡后能提高 平衡转化率的措施是
平衡转化率的措施是______ (任填一条)。
(3)在 、
、 、
、 三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率(
三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率( )与温度关系如图1所示。
)与温度关系如图1所示。
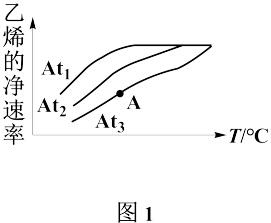
催化效率最高的是______ (填“ ”、“
”、“ ”或“
”或“ ”),A点的正反应速率
”),A点的正反应速率______ (填“大于”、“小于”或“等于”)逆反应速率。
(4)一定温度下,在容积为2L的恒容密闭容器中充入 和
和 ,同时发生了主反应和副反应,达到平衡时
,同时发生了主反应和副反应,达到平衡时 的转化率为45%,
的转化率为45%, 的选择性为80%,则该温度下,副反应的平衡常数
的选择性为80%,则该温度下,副反应的平衡常数
______ (结果保留2位小数)。
提示: 的选择性
的选择性
(5)常盖下,HCOOH的电离常数 ,将
,将 的NaOH溶液和
的NaOH溶液和 的HCOOH溶液等体积混合,得到混合溶液的pH
的HCOOH溶液等体积混合,得到混合溶液的pH______ (填“>”“<”或“=”)7。
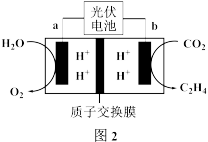
(6)以光伏电池为能源,采用电催化还原 制备乙烯,装置如图2所示,该装置阴极上的电极反应式为
制备乙烯,装置如图2所示,该装置阴极上的电极反应式为______ 。
反应原理:
主反应:
副反应:
(1)已知:
(2)在一定温度下,向恒容密闭容器中充入
A.混合气体密度保持不变B.混合气体总压强保持不变
C.乙烯体积分数保持不变D.气体平均摩尔质量保持不变
达到平衡后能提高
(3)在

催化效率最高的是
(4)一定温度下,在容积为2L的恒容密闭容器中充入
提示:
(5)常盖下,HCOOH的电离常数
(6)以光伏电池为能源,采用电催化还原

21-22高三上·河北保定·阶段练习
类题推荐
我国科学家修饰催化剂将 转化为烃的效率提高1000倍。已知:在某催化剂作用下,
转化为烃的效率提高1000倍。已知:在某催化剂作用下, 和
和 发生反应:
发生反应:

(1)已知 、
、 的燃烧热(
的燃烧热( )分别为
)分别为 、
、 ,
,
 ,则
,则

___________  。
。
(2)在恒容恒温条件下,向密闭容器中充入 、
、 ,加入合适催化剂,发生上述反应,下列情况表示达到平衡状态的是___________(填字母)。
,加入合适催化剂,发生上述反应,下列情况表示达到平衡状态的是___________(填字母)。
(3)在密闭容器中充入适量 和
和 发生上述反应,在催化剂作用下单位时间内
发生上述反应,在催化剂作用下单位时间内 的转化率与温度、催化剂关系如图1所示。
的转化率与温度、催化剂关系如图1所示。
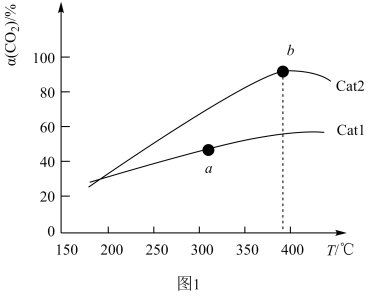
①在a点时, 的正反应速率
的正反应速率___________  的逆反应速率(填“大于”“小于”或“等于”)。催化效率:Cat2
的逆反应速率(填“大于”“小于”或“等于”)。催化效率:Cat2___________ Catl(填“>”“<”或“=”)。
②b点之后 的转化率降低,可能的原因是
的转化率降低,可能的原因是___________ 。
(4)在密闭容器中投入 和
和 发生上述反应,测得
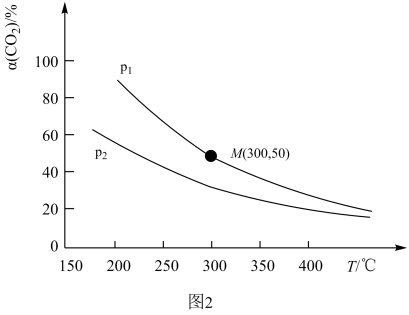
发生上述反应,测得 的平衡转化率与温度、压强的关系如图2所示。
的平衡转化率与温度、压强的关系如图2所示。
①
_______  (填“>”“<”或“=”)。随着温度升高,不同压强下,
(填“>”“<”或“=”)。随着温度升高,不同压强下, 的平衡转化率接近相等,其主要原因是
的平衡转化率接近相等,其主要原因是_______ 。
②已知M点对应的体积为1L,则在对应的温度下平衡常数K=___________ (只列计算式)。
(1)已知
(2)在恒容恒温条件下,向密闭容器中充入
| A.混合气体密度保持不变 | B.气体总压强保持不变 |
| C.气体平均摩尔质量保持不变 | D.混合气体中 |

①在a点时,
②b点之后
(4)在密闭容器中投入

①
②已知M点对应的体积为1L,则在对应的温度下平衡常数K=
2022年北京冬奥会主火炬首次采用以氢气为燃料的微火形式,体现了绿色奥运理念。工业上,利用天然气制备氢气,还可得到乙烯、乙炔等化工产品,有关反应原理如下:
反应1:

反应2:

请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
①能表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
②上述反应中,
_______  。
。
(2)向恒温恒容密闭容器中充入适量 ,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
(3)实验测得 的速率方程:
的速率方程: ,
, (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时
分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时 ,T2℃下反应达到平衡时
,T2℃下反应达到平衡时 。由此推知,T1
。由此推知,T1_______ (填“>”、“<”或“=”)T2。
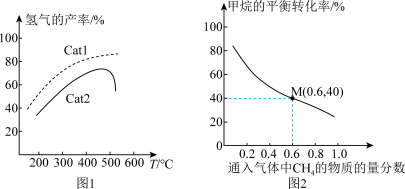
(4)在密闭容器中充入 ,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内
,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内 的产率与温度的关系如图1。在其他条件相同时,催化效率较高的
的产率与温度的关系如图1。在其他条件相同时,催化效率较高的_______ 是(填“Cat1”或“Cat2“”)。在Cat2作用下,温度高于500℃时, 的产率降低的可能原因是
的产率降低的可能原因是_______ 。
(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由 和
和 组成的混合气体(
组成的混合气体( 不参与反应),同时发生反应1和反应2,测得
不参与反应),同时发生反应1和反应2,测得 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图2。
的物质的量分数的关系如图2。
①图2中,随着通入气体中 的物质的量分数增大,甲烷的平衡转化率降低的主要原因是
的物质的量分数增大,甲烷的平衡转化率降低的主要原因是_______ 。
②已知M点对应的乙炔的选择性为75%[提示:乙炔的选择性 ]。该温度下,反应2的平衡常数
]。该温度下,反应2的平衡常数
_______ (结果保留2位有效数字)kPa。
提示:用平衡时气体分压计算的平衡常数为 ,气体分压等于气体总压×气体的物质的量分数。
,气体分压等于气体总压×气体的物质的量分数。
反应1:
反应2:
请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
| 物质 | ||||
| 燃烧热 | -890.3 | -1299.5 | -1411.0 | -285.8 |
②上述反应中,
(2)向恒温恒容密闭容器中充入适量
| A.气体总压强不随时间变化 | B.气体密度不随时间变化 |
| C.气体平均摩尔质量不随时间变化 | D. |
(4)在密闭容器中充入

(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由
①图2中,随着通入气体中
②已知M点对应的乙炔的选择性为75%[提示:乙炔的选择性
提示:用平衡时气体分压计算的平衡常数为
2022年北京冬奥会主火炬首次采用以氢气为燃料的微火形式,体现了绿色奥运理念。工业上,利用天然气制备氢气,还可得到乙烯、乙炔等化工产品,有关反应原理如下:
反应l:2CH4(g) C2H2(g)+3H2(g) △H1
C2H2(g)+3H2(g) △H1
反应2:2CH4(g) C2H4(g)+2H2(g) △H2
C2H4(g)+2H2(g) △H2
请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
能表示C2H2(g)燃烧热的热化学方程式为_______ 。
(2)向恒温恒容密闭容器中充入适量CH4,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
(3)实验测得2CH4(g) C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1
C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1_______ (填“>”、“<”或“=”)T2。
(4)在密闭容器中充入CH4,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图1。在其他条件相同时,催化效率较高的是_______ (填“Cat1”或“Cat2”)。在Cat2作用下,温度高于500°C时,H2的产率降低的可能原因是_______ 。
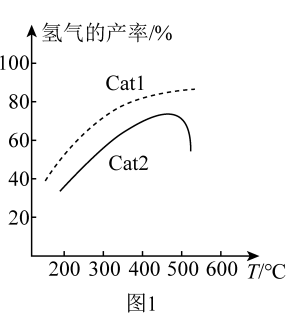
(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由CH4和N2组成的混合气体(N2不参与反应),同时发生反应1和反应2,测得CH4的平衡转化率与通入气体中CH4的物质的量分数的关系如图2。
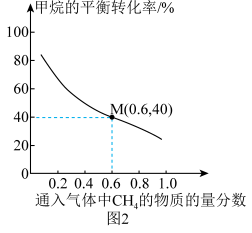
①图2中,随着通入气体中CH4的物质的量分数增大,甲烷的平衡转化率降低的主要原因是_______ 。
②已知M点对应的乙炔的选择性为75%[乙炔的选择性= ]。该温度下,生成的H2的分压为
]。该温度下,生成的H2的分压为_______ kPa。
反应l:2CH4(g)
反应2:2CH4(g)
请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
| 物质 | CH4(g) | C2H2(g) | C2H4(g) | H2(g) |
| 燃烧热(ΔH/kJ·mol-1) | -890.3 | -1299.5 | -1411.0 | -285.8 |
(2)向恒温恒容密闭容器中充入适量CH4,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
| A.气体总压强不随时间变化 | B.气体密度不随时间变化 |
| C.气体平均摩尔质量不随时间变化 | D.H2体积分数不随时间变化 |
(4)在密闭容器中充入CH4,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图1。在其他条件相同时,催化效率较高的是

(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由CH4和N2组成的混合气体(N2不参与反应),同时发生反应1和反应2,测得CH4的平衡转化率与通入气体中CH4的物质的量分数的关系如图2。

①图2中,随着通入气体中CH4的物质的量分数增大,甲烷的平衡转化率降低的主要原因是
②已知M点对应的乙炔的选择性为75%[乙炔的选择性=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


