解答题-原理综合题 较难0.4 引用3 组卷150
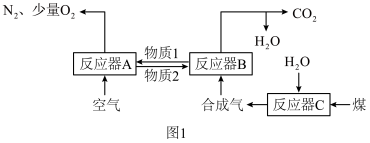
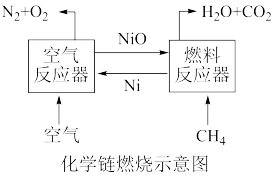
化学链燃烧技术的基本原理是将传统燃料与空气接触反应的燃烧借助载氧剂(如 ,FeO等)的作用分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
,FeO等)的作用分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
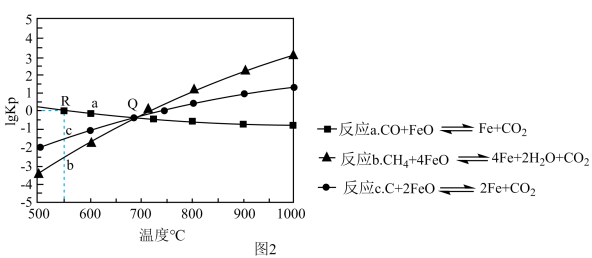
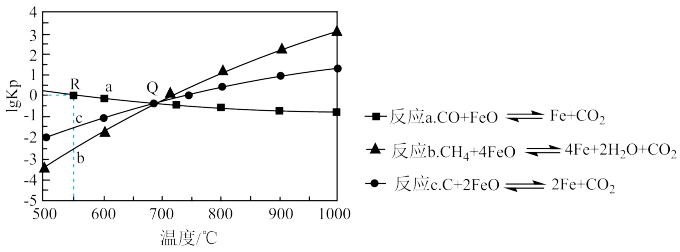
(1)用Fe0作载氧剂,部分反应的1g Kp与温度的关系如图所示。[已知:平衡常数Kp是用平衡分压代替平衡浓度(平衡分压=总压×物质的量分数)]
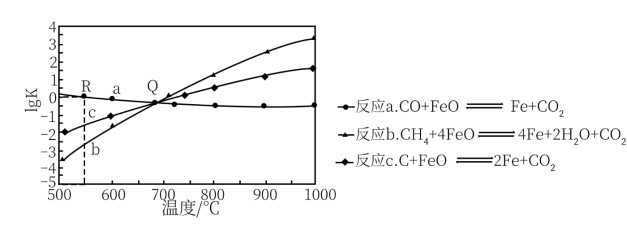
①图中涉及的反应中,属于吸热反应的是反应___________ (填字母a、b或c)。
②R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应 ,则CO的平衡转化率为
,则CO的平衡转化率为___________ 。
(2)在T℃下,向某恒容密闭容器中加入2mol (g)和8mol FeO(s)进行反应:
(g)和8mol FeO(s)进行反应: 。反应起始时压强为
。反应起始时压强为 ,达到平衡状态时,容器的气体压强是起始压强的2倍。
,达到平衡状态时,容器的气体压强是起始压强的2倍。
①反应达平衡时,容器内气体的总物质的量为___________ mol;
②T℃下,该反应的Kp=___________ 。
(3)一种微胶囊吸收剂,将煤燃烧排放的 以安全、高效的方式处理掉,胶囊内部充有
以安全、高效的方式处理掉,胶囊内部充有 溶液,其原理如图所示。
溶液,其原理如图所示。
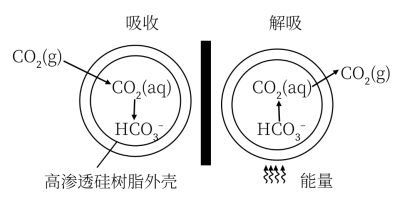
①这种微胶囊吸收 的原理是
的原理是___________ (用离子方程式表示)。
②将解吸后的 催化加氢可制取乙烯。
催化加氢可制取乙烯。
已知:






___________ 。
(1)用Fe0作载氧剂,部分反应的1g Kp与温度的关系如图所示。[已知:平衡常数Kp是用平衡分压代替平衡浓度(平衡分压=总压×物质的量分数)]

①图中涉及的反应中,属于吸热反应的是反应
②R点对应温度下,向某恒容密闭容器中通入1mol CO,并加入足量的FeO,只发生反应
(2)在T℃下,向某恒容密闭容器中加入2mol
①反应达平衡时,容器内气体的总物质的量为
②T℃下,该反应的Kp=
(3)一种微胶囊吸收剂,将煤燃烧排放的

①这种微胶囊吸收
②将解吸后的
已知:
21-22高三上·湖南·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网