解答题-原理综合题 较难0.4 引用2 组卷576
O2对人类有着重要的作用。请回答下列问题:
(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ. 2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0kJ•mol-1
ⅱ. 2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ•mol-1
ⅲ. CO(g)+2H2(g)=CH3OH(g) ΔH3=-574.4kJ•mol-1
则计算CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)的ΔH=
O2(g)=CO2(g)+2H2O(g)的ΔH=_______ kJ•mol-1。
(2)合成硝酸工艺中涉及到反应:2NO(g)+O2(g)=2NO2(g)、2NO2(g) N2O4(g)。T℃时,在恒容密闭容器中以投料比
N2O4(g)。T℃时,在恒容密闭容器中以投料比 =1:1进行投料,容器内总压强p的变化如下表:
=1:1进行投料,容器内总压强p的变化如下表:
已知:a. 2NO2(g) N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。
N2O4(g)可认为迅速达到平衡状态。b.时间t=∞时,NO(g)完全反应。
①已知时间为t1min时,测得容器内O2分压p(O2)=10.6 kPa,则此时NO的分压p(NO)_______ kPa。
②T℃时,可逆反应2NO2(g) N2O4(g)的平衡常数Kp=
N2O4(g)的平衡常数Kp=_______ kPa -1(用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可),NO2的平衡转化率为_______ %(保留2位有效数字)。
③若将上述反应容器内温度升高至(T+50)℃,达到平衡时,容器内混合气体的平均相对分子质量减小,则2NO2(g) N2O4(g)ΔH
N2O4(g)ΔH_______ 0(填“>”或“<”)。
(3)人体内化学反应时刻需要O2参与,如广泛存在于肌肉中的肌红蛋白( ),具有结合O2的能力,可表示为Mb(aq)+O2(g)
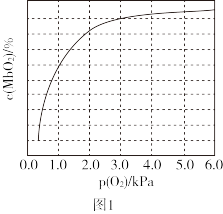
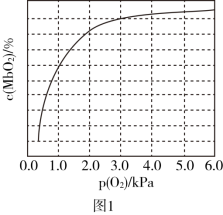
),具有结合O2的能力,可表示为Mb(aq)+O2(g) MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
MbO2(aq)。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压p(O2)密切相关,其变化曲线如图1,37℃时,测得平衡常数K=2(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
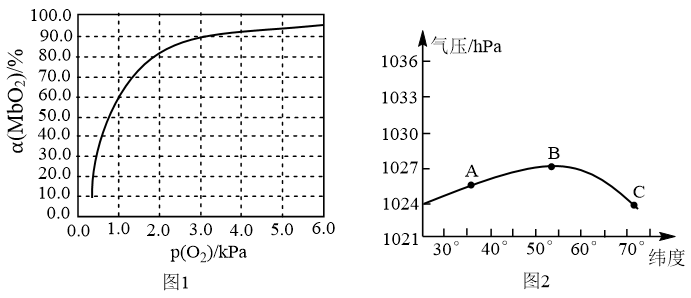
①平衡时,平衡常数表达式K=_______ [用含α和p(O2)的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压p(O2)=_______ kPa(保留3位有效数字)。
②某天不同纬度的大气压变化曲线如图2所示,某运动员处于A、B、C不同位置时,其体内MbO2的浓度最大位置为_______ (填“A”“B”或“C”)。
(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ. 2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0kJ•mol-1
ⅱ. 2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ•mol-1
ⅲ. CO(g)+2H2(g)=CH3OH(g) ΔH3=-574.4kJ•mol-1
则计算CH3OH(g)+
(2)合成硝酸工艺中涉及到反应:2NO(g)+O2(g)=2NO2(g)、2NO2(g)
| t/min | 0 | 40 | 80 | 160 | 260 | 700 | |
| p/kPa | 33.2 | 28.6 | 27.1 | 26.3 | 25.9 | 25.2 | 22.3 |
已知:a. 2NO2(g)
①已知时间为t1min时,测得容器内O2分压p(O2)=10.6 kPa,则此时NO的分压p(NO)
②T℃时,可逆反应2NO2(g)
③若将上述反应容器内温度升高至(T+50)℃,达到平衡时,容器内混合气体的平均相对分子质量减小,则2NO2(g)
(3)人体内化学反应时刻需要O2参与,如广泛存在于肌肉中的肌红蛋白(

①平衡时,平衡常数表达式K=
②某天不同纬度的大气压变化曲线如图2所示,某运动员处于A、B、C不同位置时,其体内MbO2的浓度最大位置为
21-22高三上·河北石家庄·阶段练习
类题推荐
氮及其化合物在工农业生产、生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一,
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-l
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-l
2C(s)+O 2(g)=2CO(g) ΔH=-221kJ·mol-l
若某反应的平衡常数表达式为:K= ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式 ___________ 。
(2)N2O5在一定条件下可发生分解:2N2O5(g) 4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
①反应开始时体系压强为P0,第3.00 min时体系压强为p1,则p1:p0= ___________ ;2.00min~5.00 min内,O2的平均反应速率为___________ 。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是___________ 。
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O4与NO2 之间存在反应:N2O4(g) 2NO2(g) ΔH=QkJ·mol-1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。
2NO2(g) ΔH=QkJ·mol-1。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图所示。
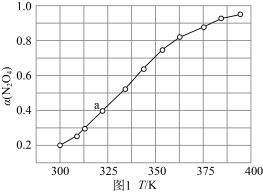
如图中a点对应温度下,已知N2O4的起始压强p0为200 kPa,该温度下反应的平衡常数Kp=___________ (小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
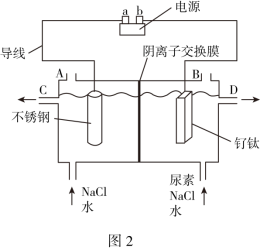
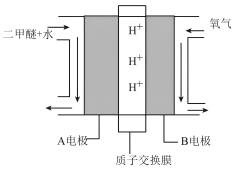
(4)绿色电源“直接二甲醚CH3OCH3(g)燃料电池”的工作原理示意图如图所示:正极为___________ (填“A电极”或“B电极”),写出A电极的电极反应式:___________ 。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-l
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-l
2C(s)+O 2(g)=2CO(g) ΔH=-221kJ·mol-l
若某反应的平衡常数表达式为:K=
(2)N2O5在一定条件下可发生分解:2N2O5(g)
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol/L) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是
a.容器中压强不再变化 b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5) d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O4与NO2 之间存在反应:N2O4(g)

如图中a点对应温度下,已知N2O4的起始压强p0为200 kPa,该温度下反应的平衡常数Kp=
(4)绿色电源“直接二甲醚CH3OCH3(g)燃料电池”的工作原理示意图如图所示:正极为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网