单选题 适中0.65 引用2 组卷230
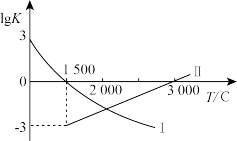
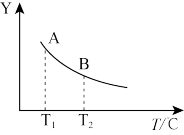
由铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有 广泛应用。高炉炼铁的反应为 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1。对于反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g),下列有关说法正确的是
| A.该反应一定能自发进行,则该反应的ΔS>0 |
| B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率 |
| C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数 |
| D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁慢 |
21-22高三上·江苏镇江·期中
类题推荐
高炉炼铁过程中发生反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
 2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )| 温度T/°C | 1000 | 1150 | 1300 |
| 平衡常数K | 4.0 | 3.7 | 3.5 |
| A.a>0 |
| B.当反应达到平衡时,在其他条件不变的情况下,加入少量的Fe2O3,CO的转化率不变 |
| C.为了使该反应的K增大,可以在其他条件不变时,增大c(CO) |
| D.1000°C下Fe2O3与CO反应,tmin达到平衡时c(CO)=2×10-3mol/L,则用CO表示该反应的平均速率为2×10-3/tmol/(L·min) |
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
Ⅰ.已知:2CO(g) + O2(g)=2CO2(g) ΔH=-566 kJ/mol
2Fe(s) + 3/2O2(g)=Fe2O3(s) ΔH=-825.5 kJ/mol
反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=
2Fe(s)+3CO2(g) ΔH=________ kJ/mol。
Ⅱ.反应1/3Fe2O3(s)+CO(g) 2/3 Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一容积为10 L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10min后达到平衡。
2/3 Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一容积为10 L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10min后达到平衡。
(1)CO的平衡转化率为__________ 。
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是_________ 。
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下与H2反应制备甲醇: CO(g)+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
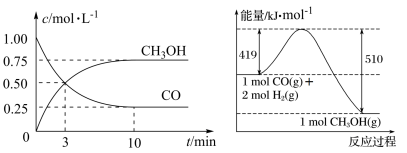
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率υ(H2)=_____________ 。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
则下列关系正确的是_________ (填序号)。
A .c1=c2;B.2Q1=Q3;C.2α1=α3;D.α1+α2=1;E.该反应若生成1 mol CH3OH,则放出(Q1+Q2)kJ热量
Ⅰ.已知:2CO(g) + O2(g)=2CO2(g) ΔH=-566 kJ/mol
2Fe(s) + 3/2O2(g)=Fe2O3(s) ΔH=-825.5 kJ/mol
反应:Fe2O3(s)+3CO(g)
Ⅱ.反应1/3Fe2O3(s)+CO(g)
(1)CO的平衡转化率为
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是
a.提高反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下与H2反应制备甲醇: CO(g)+2H2(g)

(1)从反应开始到平衡,用H2浓度变化表示平均反应速率υ(H2)=
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物 转化率 | CH3OH的浓度 | 能量变化 (Q1,Q2,Q3均大于0) |
| 甲 | 1 mol CO和2 mol H2 | α1 | c1 | 放出Q1 kJ热量 |
| 乙 | 1 mol CH3OH | α2 | c2 | 吸收Q2 kJ热量 |
| 丙 | 2 mol CO和4 mol H2 | α3 | c3 | 放出Q3 kJ热量 |
则下列关系正确的是
A .c1=c2;B.2Q1=Q3;C.2α1=α3;D.α1+α2=1;E.该反应若生成1 mol CH3OH,则放出(Q1+Q2)kJ热量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网