解答题-工业流程题 较难0.4 引用2 组卷152
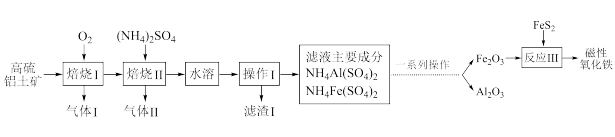
磁性氧化铁具有广阔的应用前景,中国已成为世界磁性材料生产大国。以高硫铝土矿(主要含 、
、 、
、 和少量的
和少量的 等)提取氧化铝和磁性氧化铁,其流程如图:
等)提取氧化铝和磁性氧化铁,其流程如图: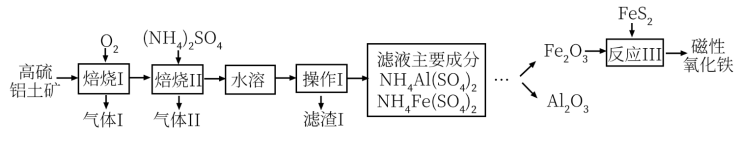
(1)磁性氧化铁的化学式为_______ ;写出滤渣Ⅰ主要成分的两种用途:_______ ;反应Ⅲ加入 的目的是作为
的目的是作为_______ (填“氧化剂”或“还原剂”)。
(2)操作Ⅰ在实验中要用到的玻璃仪器有_______ 。
(3)焙烧Ⅰ中, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
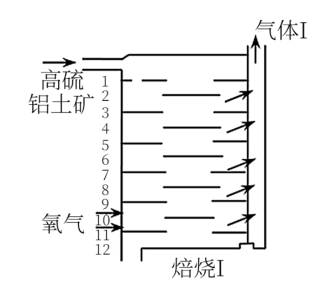
(4)焙烧Ⅰ的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是_______ (任答一点)。
(5)流程中“气体Ⅱ”的化学式为_______ ,焙烧Ⅱ中氧化铝参与反应的化学方程式为_______ 。
(6)为了测定mg高硫铝土矿中铝元素的含量,将流程中制取的 溶解于足量稀硫酸,配成100mL溶液,取出
溶解于足量稀硫酸,配成100mL溶液,取出 ,加入
,加入 标准溶液amL,调节溶液
标准溶液amL,调节溶液 并煮沸,冷却后用
并煮沸,冷却后用 标准溶液滴定过量的
标准溶液滴定过量的 至终点,消耗
至终点,消耗 标准溶液VmL(已知
标准溶液VmL(已知 、
、 与
与 反应的化学计量比均为1∶1)。则mg高硫铝土矿中铝元素的质量分数为
反应的化学计量比均为1∶1)。则mg高硫铝土矿中铝元素的质量分数为_______ (用含V、m、a、b、c的代数式表示)。

(1)磁性氧化铁的化学式为
(2)操作Ⅰ在实验中要用到的玻璃仪器有
(3)焙烧Ⅰ中,
(4)焙烧Ⅰ的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(5)流程中“气体Ⅱ”的化学式为
(6)为了测定mg高硫铝土矿中铝元素的含量,将流程中制取的
21-22高三上·重庆·阶段练习
类题推荐
磁性氧化铁是电讯器材的重要原料,以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)提取氧化铝和磁性氧化铁的流程如图:
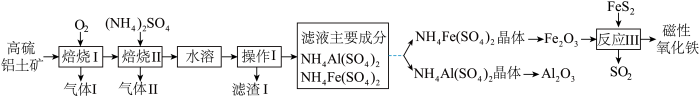
已知:不同温度下,NH4Fe(SO4)2和NH4Al(SO4)2的溶解度(g/100gH2O)如表:
(1)气体I中的成分中除氧气外,还有______ 。
(2)写出“焙烧II”中Fe2O3发生的化学反应方程式______ 。
(3)写出滤渣I主要成分的一种用途______ 。
(4)从滤液中获得NH4Al(SO4)2的操作是______ 。
(5)“反应III”在隔绝空气条件下进行,参与反应的n(FeS2):n(Fe2O3)=______ 。
(6)该工业流程中有多种气体产生,将它们综合利用可合成流程中的某种反应物,该合成总反应的化学方程式为______ 。
(7)为测定Al2O3产品的纯度(Al2O3的质量分数),称量mg样品溶解于足量稀硫酸,配成100.00mL溶液,取出20.00mL溶液,加入c1mol•L-1EDTA标准溶液V1mL,调节溶液pH并煮沸,冷却后用c2mol•L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V2mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则制得的Al2O3的纯度为______ (用代数式表示)。

已知:不同温度下,NH4Fe(SO4)2和NH4Al(SO4)2的溶解度(g/100gH2O)如表:
| 温度/℃ | 0 | 20 | 30 | 40 | 100 |
| NH4Fe(SO4)2 | 70.6 | 75.4 | 78.3 | 81.0 | 102.1 |
| NH4Al(SO4)2 | 2.1 | 5.0 | 7.7 | 10.9 | 26.7 |
(2)写出“焙烧II”中Fe2O3发生的化学反应方程式
(3)写出滤渣I主要成分的一种用途
(4)从滤液中获得NH4Al(SO4)2的操作是
(5)“反应III”在隔绝空气条件下进行,参与反应的n(FeS2):n(Fe2O3)=
(6)该工业流程中有多种气体产生,将它们综合利用可合成流程中的某种反应物,该合成总反应的化学方程式为
(7)为测定Al2O3产品的纯度(Al2O3的质量分数),称量mg样品溶解于足量稀硫酸,配成100.00mL溶液,取出20.00mL溶液,加入c1mol•L-1EDTA标准溶液V1mL,调节溶液pH并煮沸,冷却后用c2mol•L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液V2mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1:1)。则制得的Al2O3的纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网