填空题 适中0.65 引用1 组卷529
砷(As)是一些工厂和矿山废水中的污染元素,其剧毒、难降解且易生物聚集的特点极大的威胁了水环境安全和人体健康。天然水体中砷元素主要以As(III)和As(V)存在,且As(III)的毒性更大。常见除砷的方法有沉淀法、氧化絮凝法和离子交换法等。
(1)沉淀法除砷:砷酸盐的溶解度小,工业上需要将废水中和至pH>12,再用氧化剂将As(III)转化成As(V),然后用石灰乳沉淀除砷,得到Ca5(AsO4)3OH沉淀。“沉砷”的最佳温度控制在80~85℃的原因是_______ 。
(2)高铁酸盐氧化絮凝法除砷。
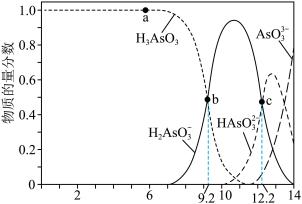
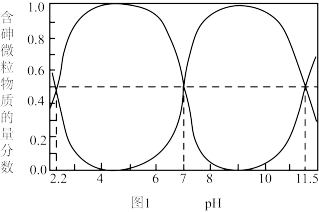
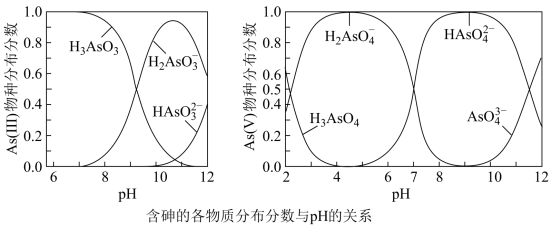
已知:a.As(III)和As(V)水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图所示。
b.高铁酸钾易溶于水,具有强氧化性;溶液酸性越强,其氧化性越强;在pH<1的酸性条件下质子化,主要以HFeO 形式存在。
形式存在。
c.高铁酸钾在一定pH范围的水溶液中易生成Fe(OH)3胶体,溶液的pH对胶体粒子表面所带电荷有影响。pH=7.1时,胶体粒子表面不带电荷;pH>7.1时,胶体粒子表面带负电荷,pH越高,表面所带负电荷越多;pH<7.1时,胶体粒子表面带正电荷,pH越低,表面所带正电荷越多。
①pH<1时,HFeO 将As(III)氧化为As(V)的离子方程式为
将As(III)氧化为As(V)的离子方程式为_______ 。
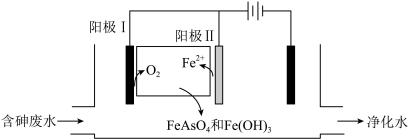
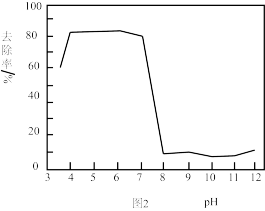
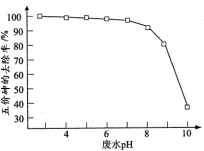
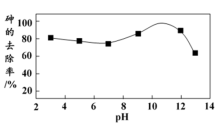
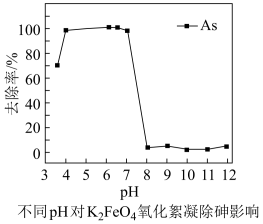
②在一定pH范围内,K2FeO4的还原产物可形成Fe(OH)3胶体,吸附As(V)的离子达到除砷目的;不同pH对K2FeO4氧化絮凝除砷影响如图所示。除砷过程中控制废水pH为4~7,pH过低或过高,砷的去除率都下降,其原因是_______ 。
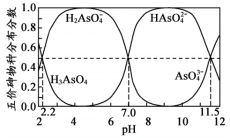
(3)离子交换法除砷:强碱性离子交换树脂上的OH与废水中的H2AsO 、HAsO
、HAsO 、AsO
、AsO 进行离子交换,OH-进入水中,H2AsO
进行离子交换,OH-进入水中,H2AsO 、HAsO
、HAsO 、AsO
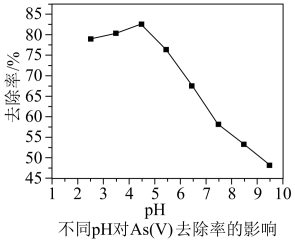
、AsO 被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是
被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是_______ 。
(1)沉淀法除砷:砷酸盐的溶解度小,工业上需要将废水中和至pH>12,再用氧化剂将As(III)转化成As(V),然后用石灰乳沉淀除砷,得到Ca5(AsO4)3OH沉淀。“沉砷”的最佳温度控制在80~85℃的原因是
(2)高铁酸盐氧化絮凝法除砷。
已知:a.As(III)和As(V)水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图所示。

b.高铁酸钾易溶于水,具有强氧化性;溶液酸性越强,其氧化性越强;在pH<1的酸性条件下质子化,主要以HFeO
c.高铁酸钾在一定pH范围的水溶液中易生成Fe(OH)3胶体,溶液的pH对胶体粒子表面所带电荷有影响。pH=7.1时,胶体粒子表面不带电荷;pH>7.1时,胶体粒子表面带负电荷,pH越高,表面所带负电荷越多;pH<7.1时,胶体粒子表面带正电荷,pH越低,表面所带正电荷越多。
①pH<1时,HFeO
②在一定pH范围内,K2FeO4的还原产物可形成Fe(OH)3胶体,吸附As(V)的离子达到除砷目的;不同pH对K2FeO4氧化絮凝除砷影响如图所示。除砷过程中控制废水pH为4~7,pH过低或过高,砷的去除率都下降,其原因是

(3)离子交换法除砷:强碱性离子交换树脂上的OH与废水中的H2AsO

21-22高三上·江苏盐城·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网