解答题-工业流程题 适中0.65 引用1 组卷75
磷酸二氢钾 是重要的精细磷酸盐,其大晶体已应用于我国研制的巨型激光器“神光二号”中。某兴趣小组制备
是重要的精细磷酸盐,其大晶体已应用于我国研制的巨型激光器“神光二号”中。某兴趣小组制备 的流程如下:
的流程如下:
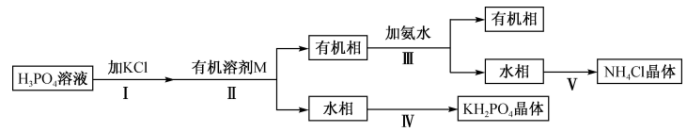
已知:a. 易溶于水,不溶于乙醇和醚等有机溶剂;溶解度随温度升高而增大。
易溶于水,不溶于乙醇和醚等有机溶剂;溶解度随温度升高而增大。
b.HCl易溶于乙醇和醚等有机溶剂。
回答下列问题:
(1)步骤II的实验操作中除烧杯外,还必须用到的硅酸盐材质的仪器有___________ 。
(2)有关步骤II和步骤III,下列说法正确的是___________(填标号)。
(3)试从平衡角度分析,由步骤I、II得到 溶液的原理:
溶液的原理:___________ 。
(4)步骤IV主要包括蒸发浓缩、冷却结晶、减压过滤、洗涤、干燥等多步操作,在冷却结晶操作中,为了得到 大晶体,常采取的措施有
大晶体,常采取的措施有___________ ;减压过滤后进行洗涤操作方法为___________ (洗涤剂用“X溶液”表示)。
(5)提纯 晶体的方法是
晶体的方法是___________ 。
(6)已知常温下,磷酸的电离常数 、
、 、
、 ,则
,则 溶液呈
溶液呈___________ (填“酸性”“碱性”或“中性”),并通过计算说明:___________ 。

已知:a.
b.HCl易溶于乙醇和醚等有机溶剂。
回答下列问题:
(1)步骤II的实验操作中除烧杯外,还必须用到的硅酸盐材质的仪器有
(2)有关步骤II和步骤III,下列说法正确的是___________(填标号)。
| A.有机溶剂M可用乙醇 |
| B.步骤III与步骤II的实验操作基本相同 |
| C. |
| D.有机溶剂M可循环使用 |
(4)步骤IV主要包括蒸发浓缩、冷却结晶、减压过滤、洗涤、干燥等多步操作,在冷却结晶操作中,为了得到
(5)提纯
(6)已知常温下,磷酸的电离常数
21-22高三上·广东·阶段练习
类题推荐
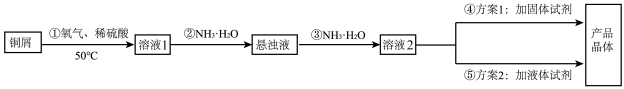
为充分利用资源,变废为宝,实验室里利用废铁屑制取硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]。某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。

已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。请回答下列问题:
(1)步骤②中,H2C2O4稍过量的主要原因是________ 。
(2)为了提高步骤③得到的FeC2O4·2H2O的纯度,宜用________ (填“热水”“冷水”或“无水乙醇”)洗涤,检验洗涤是否干净的操作是________ 。
(3)实现步骤④必须用到的两种仪器是________ (供选仪器:a. 烧杯;b. 坩埚;c. 蒸馏烧瓶;d. 高温炉;e. 表面皿;f. 锥形瓶)。
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________ 。
(5)硫酸亚铁铵是重要的工业原料,其溶解性如表所示:
(注意:高于73.3℃,FeSO4·7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸铵为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,______ ,冷却,过滤,用蒸馏水洗涤铁屑至中性,将铁屑置于锥形瓶中,_____ 至铁屑完全溶解,_____ ,冷却结晶,用无水乙醇洗涤2~3次,低温干燥。[实验中必须使用的试剂:铁屑、1.0 mol·L-1的Na2CO3溶液、3.0 mol·L-1的H2SO4溶液,饱和(NH4)2SO4溶液]

已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。请回答下列问题:
(1)步骤②中,H2C2O4稍过量的主要原因是
(2)为了提高步骤③得到的FeC2O4·2H2O的纯度,宜用
(3)实现步骤④必须用到的两种仪器是
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是
(5)硫酸亚铁铵是重要的工业原料,其溶解性如表所示:
| 10 | 20 | 30 | 40 | 50 | 60 | |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4·7H2O | 40.0 | 48.0 | 60.0 | 73.3 | — | — |
| (NH4)2Fe(SO4)2·6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(注意:高于73.3℃,FeSO4·7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸铵为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网