解答题-原理综合题 较难0.4 引用1 组卷263
二甲醚是一种十分重要的化工原料,可用来制杀虫剂、抛光剂、防锈剂、烷基化剂、溶剂等,工业上利用“一步法”合成二甲醚的总反应为2CO(g)+4H2(g)  CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:
CH3OCH3(g)+H2O(g) ΔH=—221.51 kJ·mol-1,回答下列问题:
(1)600 °C时,在复合催化剂CuO/ZnO/Al2O3上合成二甲醚的过程如下:
ⅰ.合成气合成甲醇:CO(g) +2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
ⅱ.甲醇脱水生成二甲醚:2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1
CH3OCH3(g)+H2O(g)ΔH2=—20.59 kJ·mol-1
ⅲ.水煤气变换反应:CO(g)+H2O(g) CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1
CO2(g)+ H2(g) ΔH3=—38.7 kJ·mol-1
①ΔH1=___________ kJ·mol-1。
②传统合成法将反应i、ii分别在不同的反应器中进行,“一步法”连续发生以上i、ii、iii三步反应,“一步法”的优点是___________ 。
(2)实验室模拟上述“一步法”合成过程,在1 L容器中充入6 molCO和6 mol H2,t h后达到平衡,测得混合体系中各组分浓度如下表:
平衡后,整个过程中CO的转化率为___________ ,第ii步反应放出的热量为___________ kJ(保留一位小数),v(CH3OCH3)=___________ mol· L-1·h-1,第ii步反应的K=___________ (保留两位小数)。
(3)第iii步反应机理中,调控反应条件,CO和OH在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理的两种不同途径如图所示。

分析图象可知,以上过程为___________ ( 填“放热”或“吸热”)过程,从第一步来看,___________ (填“氧化还原机理”或“羧基机理”)对合成有利,最终选择另一反应机理途径更有利的原因是___________ 。
(1)600 °C时,在复合催化剂CuO/ZnO/Al2O3上合成二甲醚的过程如下:
ⅰ.合成气合成甲醇:CO(g) +2H2(g)
ⅱ.甲醇脱水生成二甲醚:2CH3OH(g)
ⅲ.水煤气变换反应:CO(g)+H2O(g)
①ΔH1=
②传统合成法将反应i、ii分别在不同的反应器中进行,“一步法”连续发生以上i、ii、iii三步反应,“一步法”的优点是
(2)实验室模拟上述“一步法”合成过程,在1 L容器中充入6 molCO和6 mol H2,t h后达到平衡,测得混合体系中各组分浓度如下表:
| 物质 | H2 | CH3OH | H2O | CO2 |
| 物质的量浓度/(mol· L-1) | 1.956 | 0.72 | 0.084 | 0.756 |
平衡后,整个过程中CO的转化率为
(3)第iii步反应机理中,调控反应条件,CO和OH在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理的两种不同途径如图所示。

分析图象可知,以上过程为
20-21高三上·河北衡水·阶段练习
类题推荐
二甲醚(CH3OCH3)是重要的化工原料,可用CO和H2制得,总反应的热化学方程式如下。
2CO (g) +4H2 (g) CH3OCH3 (g)+ H2O (g) ΔH = -206.0 kJ/mol
CH3OCH3 (g)+ H2O (g) ΔH = -206.0 kJ/mol
工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行:
i.甲醇合成反应:
ii.甲醇脱水反应:2CH3OH (g) CH3OCH3 (g)+ H2O (g),ΔH = -24.0 kJ/mol
CH3OCH3 (g)+ H2O (g),ΔH = -24.0 kJ/mol
(1)起始时向容器中投入2 mol CO和4 mol H2,测得某时刻上述总反应中放出的热量为51.5kJ,此时CO的转化率为_______ 。
(2)请补全甲醇合成反应的热化学方程式:_______ 。
(3)甲醇脱水反应2CH3OH (g) CH3OCH3 (g)+ H2O (g) 在某温度下的化学平衡常数为400.此温度下,在恒容密闭容器中加入一定量的CH3OH(g),测得某时刻各组分浓度如下表所示。此时反应
CH3OCH3 (g)+ H2O (g) 在某温度下的化学平衡常数为400.此温度下,在恒容密闭容器中加入一定量的CH3OH(g),测得某时刻各组分浓度如下表所示。此时反应_______ (填“已达到”或“未达到”)化学平衡状态。
(4)生产二甲醚的过程中存在以下副反应,与甲醇脱水反应形成竞争:
CH3OH(g)+H2O(g) CO2(g) +3H2 (g) ΔH = +48.8 kJ/mol
CO2(g) +3H2 (g) ΔH = +48.8 kJ/mol
将反应物混合气按进料比n(CO)∶n(H2) = 1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得二甲醚的选择性分别如图1、图2所示。
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。
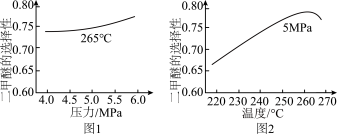
①图1中,温度一定,压强增大,二甲醚选择性增大的原因是_______ 。
②图2中,温度高于265℃后,二甲醚选择性降低的原因有_______ 。
2CO (g) +4H2 (g)
工业中采用“一步法”,通过复合催化剂使下列甲醇合成和甲醇脱水反应同时进行:
i.甲醇合成反应:
ii.甲醇脱水反应:2CH3OH (g)
(1)起始时向容器中投入2 mol CO和4 mol H2,测得某时刻上述总反应中放出的热量为51.5kJ,此时CO的转化率为
(2)请补全甲醇合成反应的热化学方程式:
(3)甲醇脱水反应2CH3OH (g)
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol/L) | 0.02 | 0.4 | 0.4 |
CH3OH(g)+H2O(g)
将反应物混合气按进料比n(CO)∶n(H2) = 1∶2通入反应装置,选择合适的催化剂。在不同温度和压强下,测得二甲醚的选择性分别如图1、图2所示。
资料:二甲醚的选择性是指转化为二甲醚的CO在全部CO反应物中所占的比例。

①图1中,温度一定,压强增大,二甲醚选择性增大的原因是
②图2中,温度高于265℃后,二甲醚选择性降低的原因有
二甲醚又称甲醚,是一种十分重要的化工原料,在制药、燃料、农药等化学工业中有许多独特的用途。一定条件下,利用合成气(CO、H2)合成二甲醚,其中主要包括以下三个相互联系的反应:
i.合成气合成甲醇:CO(g) +2H2 (g) CH3OH(g);
CH3OH(g);
ii.甲醇脱水生成二甲醚:2CH3OH(g) CH3OCH3(g)+ H2O(g);
CH3OCH3(g)+ H2O(g);
iii.水煤气变换反应:CO(g)+ H2O(g) CO2(g)+ H2(g)。
CO2(g)+ H2(g)。
请回答下列问题:
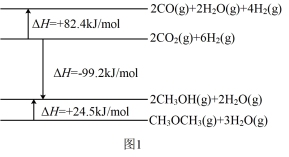
(1)已知相关物质变化的焓变如图1所示,写出CO直接加氢合成二甲醚的热化学方程式:_______ 。
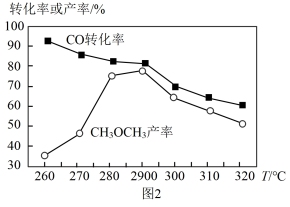
(2)有研究者在催化剂(CuO/ZnO/Al2O3)、压强为5.0 MPa的条件下,由CO和H2直接制备二甲醚,结果如图2所示,其中CO转化率随温度升高而降低的原因是_______ 。
(3)实验室模拟上述合成过程,在1 L恒容密闭容器中充入6 mol CO和6 mol H2,连续发生以上i、ii、iii反应,2 h后达到平衡,测得混合体系中各组分浓度如下表:
①平衡后,整个过程中CO的转化率为_______ ;v(CH3OCH3)=_______ mol· L-1· h-1。
②反应ii的K=_______ (保留两位小数)。
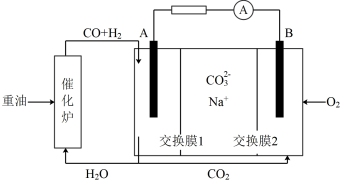
(4)合成气可做燃料电池的燃料。一种熔融盐燃料电池的工作原理如图所示,电极A上H2参与的电极反应为_______ ,假设催化炉产生的CO与H2的物质的量之比为2:1,电极A处产生的CO2有部分参与循环利用,其利用率为_______ 。
i.合成气合成甲醇:CO(g) +2H2 (g)
ii.甲醇脱水生成二甲醚:2CH3OH(g)
iii.水煤气变换反应:CO(g)+ H2O(g)
请回答下列问题:
(1)已知相关物质变化的焓变如图1所示,写出CO直接加氢合成二甲醚的热化学方程式:

(2)有研究者在催化剂(CuO/ZnO/Al2O3)、压强为5.0 MPa的条件下,由CO和H2直接制备二甲醚,结果如图2所示,其中CO转化率随温度升高而降低的原因是

(3)实验室模拟上述合成过程,在1 L恒容密闭容器中充入6 mol CO和6 mol H2,连续发生以上i、ii、iii反应,2 h后达到平衡,测得混合体系中各组分浓度如下表:
| 物质 | H2 | CH3OH | H2O | CO2 |
| 物质的量浓度/(mol·L-1) | l.44 | 0. 78 | 0. 12 | 0.84 |
②反应ii的K=
(4)合成气可做燃料电池的燃料。一种熔融盐燃料电池的工作原理如图所示,电极A上H2参与的电极反应为

(一)二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”。工业上以合成气(CO/H2)为原料“一步法”合成二甲醚的总反应为:2CO(g)+4H2(g)  CH3OCH3(g)+H2O(g) ΔH=﹣221.51 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=﹣221.51 kJ·mol-1
(1)600℃时,在复合催化剂CuO/ZnO/Al2O3作用下,反应器中发生了下列反应:
Ⅰ.合成气合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
Ⅱ.甲醇脱水生成二甲醚:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=﹣20.59 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=﹣20.59 kJ·mol-1
则ΔH1=___________ 。
(二)Ⅲ.水煤气变换反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=﹣38.7 kJ·mol-1
CO2(g)+H2(g) ΔH3=﹣38.7 kJ·mol-1
(2)一定条件下,CO的起始浓度为0.6 mol·L−1,10 min后反应I达到化学平衡,CO的平衡转化率为50%,则0~10 min H2的平均反应速率为___________ 。
(3)传统合成法将反应I和II分别在不同的反应器中进行,“一步法”连续发生以上三步反应。从物质转化和化学平衡的角度,分析“一步法”的优点是___________ 。
(4)反应Ⅲ,水煤气变换部分基元反应如下:
第②步基元反应逆反应的活化能为___________ eV。
(三)目前又有一种新合成二甲醚的方法是以CO2和H2为原料直接反应,其反应原理为:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH=﹣144.1 kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=﹣144.1 kJ·mol-1
(5)在___________ 下该反应能自发进行。
A.低温 B.高温 C.任何温度
(6)在恒容绝热密闭容器中,下列能判断该反应达到化学平衡状态的是___________。
(7)当 =3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示:
=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示:
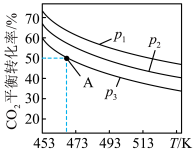
图中压强(p)从大到小顺序为___________。
(8)若在1 L密闭容器中充入0.2 mol CO2和0.6 mol H2,CO2的平衡转化率对应图1中A点,则在此温度下,该反应的化学平衡常数K=___________ (取整数)。
(9)合成二甲醚选用硅铝化合物作催化剂,硅铝比与产物选择性如图所示,A点和B点的化学平衡常数比较:KA___________ KB(选填“>”“<”或“=”),根据以上两条曲线,写出其中一条变化规律___________ 。

(1)600℃时,在复合催化剂CuO/ZnO/Al2O3作用下,反应器中发生了下列反应:
Ⅰ.合成气合成甲醇:CO(g)+2H2(g)
Ⅱ.甲醇脱水生成二甲醚:2CH3OH(g)
则ΔH1=
(二)Ⅲ.水煤气变换反应:CO(g)+H2O(g)
(2)一定条件下,CO的起始浓度为0.6 mol·L−1,10 min后反应I达到化学平衡,CO的平衡转化率为50%,则0~10 min H2的平均反应速率为
(3)传统合成法将反应I和II分别在不同的反应器中进行,“一步法”连续发生以上三步反应。从物质转化和化学平衡的角度,分析“一步法”的优点是
(4)反应Ⅲ,水煤气变换部分基元反应如下:
| 基元反应 | 活化能Ea(eV) | 反应热ΔH(eV) |
| ① CO+H2O+2*=CO*+H2O* | 0 | -1.73 |
| ② H2O*+*=H*+OH* | 0.81 | -0.41 |
(三)目前又有一种新合成二甲醚的方法是以CO2和H2为原料直接反应,其反应原理为:2CO2(g)+6H2(g)
(5)在
A.低温 B.高温 C.任何温度
(6)在恒容绝热密闭容器中,下列能判断该反应达到化学平衡状态的是___________。
| A.v正(CO2)=3v逆(H2) |
| B.容器内CH3OCH3体积分数不变 |
| C.容器内温度保持不变 |
| D.单位时间内断裂6 mol H—H键,同时断裂3 mol H—O键 |
(7)当

图中压强(p)从大到小顺序为___________。
| A.p1>p2>p3 | B.p3>p2>p1 | C.p2>p1>p3 | D.p3>p1>p2 |
(8)若在1 L密闭容器中充入0.2 mol CO2和0.6 mol H2,CO2的平衡转化率对应图1中A点,则在此温度下,该反应的化学平衡常数K=
(9)合成二甲醚选用硅铝化合物作催化剂,硅铝比与产物选择性如图所示,A点和B点的化学平衡常数比较:KA

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


