解答题-工业流程题 适中0.65 引用2 组卷41
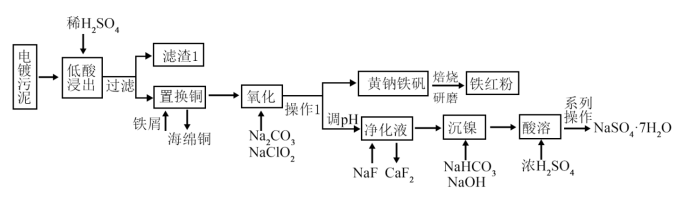
对电镀污泥(含Cu,Ca,Ni,Fe的氢氧化物)进行无害化和资源化处理,从其中回收金属、并制备硫酸镍的工艺流程如下图所示:
已知:氯酸不稳定,易发生歧化反应,可生成 气体。
气体。
(1)“低酸浸出”工序提高浸出率的措施为___________ (只写一条即可),实验室配制500mL 1.84mol/L该低酸溶液应量取质量分数为98%,密度为 的浓硫酸
的浓硫酸___________ mL。
(2)“氧化”工序中被氧化的元素为___________ (填元素符号),“氧化”工序中加入试剂 调pH的原因为
调pH的原因为___________ (结合离子方程式解释原因),写出氧化工序生成黄钠铁矾 的离子方程式
的离子方程式___________ 。
(3)控制净化液的pH不能过低,否则会导致 沉淀不完全,原因为
沉淀不完全,原因为___________ [ ,
, ]。
]。
(4)酸溶后的“系列操作”为___________ ,过滤、洗涤、干燥,该结晶工序得到的废液可以返回___________ 工序循环利用。
已知:氯酸不稳定,易发生歧化反应,可生成

(1)“低酸浸出”工序提高浸出率的措施为
(2)“氧化”工序中被氧化的元素为
(3)控制净化液的pH不能过低,否则会导致
(4)酸溶后的“系列操作”为
21-22高三上·江西抚州·阶段练习
类题推荐
电镀污泥[主要含 、
、 、
、 、
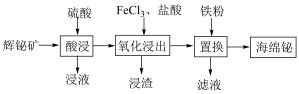
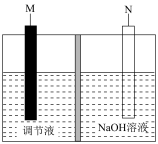
、 等]中铬镍资源再利用生产红矾钠(
等]中铬镍资源再利用生产红矾钠( )和粗镍,该工业流程如图。
)和粗镍,该工业流程如图。

已知:
① 、
、 、
、 、
、 的
的 依次为
依次为 、
、 、
、 、
、 ;
;
②Cr及其化合物的性质与Al类似;
③溶液中金属离子开始沉淀、沉淀完全和沉淀开始溶解的pH如下表所示:
请回答下列问题:
(1)若污泥中Cr以 的形式存在,则“①浸出”时发生反应的化学方程式为
的形式存在,则“①浸出”时发生反应的化学方程式为___________ 。
(2)“②除杂”时,若镍离子浓度为0.05mol/L,则溶液中 浓度范围为
浓度范围为___________ mol/L。
(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为___________ (用离子方程式表示)。
(4)“④氧化”步骤中包括先将 、
、 沉淀,过滤后溶液中继续加入NaOH溶液和
沉淀,过滤后溶液中继续加入NaOH溶液和 。沉淀
。沉淀 、
、 时,pH应控制的范围为
时,pH应控制的范围为___________ ,加入 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)操作Ⅲ为___________ 。
(6)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr元素回收率为___________ (结果保留一位小数)。

已知:
①
②Cr及其化合物的性质与Al类似;
③溶液中金属离子开始沉淀、沉淀完全和沉淀开始溶解的pH如下表所示:
| 金属离子 | ||||
| 开始沉淀时( | 7.2 | 4.9 | 3.7 | 2.2 |
| 沉淀完全时( | 8.7 | 6.8 | 4.7 | 3.2 |
| 沉淀开始溶解的pH | ― | 12.0 | 7.8 |
(1)若污泥中Cr以
(2)“②除杂”时,若镍离子浓度为0.05mol/L,则溶液中
(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为
(4)“④氧化”步骤中包括先将
(5)操作Ⅲ为
(6)若实验取干污泥250g,其中含Cr11.2%,实验所得晶体为59.6g,则Cr元素回收率为
氢氧化铍可用作核技术和制备含铍材料的中间体等。以硅铍石(主要成分Be2SiO4含少量Al2O3)和方解石(主要成分CaCO3,含少量FeCO3、SiO2)为原料,制备Be(OH)2的工艺流程如图所示:

已知:I.硅铍石不易被硫酸直接分解;铍的性质与铝相似;粗Be(OH)2含有少量Al(OH)3;
II.生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)“熔炼”时加入方解石粉的作用为_______ ;生成气体的电子式为_______ 。
(2)浸渣中除含有CaSiO3、H2SiO3外,还含有_______ (填化学式)。
(3)滤渣1中含有NH4Al(SO4)2·12H2O、(NH4)2 Fe(SO4)2·6H2O。NH4Al(SO4)2 ·12H2O能用作净水剂,原因为_______ (用离子方程式表示);(NH4)2 Fe(SO4)2·6H2O可用于测定KMnO4的含量,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)根据已知II信息可知,“深度除铁”的适宜方案为_______ 。
(5)“调pH”所得母液中的主要溶质可返回到_______ 工序循环利用。
(6)“洗涤”的目的是除去粗Be(OH)2中所含的Al(OH)3,若用足量NaOH浓溶液代替NaOH稀溶液,会导致的后果为_______ (用离子方程式表示)。

已知:I.硅铍石不易被硫酸直接分解;铍的性质与铝相似;粗Be(OH)2含有少量Al(OH)3;
II.生成氢氧化物沉淀的pH如下表所示:
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Be(OH)2 |
| 开始沉淀的pH | 7.7 | 2.5 | 3.5 | 4.6 |
| 沉淀完全的pH (溶液中金属离子浓度等于10-5 mol·L-1) | 8.7 | 3.2 | 4.7 | 5.9 |
回答下列问题:
(1)“熔炼”时加入方解石粉的作用为
(2)浸渣中除含有CaSiO3、H2SiO3外,还含有
(3)滤渣1中含有NH4Al(SO4)2·12H2O、(NH4)2 Fe(SO4)2·6H2O。NH4Al(SO4)2 ·12H2O能用作净水剂,原因为
(4)根据已知II信息可知,“深度除铁”的适宜方案为
(5)“调pH”所得母液中的主要溶质可返回到
(6)“洗涤”的目的是除去粗Be(OH)2中所含的Al(OH)3,若用足量NaOH浓溶液代替NaOH稀溶液,会导致的后果为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网