解答题-原理综合题 适中0.65 引用1 组卷106
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
(1)汽油的主要成分之一是辛烷[ ]。已知:25℃、101kPa时,1mol
]。已知:25℃、101kPa时,1mol 完全燃烧生成气态二氧化碳和液态水,放出5518kJ热量。该反应的热化学方程式为
完全燃烧生成气态二氧化碳和液态水,放出5518kJ热量。该反应的热化学方程式为______ 。
(2)已知:25℃、101kPa时,

相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是______ 。
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

根据图信息分析,与汽油相比,甲醇作为燃料的优点是______ 。
Ⅱ.甲醇的合成
(4)以 和
和 为原料合成甲醇,反应的能量变化如图所示。
为原料合成甲醇,反应的能量变化如图所示。
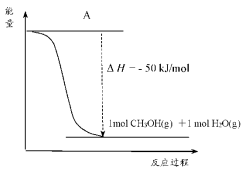
①补全图:图中A处应填入______ 。
②由图可知,该反应中反应物 和
和 的总能量
的总能量______ (填“大于”、“小于”或“等于”)生成物 和
和 的总能量。
的总能量。
(5)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由 合成1mol液态甲醇和1mol液态水将
合成1mol液态甲醇和1mol液态水将______ (填“吸收”或“放出”)______ kJ热量。
(6)已知:





以 和
和 为原料合成甲醇的反应为
为原料合成甲醇的反应为 。
。
该反应的 为
为______ kJ/mol。
(1)汽油的主要成分之一是辛烷[
(2)已知:25℃、101kPa时,
相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。

根据图信息分析,与汽油相比,甲醇作为燃料的优点是
Ⅱ.甲醇的合成
(4)以

①补全图:图中A处应填入
②由图可知,该反应中反应物
(5)已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由
(6)已知:
以
该反应的
20-21高一下·北京·期中
类题推荐
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:_____
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是_____ (填化学式)
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
则 X=_____ 。
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。
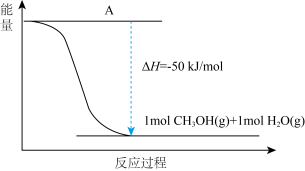
①补全上图:图中A 处应填入_____ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH_____ (填“变大”“变小”“不变”)。
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=_____ kJ·mol-1。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
| 化学键 | O=O | C-O | C=O | H-O | C-H |
| E/( kJ·mol-1) | X | 343 | 1076 | 465 | 413 |
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

①补全上图:图中A 处应填入
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=
甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为___ 。25℃,101KPa时CH3OH(l)+ O2(g)=CO2(g)+2H2O(l)ΔH=-726.5kJ·mol-1,相同质量的甲醇和辛烷分别燃烧时释放的热量用于煅烧石灰石制备CaO,则得到CaO多的是
O2(g)=CO2(g)+2H2O(l)ΔH=-726.5kJ·mol-1,相同质量的甲醇和辛烷分别燃烧时释放的热量用于煅烧石灰石制备CaO,则得到CaO多的是___ (填“甲醇”或“辛烷”)。
(2)CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-393kJ·mol-1,该反应相关化学键键能数据如下表:则X=___ 。
Ⅱ.甲醇的合成
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。___ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应ΔH___ (填“变大”、“变小”或“不变”)。
③已知:CO(g)+ O2(g)=CO2(g) ΔH1=-283kJ·mol-1
O2(g)=CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH2=-242kJ·mol-1
O2(g)=H2O(g) ΔH2=-242kJ·mol-1
CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH3=-676kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH3=-676kJ·mol-1
以CO(g)和H2(g)为原料合成甲醇的热化学方程式为___ 。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为
(2)CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-393kJ·mol-1,该反应相关化学键键能数据如下表:则X=
| 化学键 | O=O | C-O | C≡O | H-O | C-H |
| E/(kJ·mol-1) | 496 | 343 | 1076 | X | 413 |
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应ΔH
③已知:CO(g)+
H2(g)+
CH3OH(g)+
以CO(g)和H2(g)为原料合成甲醇的热化学方程式为
甲醇 作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷 。已知:25℃、101kPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为
。已知:25℃、101kPa时,0.2mol辛烷完全燃烧生成气态二氧化碳和液态水,放出1103.6kJ热量。该反应的热化学方程式为___________ 。
25℃、101kPa,
 ,相同质量的甲醇和辛烷分别燃烧释放热量多的是
,相同质量的甲醇和辛烷分别燃烧释放热量多的是___________ (填“甲醇”或“辛烷”)。
(2) 的结构式为
的结构式为

 ,该反应相关化学键键能数据如下表
,该反应相关化学键键能数据如下表
则
___________ 。
Ⅱ.甲醇的合成
(3)以 和
和 为原料合成甲醇,反应的能量变化如图。
为原料合成甲醇,反应的能量变化如图。___________ 。
②该反应需要加入铜锌基催化剂。
加入催化剂后,该反应的
___________ (填“变大”“变小”或“不变”)。
③已知:CO的燃烧热为




以 和
和 为原料合成甲醇的热化学方程式为
为原料合成甲醇的热化学方程式为___________ 。
Ⅰ.甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷
25℃、101kPa,
(2)

| 化学键 | O=O | C—O | C≡O | H—O | C—H |
| 496 | 343 | 1076 | X | 413 |
Ⅱ.甲醇的合成
(3)以

②该反应需要加入铜锌基催化剂。
加入催化剂后,该反应的
③已知:CO的燃烧热为
以
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


