解答题-原理综合题 较难0.4 引用2 组卷397
大气污染是中国第一大环境污染问题,氮和硫的氧化物排放是造成大气污染的原因之一,研究它们的反应机理,对于消除环境污染有重要意义。
(1)汽车尾气中的 由如下反应产生:
由如下反应产生:


已知:

则

___________ 
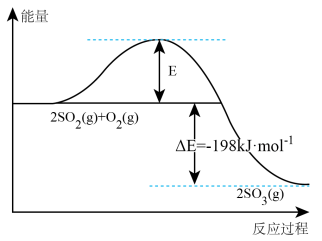
(2) 反应过程中能量变化如图所示。在
反应过程中能量变化如图所示。在 存在时,该反应的机理为:
存在时,该反应的机理为:
第一步: (快) 第二步:
(快) 第二步: (慢)
(慢)
下列说法正确的是___________(填序号)。
(3) 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表所示:
浓度随时间的变化如表所示:
① 内用
内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为___________ 。
②一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是___________ 。
A. 和
和 的浓度比保持不变 B.容器中压强不再变化
的浓度比保持不变 B.容器中压强不再变化
C. D.气体的密度保持不变
D.气体的密度保持不变
(4)某小组研究某恒容密闭容器中,在不同温度下,氮硫的氧化物之间的转化情况如图所示,已知 ,实验初始时体系中的
,实验初始时体系中的 和
和 相等、
相等、 和
和 相等,其中P表示各气体的分压。
相等,其中P表示各气体的分压。
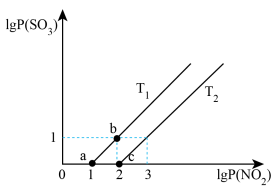
①
___________  (填“>”“<”或者“=”);温度为
(填“>”“<”或者“=”);温度为 时化学平衡常数
时化学平衡常数
___________ 。
②由平衡状态a到b,改变的条件是___________ 。
(1)汽车尾气中的
已知:
则
(2)
第一步:
下列说法正确的是___________(填序号)。

| A.反应速率主要取决于第一步 | B. |
| C.逆反应的活化能大于 | D.增大 |
| 0 | 1 | 2 | 3 | 4 | 5 | |
| 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①
②一定温度下,在恒容密闭容器中充入一定量
A.
C.
(4)某小组研究某恒容密闭容器中,在不同温度下,氮硫的氧化物之间的转化情况如图所示,已知

①
②由平衡状态a到b,改变的条件是
21-22高三上·重庆九龙坡·阶段练习
类题推荐
大气污染是中国第一大环境污染问题,氮和硫的氧化物排放是造成大气污染的原因之一,研究它们的反应机理,对于消除环境污染有重要意义。
(1)汽车尾气中的 由如下反应产生:
由如下反应产生:


已知:

则

_______ 
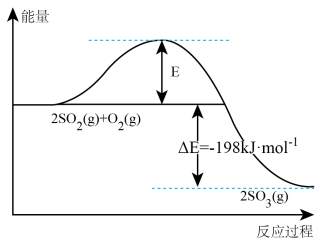
(2) 反应过程中能量变化如图所示。在
反应过程中能量变化如图所示。在 存在时,该反应的机理为:
存在时,该反应的机理为:
第一步: (快)
(快)
第二步: (慢)
(慢)
下列说法正确的是_______(填序号)。
(3) 在一定条件下可发生分解反应:
在一定条件下可发生分解反应: ,某温度下向恒容密闭容器中加入一定量
,某温度下向恒容密闭容器中加入一定量 ,测得
,测得 浓度随时间的变化如表所示:
浓度随时间的变化如表所示:
① 内用
内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为_______ 。
②一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是
进行该反应,能判断反应已达到化学平衡状态的是_______ 。
A. 和
和 的浓度比保持不变 B.容器中压强不再变化
的浓度比保持不变 B.容器中压强不再变化
C. D.气体的密度保持不变
D.气体的密度保持不变
(4)氢气作为一种理想燃料,但不利于贮存和运输。利用氢能需要选择合适的储氢材料,镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g)⇌LaNi5H6(s) ΔH<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
(5)含乙酸钠和对氯酚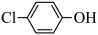 的废水可以利用微生物电池除去,其原理如图所示:
的废水可以利用微生物电池除去,其原理如图所示:
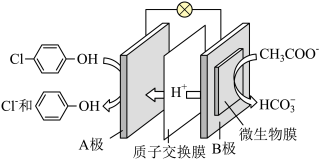
①B是电池的_______ 极(填“正”或“负”);
②A极的电极反应式为_______ 。
(1)汽车尾气中的
已知:
则
(2)
第一步:
第二步:
下列说法正确的是_______(填序号)。

| A.反应速率主要取决于第一步 | B. |
| C.逆反应的活化能大于 | D.增大 |
| 0 | 1 | 2 | 3 | 4 | 5 | |
| 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量
A.
C.
(4)氢气作为一种理想燃料,但不利于贮存和运输。利用氢能需要选择合适的储氢材料,镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g)⇌LaNi5H6(s) ΔH<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是_______(填字母编号)。
| A.增加LaNi5H6(s)的量 | B.升高温度 |
| C.使用催化剂 | D.减小压强 |
 的废水可以利用微生物电池除去,其原理如图所示:
的废水可以利用微生物电池除去,其原理如图所示:
①B是电池的
②A极的电极反应式为
氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)碘蒸气的存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________
(2)对反应 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
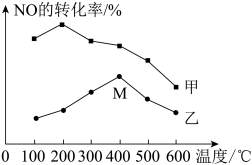
图中M点对应的速率(对应温度 )
)
___________  (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是___________ 。
(3)在密闭容器中充入 和
和 ,发生反应:
,发生反应: 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。

①下列物理量中,图中d点大于b点的是___________ (填字母)。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为___________ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的___________ 点。
(4) 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、 ,发生反应:
,发生反应:
 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示:
① 内该反应的平均反应速率
内该反应的平均反应速率
___________  。
。
②该温度下反应的平衡常数
___________  (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(1)碘蒸气的存在能大幅度提高
第一步:
第二步:
第三步:
实验表明,含碘时
| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
| C. |
| D. |
(2)对反应

图中M点对应的速率(对应温度
(3)在密闭容器中充入

①下列物理量中,图中d点大于b点的是
A.正反应速率 B.逆反应速率
C.
②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的
(4)
| 0 | 10 | 20 | 30 | 40 | |
| 240 | 226 | 216 | 210 | 210 |
②该温度下反应的平衡常数
氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)碘蒸汽的存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。
下列表述正确的是___________
(2)对反应
 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
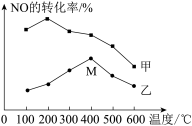
图中M点对应的速率(对应温度400℃)
___________  (填“>”、“<”或“=”),温度高于400℃,NO转化率降低的原因可能是
(填“>”、“<”或“=”),温度高于400℃,NO转化率降低的原因可能是___________ 。
(3)在密闭容器中充入4molNO和5mol ,发生反应:
,发生反应: 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。
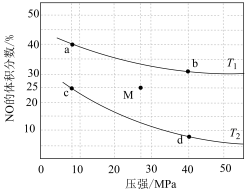
①下列物理量中,图中d点大于b点的是___________ (填字母)。
A. B.
B. 的浓度 C.对应温度的平衡常数
的浓度 C.对应温度的平衡常数
②c点NO的平衡转化率为___________ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的___________ 点。
(4)T℃时,向容积为2L的恒容容器中充入0.4molNO、0.8mol ,发生反应:
,发生反应: ,体系的总压强p随时间t的变化如下表所示:
,体系的总压强p随时间t的变化如下表所示:
①0~20min内该反应的平均反应速率v(NO)=___________  。
。
②该温度下反应的平衡常数
___________  (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(1)碘蒸汽的存在能大幅度提高
第一步:
第二步:
第三步:
实验表明,含碘时
下列表述正确的是___________
| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
| C.IO为反应的催化剂 |
| D. |
(2)对反应

图中M点对应的速率(对应温度400℃)
(3)在密闭容器中充入4molNO和5mol

①下列物理量中,图中d点大于b点的是
A.
②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的
(4)T℃时,向容积为2L的恒容容器中充入0.4molNO、0.8mol
| t/min | 0 | 10 | 20 | 30 | 40 |
| p/kPa | 240 | 226 | 216 | 210 | 210 |
②该温度下反应的平衡常数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


