解答题-实验探究题 适中0.65 引用1 组卷187
苯胺(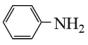 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为:
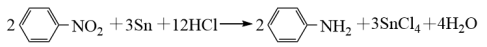
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐 。
。
乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为_______ 。
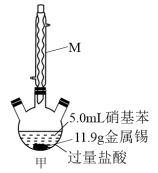
(2)图甲中 装置的名称为
装置的名称为_______ ,往硝基苯中加入 和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量
和足量盐酸充分还原生成盐,冷却后,往混合物中加入过量 溶液得碱化液。加
溶液得碱化液。加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为_______ 。
(3)分离提纯:
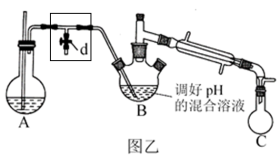
步骤i.如图乙,加热装置 产生水蒸气,采用水蒸气蒸馏的方法,用
产生水蒸气,采用水蒸气蒸馏的方法,用热的水蒸气 将 中的苯胺逐渐吹出至
中的苯胺逐渐吹出至 中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
中(收集到苯胺及水的混合液体),从混合物中分离出粗苯胺及水溶液。
步骤ⅱ.步骤i所得水溶液中加 至饱和,用乙醚萃取得萃取液与粗苯胺合并。
至饱和,用乙醚萃取得萃取液与粗苯胺合并。
步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺 。
。
①图乙中T型管 处方框区域玻璃导管不宜过长,原因是
处方框区域玻璃导管不宜过长,原因是_______ 。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是_______ 。步骤ⅲ中干燥剂可以选用_______ (填序号)
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为_______ 左右。
④该实验中所得苯胺的产率为_______ (保留三位有效数字)。
 )是重要的化工原料,其制备原理为:
)是重要的化工原料,其制备原理为: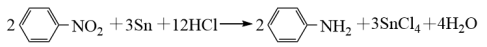
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐
 。
。乙醚为极易挥发的液体,是用途广泛的有机溶剂,与空气接触会形成易爆混合物。部分物质物理性质见表:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 溶解性 | 密度 |
| 苯胺 | 微溶于水,易溶于乙醚 | ||||
| 硝基苯 | 难溶于水,易溶于乙醚 | ||||
| 乙醚 | 微溶于水 |
(1)实验室用苯制取硝基苯的化学方程式为
(2)图甲中

(3)分离提纯:

步骤i.如图乙,加热装置
步骤ⅱ.步骤i所得水溶液中加
步骤ⅲ.合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度T时的馏分得到苯胺
①图乙中T型管
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是
a.浓硫酸 b.五氧化二磷 c.碱石灰
③步骤ⅲ中蒸馏获得苯胺需控制温度为
④该实验中所得苯胺的产率为
21-22高三上·黑龙江哈尔滨·阶段练习
类题推荐
苯胺(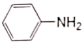 )是重要的化工原料,其制备原理为:2
)是重要的化工原料,其制备原理为:2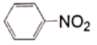 +3Sn+12HCl
+3Sn+12HCl 2
2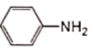 +3SnCl4+4 H2O
+3SnCl4+4 H2O
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐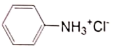 ;部分物质物理性质见下表:
;部分物质物理性质见下表:
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为___________ 。
(2)往硝基苯中加入 和足量盐酸充分还原,冷却后,往混合物中加入过量
和足量盐酸充分还原,冷却后,往混合物中加入过量 溶液得碱化液,加
溶液得碱化液,加 溶液的主要目的是析出苯胺,反应的离子方程式为
溶液的主要目的是析出苯胺,反应的离子方程式为___________ 。
(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加 至饱和,用乙醚萃取得萃取液与粗苯胺合并:
至饱和,用乙醚萃取得萃取液与粗苯胺合并:
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度 时的馏分得到苯胺。
时的馏分得到苯胺。
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是___________ 。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是___________ 。如果没有步骤ⅱ,苯胺的产率___________ (填“不变”、“增大”或“减小”)。步骤ⅲ中干燥剂可以选用___________ (填序号)
a.浓硫酸 b.五氧化二磷 c. 固体
固体
③步骤ⅲ中蒸馏获得苯胺的温度 的范围为
的范围为___________ 。
(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
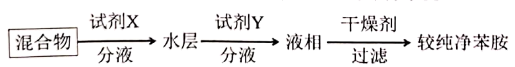
试剂 是
是___________ ,试剂 是
是___________ ,“液相”是___________ (填“水层”或“有机层”)
 )是重要的化工原料,其制备原理为:2
)是重要的化工原料,其制备原理为:2 +3Sn+12HCl
+3Sn+12HCl +3SnCl4+4 H2O
+3SnCl4+4 H2O已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐
 ;部分物质物理性质见下表:
;部分物质物理性质见下表:| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/ |
| 苯胺 | 184 | 微溶于水,易溶于乙醚 | 1.02 | |
| 硝基苯 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | 34.6 | 微溶于水 | 0.7134 |
(1)实验室用苯制取硝基苯的化学方程式为
(2)往硝基苯中加入
(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是
a.浓硫酸 b.五氧化二磷 c.
③步骤ⅲ中蒸馏获得苯胺的温度
(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:

试剂
苯胺(C6H5NH2)是重要的化工原料,可合成染料、药物、树脂等,也可作为橡胶硫化促进剂;苯胺是三类致癌物;尽量避免接触皮肤及蒸汽吸入。实验室拟制取及提纯苯胺,且已知有关信息如下:
①C6H5NH2与NH3类似,与盐酸反应生成易溶于水的盐酸苯胺(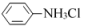 )。
)。
②用金属Sn和盐酸还原硝基苯制得苯胺的反应如下:2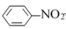 +3Sn+12HCl
+3Sn+12HCl 2
2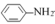 +3SnCl2+4H2O
+3SnCl2+4H2O
③下表为某些物质的物理性质(密度为实验条件温度下所测):
步骤I制备苯胺:
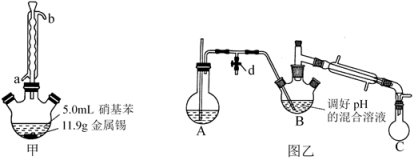
向如图甲所示的装置中,加入过量的20mL浓盐酸、11.9g金属Sn、5.00mL硝基苯,在热水浴中充分反应约30min;冷却后向三颈烧瓶中加入足量的NaOH溶液至呈碱性。
(1)在进行苯胺的有关实验时,必须戴硅橡胶手套,宜在___________ 中进行。
(2)图甲中,除了三颈烧瓶外,另一种仪器是___________ ,其作用是___________ ,冷却水从___________ 进,___________ 出(填:a或b)。
(3)加入NaOH溶液与有机物反应的离子方程式是___________ 。
步骤Ⅱ提纯苯胺:
①取出上图甲中的三瓶烧瓶,改为如图乙所示的装置。加热装置A产生水蒸气,采用水蒸气蒸馏的方法,将B中的苯胺逐渐吹出至C中(收集到苯胺及水的混合液体);从混合中分离出粗苯胺及水溶液x。
②向所得的水溶液x中加入固体NaCl至饱和,再用乙醚萃取,得到乙醚的萃取液。
③合并粗苯胺及乙醚的萃取液,用固体KOH干燥后,取干燥后的液体进行蒸馏得到得到2.00mL苯胺。
(4)装置A中玻璃管的作用是___________ 。
(5)该实验中所得苯胺的产率为___________ (保留三位有效数字)。
①C6H5NH2与NH3类似,与盐酸反应生成易溶于水的盐酸苯胺(
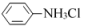 )。
)。②用金属Sn和盐酸还原硝基苯制得苯胺的反应如下:2
 +3Sn+12HCl
+3Sn+12HCl +3SnCl2+4H2O
+3SnCl2+4H2O③下表为某些物质的物理性质(密度为实验条件温度下所测):
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/g·mL-1 |
| 苯胺 | 93 | -6.2 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 123 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | 74 | -116.2 | 34.6 | 微溶于水 | 0.713 |
向如图甲所示的装置中,加入过量的20mL浓盐酸、11.9g金属Sn、5.00mL硝基苯,在热水浴中充分反应约30min;冷却后向三颈烧瓶中加入足量的NaOH溶液至呈碱性。

(1)在进行苯胺的有关实验时,必须戴硅橡胶手套,宜在
(2)图甲中,除了三颈烧瓶外,另一种仪器是
(3)加入NaOH溶液与有机物反应的离子方程式是
步骤Ⅱ提纯苯胺:
①取出上图甲中的三瓶烧瓶,改为如图乙所示的装置。加热装置A产生水蒸气,采用水蒸气蒸馏的方法,将B中的苯胺逐渐吹出至C中(收集到苯胺及水的混合液体);从混合中分离出粗苯胺及水溶液x。
②向所得的水溶液x中加入固体NaCl至饱和,再用乙醚萃取,得到乙醚的萃取液。
③合并粗苯胺及乙醚的萃取液,用固体KOH干燥后,取干燥后的液体进行蒸馏得到得到2.00mL苯胺。
(4)装置A中玻璃管的作用是
(5)该实验中所得苯胺的产率为
苯胺(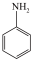 )是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
)是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
已知:① 与NH3相似,与盐酸反应生成
与NH3相似,与盐酸反应生成 (易溶于水的盐)。
(易溶于水的盐)。
②用硝基苯制取苯胺的反应为:2 +3Sn+12HCl
+3Sn+12HCl 2
2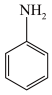 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
Ⅰ.制备苯胺
图1所示装置中加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,向三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。
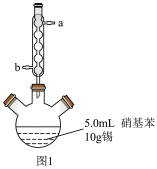
(1)滴加适量NaOH溶液的目的是___ ,写出主要反应的离子方程式___ 。
Ⅱ.纯化苯胺
ⅰ.取出图l所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气。用“水蒸气蒸馏”的方法把B中苯胺逐渐吹出,在烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液甲。
ⅱ.向所得水溶液甲中加入氯化钠固体至饱和,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺1.86g。

(2)装置A中玻璃管的作用是__ 。
(3)在苯胺吹出完毕后,应进行的操作是先__ ,再___ 。
(4)该实验中苯胺的产率为___ (保留三位有效数字)。
(5)欲在不加热条件下除去苯胺中少量的硝基苯杂质,简述实验方案___ 。
 )是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
)是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。已知:①
 与NH3相似,与盐酸反应生成
与NH3相似,与盐酸反应生成 (易溶于水的盐)。
(易溶于水的盐)。②用硝基苯制取苯胺的反应为:2
 +3Sn+12HCl
+3Sn+12HCl +3SnCl4+4H2O
+3SnCl4+4H2O③有关物质的部分物理性质见下表:
| 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/g·cm-3 |
| 苯胺 | 93 | 6.3 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 123 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | 74 | 116.2 | 34.6 | 微溶于水 | 0.7134 |
图1所示装置中加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,向三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。

(1)滴加适量NaOH溶液的目的是
Ⅱ.纯化苯胺
ⅰ.取出图l所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气。用“水蒸气蒸馏”的方法把B中苯胺逐渐吹出,在烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液甲。
ⅱ.向所得水溶液甲中加入氯化钠固体至饱和,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺1.86g。

(2)装置A中玻璃管的作用是
(3)在苯胺吹出完毕后,应进行的操作是先
(4)该实验中苯胺的产率为
(5)欲在不加热条件下除去苯胺中少量的硝基苯杂质,简述实验方案
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


