多选题 适中0.65 引用1 组卷93
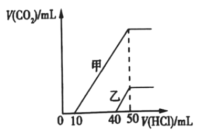
向体积均为10mL、物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是
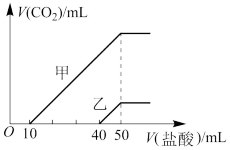

| A.原NaOH溶液的物质的量浓度为 0.5mol/L |
| B.当0<V(盐酸)<10mL时,甲溶液中发生反应的离子方程式为H++ CO |
| C.乙溶液中含有的溶质是Na2CO3和NaOH且二者物质的量比值是3:1 |
| D.向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224mL |
21-22高三上·陕西渭南·阶段练习
类题推荐
取一定物质的量浓度的NaOH溶液,体积为50mL,向其中通入一定量的CO2后,再稀释到100mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如图,下列说法正确的是
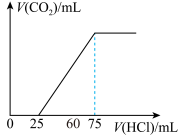

| A.原NaOH溶液的物质的量浓度0.15mol/L |
| B.溶液通入CO2后,所得溶质为NaOH和Na2CO3且物质的量之比为1:3 |
| C.所得溶质为Na2CO3和NaHCO3且物质的量之比为1:1 |
| D.通入的CO2的体积为33.6mL |
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是


| A.OA段所发生反应的离子方程式:H+ + OH-= H2O |
| B.产生的CO2体积(标准状况下)为0.056 L |
| C.原NaOH溶液的物质的量浓度为0.75 mol·L-1 |
| D.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网